
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Методика визначення перманганатної окисності води
1.Щоб уникнути помилок, пов’язаних з випадковим забрудненням скляних колб домішками, здатними до окиснення, перед визначенням окисності води в колбу наливають 100–150 мл концентрованого розчину перманганату калію, підкисленого сульфатною кислотою, закривають колбу лійкою і кип’ятять протягом 3–5 хвилин. Якщо на стінках колби з’являться коричневі плями MnO2, то вміст колби зливають, а колбу спочатку обробляють концентрованою хлоридною кислотою, а потім дистильованою водою і знов кип’ятять з тим же концентрованим розчином перманганату калію. Цю операцію повторюють 2–3 раза, після чого ополіскують колбу дистильованою водою. 2. У заздалегідь підготовлену конічну колбу ємкістю 250 мл піпеткою вміщують 100 мл досліджуваної води, додають 5 мл сульфатної кислоти (1:3) і доливають з бюретки точно 20 мл 0,01 н. розчину 3. Колбу закривають годинниковим склом (для запобігання випаровування води) і кип’ятять 10 хвилин від початку закипання. Щоб не було бурхливого кипіння, в колбу слід вмістити скляні капіляри. Час кип’ятіння потрібно витримувати точно. Під час кип’ятіння спостерігають за забарвленням розчину: · якщо забарвлення розчину в процесі кип’ятіння помітно послабшає, слід додати декілька мілілітрів робочого розчину перманганату калію до появи стійкого інтенсивно рожевого забарвлення, що не зникає при кип’ятінні. · якщо в процесі кип’ятіння розчин буріє, то це свідчить про нестачу сульфатної кислоти. В цьому разі необхідно до розчину додати 5 мл сульфатної кислоти (1:3). · якщо вище перелічені заходи не допомогли, пробу води необхідно розбавити. 4. Після кип’ятіння до гарячого розчину додають 20 мл 0,01 н. розчину оксалатної кислоти 5. Паралельно проводять порівняльний (холостий) дослід. Для цього беруть 100 мл дистильованої води й обробляють її аналогічно як воду, що досліджують. Витрата перманганату калію на титрування дистильованої води не повинна перевищувати 0,3 мл.
Розрахунок перманганатної окисності води (Х) здіснюють за формулою
де V1 – об’єм робочого розчину 8 – молярна маса еквіваленту кисню; г/моль.
Перманганатна окисність питної води, згідно з ДСАНПіН 383– 96, не повинна бути більшою за 4 мг О/л. Лабораторна робота № 16
|
|||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 76; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.142.171.180 (0.005 с.) |
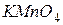
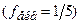 . При цьому розчин повинен набути інтенсивного рожевого забарвлення.
. При цьому розчин повинен набути інтенсивного рожевого забарвлення.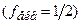 . Об’єм розчину
. Об’єм розчину 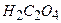 повинен чітко дорівнювати об’єму доданого об’єму робочого розчину KMnO4. Розчин збовтують і одразу титрують робочим розчином KMnO4 до появи блідо-рожевого забарвлення, що не зникає протягом 1–2 хвилин. Дослід вважається досконалим, якщо на титрування надлишку оксалатної кислоти йде не більше 7 и не менше 2 мл розчину перманганату калію.
повинен чітко дорівнювати об’єму доданого об’єму робочого розчину KMnO4. Розчин збовтують і одразу титрують робочим розчином KMnO4 до появи блідо-рожевого забарвлення, що не зникає протягом 1–2 хвилин. Дослід вважається досконалим, якщо на титрування надлишку оксалатної кислоти йде не більше 7 и не менше 2 мл розчину перманганату калію.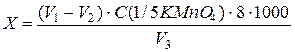 мг О/л,
мг О/л, Обчислення виконують з точністю
Обчислення виконують з точністю 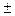 0,1 мг.
0,1 мг.


