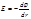Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Термодинамические свойства ионов в растворе. Термодинамика ионной сольватации. Модель Борна.
Термодинамические свойства ионов Термодинамический метод позволяет изучить свойства реальных систем без рассмотрения составляющих их частиц и взаимодействий между ними. При этом все особенности внутреннего строения систем в суммарной форме охватываются термодинамическими величинами (ΔfH, ΔfG, Ср и т.д.) Любая функция состояния полностью диссоциированного электролита AmBn представляет сумму, например в стандартном состоянии:
Для упрощения громоздкое указание стандартного состояния ионов заменяют более простым (р-р; Н2O).
Таким же путем можно рассчитать стандартную энергию Гиббса образования раствора АnBm,
Термодинамика ионной сольватации *В общем виде энтальпию сольватации (энергию сольватации) можно представить как выигрыш в энергии при переносе 1 моль исследуемых ионов из вакуума в данный растворитель. *При этом предполагается, что такой выигрыш энергии не включает в себя электростатическое взаимодействие ионов, которое неизбежно бы сказалось при введении в растворитель второго и последующих ионов. *Чтобы избежать этого осложнения, раствор нужно поддерживать электронейтральным, т.е. вводить в него соответствующее количество ионов противоположного знака, а взаимное притяжение катионов и анионов исключить (теоретически бесконечным) разбавлением Модель Борна Согласно модели М. Борна ион рассматривается как заряженный шарик радиусом ri, а растворитель как сплошная однородная среда с диэлектрической проницаемостью ε. Процесс переноса шарика из вакуума в среду разбивается на 3 этапа: 1.Разряд шарика в вакууме 2.Перенос незаряженного шарика из вакуума в растворитель 3.Заряжение шарика в
(Продолжение 3) *При этом предполагается, что работа на втором этапе равна нулю, а для расчета работы на этапах 1 и 3 используется закон Кулона
где φ – потенциал на Напряженность поля связана с электрическим потенциалом как: Теория Борна является приближенной, и рассчитанные энергии сольватации лишь качественно правильно отражают зависимости от заряда и радиуса ионов. Для получения корректных данных нужно учесть структуру растворителя, а также различные силы взаимодействия, кроме электростатических
|
|||||||||||||||||
|
Последнее изменение этой страницы: 2020-11-23; просмотров: 172; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.222.200.143 (0.005 с.) |
||||||||||||||||||
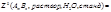
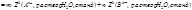
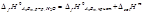 *Зная стандартную энтальпию образования кристаллического соединения, можно найти энтальпию образования вещества в стандартном состоянии в водном растворе, определив энтальпию растворения этого соединения в воде Δsol H∞:
*Зная стандартную энтальпию образования кристаллического соединения, можно найти энтальпию образования вещества в стандартном состоянии в водном растворе, определив энтальпию растворения этого соединения в воде Δsol H∞: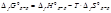 Стандартные термодинамические свойства ионов, как
Стандартные термодинамические свойства ионов, как 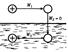 Электрическая работа заряжения сферы равна:
Электрическая работа заряжения сферы равна: