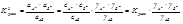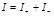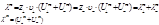Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Специфика растворов электролитов
*Электролитами называются вещества, которые в растворе или в расплаве самопроизвольно частично или полностью распадаются на ионы – заряженные частицы, способные к самостоятельному существованию. *Число ионов каждого знака определяется стехиометрическими коэффициентами в формуле электролита при соблюдении закона электронейтральности. *Ионы в растворе сольватированы, т.е. окружены определенным числом ориентированных диполей растворителя, которые прочно удерживаются вблизи иона и участвуют в тепловом движении вместе с ионом. Сольватация в водных растворах – гидратации…. Изотонический коэффициент i - величина, показывающая, во сколько раз увеличивается число частиц (ν) в растворе в результате диссоциации. Изотонический коэффициент связан со степенью диссоциации α:
При α=0 (раствор неэлектролита) i=1, а при α=1 (раствор нацело диссоциированного электролита) i=v 3.Теория Аррениуса (1887): Раствор электролита представляет собой смесь молекул растворителя, молекул и ионов электролита, в которой отсутствует взаимодействие между частицами растворенного вещества и молекулами растворителя. Нельзя было объяснить, например, почему различные методы определения Kдисс для некоторых электролитов дают разные значения, почему в ряде случаев *Теория Аррениуса не учитывает сольватационных эффектов и действия сил межионного взаимодействия
5. Подвижность ионов. Закон Кольрауша. Коэффициент электропроводности. Числа переноса и методы их определения. Подвижность ионов Электрическая проводимость определяется числом ионов, которые проходят через поперечное сечение проводника в единицу времени (скоростью движения ионов, ui’). Общая сила тока I, проходящего через раствор, обусловлена тем количеством электричества, которое переносится в единицу времени катионами и анионами: Закон Кольрауша Предельная молярная или предельная эквивалентная электрические проводимости будут равны:
Последнее уравнение является выражением закона Кольрауша: эквивалентная электрическая проводимость при бесконечном разведении равна сумме предельных подвижностей ионов. Предельная электрическая проводимость или предельные подвижности ионов являются важными константами, характеризующими способность данного электролита проводить электрический ток в растворе.
|
||||
|
Последнее изменение этой страницы: 2020-11-23; просмотров: 71; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.47.253 (0.003 с.) |