
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Проницаемость плазмалеммы для ионов калия и кальция. Колпачковый плазмолиз.Содержание книги
Поиск на нашем сайте
Таким образом, плазмолиз в клетке наступает вследствие слабой проницаемости тонопласта, а колпачки плазмы образуются вследствие набухания ее от проникших через плазмолемму ионов К+ в мезоплазму. ион Са2+ не вызывает набухания протопласта.
Цель работы. Показать различия форм плазмолиза, возникающих под влиянием ионов калия и кальция. Объект исследования. Луковица Allium сера, эпидермис которой содержит антоциан
Материалы и оборудование. Раствор KNO3 (1 M), раствор Ca(NO3)2 (1 M), предметные и покровные стекла, скальпель, бритва, препаровальная игла, микроскоп, стеклянные бюксы.
Порядок работы. 1. Приготовить препарат эпидермиса выпуклой стороны чешуи лука, содержащего антоциан. 2. Погрузить препарат в раствор азотнокислого калия (1 М) 3. Оставить препарат в растворе на 30 мин - 1 час. 4. Рассмотреть под микроскопом, отмечая образование колпачкового плазмолиза. 5. Провести параллельный опыт с нитратом кальция (1 М). 6. Зарисовать одну клетку с хорошо выраженным колпачковым плазмолизом. 7. На основании наблюдений сделать вывод о свойствах мембран цитоплазмы. Работа 3 Определение потенциального осмотического давления клеточного сока методом плазмолиза Клеточный сок - водный раствор различных органических и неорганических веществ. Потенциальное осмотическое давление зависит от числа частиц, находящихся в этом растворе, т. е. от концентрации и степени диссоциации растворенных молекул. Потенциальное осмотическое давление выражает максимальную способность клетки всасывать воду. Величина этого показателя указывает на возможность произрастания растения на почвах различной водоудерживающей силы. Повышение осмотического давления клеточного сока при засухе служит критерием обезвоживания растений и необходимости полива. Данный метод основан на подборе такой концентрации наружного раствора, которая вызывает самый начальный (уголковый) плазмолиз (Рис. 1а) в клетках исследуемой ткани. В этом случае осмотическое давление внешнего раствора примерно равно осмотическому давлению клеточного сока. Такой раствор называют изотоническим. Величину потенциального осмотического давления (в кПа) рассчитывают по формуле: П = 101,3 R T c i,
где R – газовая постоянная (0,0821 л × атм / моль × град); T – абсолютная температура по Кельвину (273 °C + комнатная); c – изотоническая концентрация в молях; i – изотонический коэффициент Вант-Гоффа; 101,3 – множитель для перевода атмосфер в килопаскали. Цель работы. Определение величины потенциального осмотического давления клеток растения. Объект исследования. Луковица Аlliиm сера L., с высоким содержанием антоциана. Материалы и оборудование. Раствор NaCl (1 M); градуированные пипетки на 5 и 10 мл; глазная пипетка; препаровальная игла; бритва, скальпель; микроскоп; фильтровальная бумага; предметные и покровные стекла; часы. Порядок работы 1. В пробирках приготовить по 10 мл 0,7; 0,6; 0,5; 0,4; 0,3 и 0,2 М растворов NaCl путем разбавления 1 М раствора дистиллированной водой. 2. Пробирки расположить в порядке возрастания концентрации и обязательно подписать карандашом по стеклу. 3. На выпуклой поверхности чешуи луковицы лезвием сделать надрез и аккуратно снять кусочек эпидермиса. 4. Полученный фрагмент ткани поместить на предметное стекло в каплю воды. Рассмотреть препарат под микроскопом при малом увеличении. 5. С одной стороны покровного стекла, не сдвигая препарата, кусочком фильтровальной бумаги удалить воду и внести 0,2 М раствор соли. 6. По истечению 10 мин кусочком фильтровальной бумаги удалить 0,2 М раствор и последовательно вносить растворы в порядке возрастания их концентрации с интервалом в 10 мин, по истечении которого рассмотреть препарат в микроскоп. Целью этой операции является нахождение изотонической концентрации (c) как среднее арифметическое между концентраций раствора, в котором плазмолиз ещё не происходит, и концентрацией раствора, при действии которого уже наблюдается начальный уголковый плазмолиз.
7. Результаты опыта записать по форме (Табл. 2). 8. Сделать выводы по результатам работы.
Таблица 2. Определение потенциального осмотического давления
Работа 4
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2020-11-23; просмотров: 1787; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.119 (0.008 с.) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

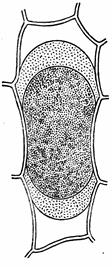 Рис. 2 Колпачковый плазмолиз
Рис. 2 Колпачковый плазмолиз



