
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Биологические и физические процессы и закономерности в живых системах. Редукционизм и антиредукцианизм. Принцип качественной несводимости.Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Биологические и физические процессы и закономерности в живых системах. Редукционизм и антиредукцианизм. Принцип качественной несводимости. Живые огранизмы – открытая, саморег-ся, самовоспр-ся и разв-ся гетерогенная система, важнейшими функциональными в-вами в которой явл-ся биополимеры: белки и нукл. к-ты сложного атомно-мол-ного строения. Первые попытки объяснения биолог. пр-сов связаны с методами сравнения с физич. пр-ми. Напр: м-м нервного проведения – как распростр. волны окисления в медной проволоки в кислоте; мышечное сокращение объяснялось работой пьезо элементов; рост клетки. Первоначально физика проникла в химию - необходимость объяснить как разл. соединения взаимод-ют в организме - физическая химия и химическая физика. Сущ 2 лагеря современ. физики: 1) Редукционисты: Любой био процесс происх. в жив организме можно свести к суме хим., физ. и механич. процессов. Объяснение сложного ч/з более простое, непонятное ч/з известное. Зная св-ва отдельных элементов, сост. систему и особенности их взаимод-вия, можно вывести все свойства этой системы. Обр. более сложного уровня - это результат усложнения более простых. Иногда: попытки заменить исследование реального объекта его упрощенной моделью. Достижение: предсказание существования планеты Нептун. Но как метод мышления не является универсальным. Неудача в биологии: не могут объяснить с этой т.зр. феномен жизни. 2) Антиредукционисты: Принцип качественной несводимости или био антиред., т.е. невозможность свести законы и принципы, управляющие живой материей к элементарной сумме физико-хим и мех. процессов процесс жизнедеятельности. Т.е. физико-матем. модели не м.б. адекватными, если в них не сод-ся элементы функциональной организации живых систем. Т.е. существует предел, после которого физические представления перестают быть самодостаточным средством познания, а дальше определяющим фактором становятся некоторые био истины, без которых уже не обойтись.
Основные направления развития современной биофизики. Уровни биофизических исследований. Биофизика – это н., изуч физ и физико-хим. пр-сы, протекающие в биосис. на разных уровнях орг-ции и явл-ся основой физиолог-их актов. Разделы биофизики: (и уровни такие же… наверно)))) 1. Молекулярная – изуч. строение и физ-хим св-ва, биофизику молекул, биополимеров и надмол-ных систем. 2. БФ клетки – изуч. особенности строения и функц-ния кл-ных и тканевых систем. БФ мембранных процессов – св-ва био мембран и их частей; БФ фотобиол. процессов - воздействия внешних источников света на живые системы; радиационная БФ: влияния ионизирующего излучения на организм. 3. БФ сложных систем – изуч. кинетику биопроц., поведение во времени разнообразных проц-ов присущих живой материи и ТД биосистем - преобразования Е в живых структурах. Современная БФ стремительно развивается, ее достижения способствуют переходу биологии на качественно более высокий молекулярный уровень исследования. Не знаю, что сюда ещё, из Википедии, можно как направления: математическая БФ. Прикладная БФ: биоинформатика (хотя не является собственным разделом БФ, но очень тесно связана с ней); биометрия; биомеханика (функции и структура опорно-двигального аппарата и физ. движения биосистем); БФ эволюционных процессов; медицинская БФ; экологическая БФ. Био объекты очень сложны и на протекающие в них процессы влияют многие факторы, кот. зависят друг от друга. Физика позволяет создать упрощенные модели объекта, кот. описываются законами ТД, электродинамики, квантовой и классической механики. С пом. корреляции физ. данных с биол-ми можно получить более глубокое понимание процессов в био объекте. Для получения инфо в био системах применяют различные оптические методы, рентгено-структурный анализ с использованием синхротронного излучения, ЯМР- и ЭПР-спектроскопию, 7-резонансную спектроскопию, различные электрометрические методы, микроэлектродную технику, методы хемилюминесценции, лазерную спектроскопию, метод меченых атомов и др. Это исп. для медицинской диагностики и терапии. Термодинамика (ТД). 4. Термодинамика, как ядро современной биофизики. Предмет и задачи. Практическое значение ТД в БФ исследованиях. ТД – это н. о превращения Е. ТД - это н., изуч. наиболее общие закономерности превращения различных видов Е в системе. Предмет ТД: Е; возникновение Е в живых сист.; взаимодейств. жив. сист. с окруж. средой. Подходы: феноменологический и детальный. Значение имеют ТД параметры только в исходном и конечном состоянии. Методы: статистический (но не даёт представление о процессе). Направления: 1) изуч. и расчёт Е в состоянии покоя и при совершении работы. Изуч-ся и опр-ся КПД разл биол процессов. 2) изуч. динамических процессов в живых сист. (транспорт в-ва). Значение: Позволяет оценить энергетические изменения, происх. в результате биохим. р-ций; рассчитать Е разрыва конкретных хим связей; рассчитать осмот. давление по обе стороны полупрониц. мембраны; рассчитать влияние концентрации соли в р-ре на растворимость макром-л. Применяется для описания процессов, происх. в электрохим. ячейках. Привлекается для обоснования теории возникновения и эволюции жизни на Земле.
Классификация ТД систем; особенности живых организмов, как ТД систем. Система – любое материальное тело / объект, который сост. из большого числа частиц. Выполняют некоторую общую функцию, несводимую к ф-циям компонентов сист. Окр. среда – всё, что находится в контакте с системой. Типы: 1) закрытые (т.е. не обмениваются в-вом): а) изолированная – сист, кот не обменивается с окр. средой не Е, не в-вом. Напр: космонавт в скафандре в открытом космосе. б) замкнутая – не обменивается с окр. средой в-вом, но обменивается Е. Напр: стакан с горячим чаем. 2) открытые – обмен и в-вом и Е. Напр: все живые сист.
Характеристика ТД функций, применяемых для анализа биолог процессов. Функция – совокупность физ. и хим. св-в, кот. определяют конкретное сост. системы. Напр: t, V, P. ТД функции = ТД параметры. ТД параметры сост. системы – измеримые св-ва системы, связанные с Е и характеризующие её состояние. Основные параметры состояния – параметры, поддающиеся прямому измерению. Те, которые нельзя измерить непосредственно, рассматривают как функции основных параметров состояния. Типы: 1) экстенсивные (=факторы ёмкости) – это ТД фукнции, кот зависят от кол-ва или числа частиц и их массы. Напр: масса, объём, E, энтропия (S), энтальпия (Н). Св-во системы = сумме свойств частей. 2) интенсивные – не зависят. Напр: t, давление, скорость изменения энтропии. Состояние системы – совокупность всех физ. и хим. св-в системы. ТД процесс - изменение сост. системы, характ-ся изм. её ТД параметров. Изменение может происходить при различных условиях, различают: 1). Равновесные и неравновесные процессы. Равн. пр. - непрерывный ряд равновесных сост. сист.; сост., не изм-ся во времени и не требующее для своего поддержания каких-либо внешних факторов. Нер. — это пр-сы, после протекания кот. систему нельзя вернуть в исходное сост. без того, чтобы в ней не осталось каких-либо изменений. 2). Обратимые и необратимые процессы. Обрю. – пр-сы, допускающие возможность возвращения системы в первоначальное сост. без того, чтобы в окр. среде остались какие-либо изменения. В противном случае – необр. 3). Самопроизвольные и несамопроизвольные процессы. Сам. – процессы, происходящие сами собой (не требующие затраты Е извне) и приближающие систему к равновесию. Несам. – процессы, требующие затраты Е извне. Некоторые частные виды процессов: а) изотермический (T = const); б) изобарный (p = const); в) изохорный (V = const); г) адиабатический (нет обмена теплотой между системой и окр. средой); д) изобарно – изотермический (p = const, T = const); е) изохорно – изотермический (V = const, T = const).
ТД полного окисления глюкозы. Расчёт эффективности (КПД) биологического окисления глюкозы. (см. вопрос 24) При окислении глюкозы до СО2 и Н2О высвобождается больше Е, чем при гликолизе. При гликолизе: глюкоза → 2 лактат- + 2Н+, ∆G0 (свободная энергия) = -47,0 ккал/моль («-» т.к. выделяется). При полном окислении: глюкоза + 6О2 → 6СО2 + 6Н2О, ∆G0= -686 ккал/моль. При гликолизе лактат содержит ≈ 93% той Е, которая была заключена в исходной м-ле глюкозы. Т.к. молочная к-та – сложное соединение, при глиголизе не происходит реального окисления. Вся био доступная Е высвобождается из глюкозы лишь в том случае, если все водородные атомы, связанные с углеродом, будут удалены и заменены кислородом с обр-нием СО2.
ЛИМИТИРУЮЩАЯ СТАДИЯ Нередко скорость сложной химической реакции может зависеть главным образом не от всех значений констант скорости отдельных ее стадий, а только от одной. Эту стадию называют лимитирующей (т. е. определяющей скорость всей реакции в целом). Скорость последовательной реакции определяется скоростью наиболее медленной стадии, скорость же параллельных реакций определяется скоростью наиболее быстрой стадии. Например, пусть имеется сложная реакция А ® D, протекающая в три стадии: А Исходное вещество А превращается в активную промежуточную частицу (АПЧ) Р 1 (константа k 1), которая в свою очередь превращается в АПЧ Р 2 (константа k 2), а уже из Р 2 образуется продукт реакции — вещество D (константа k 3). В том случае, если k 1 << k 2» k 3, то даже при малых концентрациях Р 1 и Р 2 скорости второй и третьей стадий очень велики и намного превышают скорость первой стадии. Фактически все образовавшееся количество Р 1 очень быстро превращается в продукт реакции D. Скорость всей реакции определяется скоростью образования Р 1 — лимитирующей стадией реакции будут первая: w @ w 1 = k 1 ·CA.
ЭНЕРГИЯ АКТИВАЦИИ Зависимость скорости реакции от температуры дает уравнение Аррениуса:
где k — константа скорости реакции, R — универсальная газовая постоянная, Е — энергия активации химической реакции. В случае простых реакций величина Е показывает, какой минимальной (избыточной по сравнению со средней) энергией в расчете на 1 моль должны обладать реагирующие частицы, чтобы они могли вступить в химическую реакцию. В случае сложных реакций величина Е называется эмпирической или кажущейся энергией активации и в общем случае зависит от энергий активации отдельных стадий данной реакции. Проинтегрировав уравнение (10.16), получим уравнение Аррениуса в интегральной форме:
или
где А — предэкспоненциальный множитель. Физический смысл А в случае простых реакций: мономолекулярных — это частота колебаний по разрываемой связи (А» 1013 сек-1), бимолекулярных — величина А пропорциональна общему числу столкновений между молекулами реагирующих веществ (А» 10-10 ¸ 10-11 см3/(мол-л·сек). Проинтегрировав ур-е (10.16) в пределах температур от Т 1 до Т 2, получим:
Энергию активации можно определить как аналитически по уравнению (10.18), так и графическим методом. Для этого необходимо знать ряд констант скоростей при разных температурах. Если реакция подчиняется уравнению Аррениуса, то зависимость ln k от 1/ T должна выражаться прямой линией, что следует из уравнения (10.17) (рис. 7).
Рис. 7. К расчету энергии активации реакции по температурной зависимости константы скорости. Для очень большого числа реакций энергия активации находится в пределах от 60 до 240 кДж/моль, т.е. примерно соответствует энергиям химических связей. Энерг актив. Связана с Q10: Е=0,46T1*T2lgQ10
ИСП УР Лайнуивера-Бэрка ДЛЯ ОПРЕДЕЛЕНИЯ КИНЕТ ХАР-ИК ФЕРМ Р-ЦИИ
Графическое выражение для скорости реакции в координатах Лайнуивера-Бэрка имеет вид прямой линии, тангенс угла наклона который будет равен величине Km/Vmax. Линия отсек на оси Х значение -1/Km, а на оси Y- значение 1/V max
АНАЛ НЕКОНКУР ИНГИБИР НЕКОНКУРЕНТНОЕ ИНГИБИРОВАНИЕ ПРОЯВЛЯЕТСЯ ПРИ СВЯЗЫВАНИИ ИНГИБИТОРА С ФЕРМЕНТОМ ВНЕ АКТИВНОГО ЦЕНТРА, но при этом меняется структура активного центра и связь с субстратом становится невозможной. E + I ---> EI, EI + S ----> (невозможно)
Зависимость в координатах Лайнуивера-Берка имеет вид пучка прямых, пересекающихся на оси абсцисс. ингибитор не изменяет Кm и снижает V max.
Ренатурация (renaturation) - Восстановление (после денатурации) нативной (биологически активной) пространственной структуры биополимера (белка или нуклеиновой кислоты). В частности, ренатурация ДНК (после денатурации нагреванием) может происходить при медленном охлаждении, что используется для получения гибридных гетеродуплексов. Метод дифференциальной диагностики и прямого выявления нуклеиновых кислот в исследуемом материале с помощью реакции молекулярной гибридизации и полимеразной цепной реакции (ПЦР). Диагностическая суть этих методов заключается в том, что у исследователей имеются определенные олигонуклеотиды, воспроизводящие (или комплементарные), высококонсервативные и высокоспецифичные последовательности нуклеотидовиз искомого генома. В реакции молекулярной гибридизации такие олигонуклеотилы называют зондами, в методе ПЦР -праймерами. В реакции молекулярной гибридизации назначение этих специфических олигонуклеотидов-"найти'' в исследуемой нуклеиновой кислоте комплементарные последовательности, и сформировать структуры согласно природе комплементарных взаимодействий между парами азотистых оснований. Материалом для исследований служит кровь, культуральная жидкость, ликвор, биопсийный материал, носоглоточные смывы, моча и пр. биологические субстанции. Молекулярно-генетические методы перспективны при необходимости ранней диагностики ВИЧ до появления в сыворотке AT, при неясных серологических результатах, при определении наличия ВИЧ в организме новорожденных детей от инфицированных женщин. Целесообразно использовать эти методы при обследовании серонегативных сексуальных партнеров инфицированных лиц
Электрокинетический потенциал: возникновение, измерение и факторы, определяющие его величину. Примеры электрокинетических явлений, их характеристика и научно-практическое значение. Потенцил Действия 1. Объясняется поворотом диполя на 1800. 2. Теория альтерации Германа. При возбуждении возникает избыток кислых продуктов, которые несут отрицательны заряд, что приводит к разности потенциалов между возбужденным и невозбужденым учаском. 3. Мембранная теория Берштейна. В возбужденном участке мембраны резко увеличивается проницаемость для всех ионов, концентрации ионов смешиваются и участок становится электронейтральным. 4. Ходжкин и Хаксли. Рост проницаемости мембраны для ионов в месте воздействия. При возбуждении электропроницаемость мембраны увеличивается примерно в 500 раз. Max увеличивается проницаемость мембраны для Na+ (отсюда Na-теория ПД). Na+ свободно проходит внуть клетки. При возбужедении электро-химическое равновесие определяется потенциалом Na+. Равновесный потенциал для К+ = –97 мВ, для Na+ = +50 мВ. При возбужедении мембрана перезаряжается. Положение обратной активации и инактивации Na+-каналов, Na+-канал может активироваться (открываться) при определенных значениях потенциала. Причина активации Na+-каналов – деполяризация мембраны, чем больше деполяризация, тем больше проницаемость мембраны для Na+. Зависимость близка к линейной в подкор уровне; как только мембрана достигнет критического уровня деполяризации – зависимость нелинейная, лавинообразный вход Na+ в клетку. Электрокинетический потенциал, x-потенциал, дзета-потенциал, часть общего скачка потенциала на границе двух фаз, определяющая относительное перемещение этих фаз при электрокинетических явлениях. Общий скачок потенциала при пересечении межфазной границы в дисперсных системах обусловлен существованием двойного электрического слоя. Электрокинетический потенциал — перепад потенциала по той части диффузного слоя, в пределах которой жидкость может быть вовлечена в тангенциальное движение относительно межфазной поверхности при внешнем воздействии на систему. Под влиянием сильно адсорбирующихся на поверхности ионов или изменения pH жидкости может произойти перемена знака на противоположный («перезарядка» поверхности). Электрокинетический потенциал в изоэлектрической точке равен нулю. он является одной из важнейших характеристик жидких коллоидных систем. Его значение и характер изменения при варьировании параметров электролита, адсорбции на пов-сти разл. в-в и т. п. позволяет судить о структуре граничных слоев, особенностях взаимод. компонентов р-ра с пов-стью, заряде пов-сти и т.д. 1). Для объяснения реполяризации используется положение об инактивации Na+-каналов. При приближении потенциала мембраны к равновесному для Na+, Na+-каналы инактивируются и посупление Na в клетку прекращается. К графику: в основе регенеративный процесс (сам себя поддерживающий), развивающийся по принципу обратной связи. 2). Рост К+ проницаемости мембраны. Не столь значителен, как для Na+ (в 5-15 и 500 раз соответственно). Проницаемость для К+ развивается медленнее, чем для Na+. Ионы К+ в этой ситуации будут выходить наружу и выносить заряд. 3). Механизм активного транспорта, представленный K-Na-насосом. 3 Na+ внутрь и 2 К+ наружу. Эксперименты Ходжкина и Хаксли. Гигантский аксон кальмара. Из внеклеточной среды были удалены 2/3 Na+. При этом амплитуда ПД снизилась? на 50%. Замена внутриклеточного Na+ на другие ионы приводит к некоторому росту ПД. Замена? внутриклеточного К+ на Na+ приводит к значительному снижению ПД. Метод фиксации потенциала метод Петч-Клемпинга. С его помощью можно зафиксировать на длительное время значение мембранного потенциала на любом желаемом уровне. Это делается с помощью внешнего генератора напряжения Суммарные мембранные токи при ПД 1. Подпороговая область: Слабое изменение мембранного потенциала, суммарный ионный ток направлен от клетки наружу, так как поток К+, выходящий из клетки, уже усиливается из-за удаления мембранного потенциала от равновесного потенциала для К+. Входящий ток Na+ еще слаб, так как рост Na+-проницаемости пока невелик. Однако с развитием деполяризации Na-ый поток постепенно нарастает. 2. Критический уровень деполяризации: В этот момент суммарный ионный ток через мембрану равен нулю, так как встречные токи ионов Na+ и К+ уравновешивают друг друга. Даже небольшая дальнейшая деполяризация приводит к росту входа Na+-тока в сотни раз. 3. Во время фазы деполяризации резко увеличивается Na+-проницаемость и суммарный мембранный ток, направленный внутрь клетки. Выходящий К+-ток растет медленнее и становится заметным только к моменту пика потенциала. 4. Фаза реполяризации: В момент пика потенциала большинство Na+-каналов инактивированны, а К+-ток max. Поэтому суммарный мембранный ток – выходящий. Кальциевая теория активации и инактивации Na+-каналов В состоянии покоя у наружного отверстия Na+-канала находится Са2+, который электростатически тормозит проникновение Na+ в канал. При возбуждении наружная поверхность мембраны заряжена отрицательно, при этом Са2+ уходят со своих мест, вход открывается и Na+ входит в клетки. Инактивация: по ходу деполяризации узкие Na+-каналы могут закупориваться Na+. Во многих каналах есть воротные белки (могут менять свое местоположение под влиянием изменения потенциала). В состоянии покоя активационный белок закрыт, а инактивационный открыт. При возбуждении открывается активационный белок в момент закрывания инактивационного белка. В конце реполяризации белки так же закрываются и потом открываются (исходное состояние). Факторы, определяющие скорость распространения возбуждения по нервному волокну 1. Пространственная константа определяет величину декремент деполяризации,? - пространственная константа. 2. Коэффициент надежности, соотношение между амплитудой ПД критической энергией и ПП. S=ПД/(Екр–ПП), ПД=120мВ, ПП=–70мВ, Екр=–55мВ? S=8. Чем больше S, тем быстрее проведение. 3. Временная константа? мембр. При возбуждении мембраны меняется заряд. Длительность перезарядки мембраны.?мембр=Rm*Cm. Чем больше? мембр, тем ниже С. Vраспр=S*?/?мембр.
Биологические и физические процессы и закономерности в живых системах. Редукционизм и антиредукцианизм. Принцип качественной несводимости. Живые огранизмы – открытая, саморег-ся, самовоспр-ся и разв-ся гетерогенная система, важнейшими функциональными в-вами в которой явл-ся биополимеры: белки и нукл. к-ты сложного атомно-мол-ного строения. Первые попытки объяснения биолог. пр-сов связаны с методами сравнения с физич. пр-ми. Напр: м-м нервного проведения – как распростр. волны окисления в медной проволоки в кислоте; мышечное сокращение объяснялось работой пьезо элементов; рост клетки. Первоначально физика проникла в химию - необходимость объяснить как разл. соединения взаимод-ют в организме - физическая химия и химическая физика. Сущ 2 лагеря современ. физики: 1) Редукционисты: Любой био процесс происх. в жив организме можно свести к суме хим., физ. и механич. процессов. Объяснение сложного ч/з более простое, непонятное ч/з известное. Зная св-ва отдельных элементов, сост. систему и особенности их взаимод-вия, можно вывести все свойства этой системы. Обр. более сложного уровня - это результат усложнения более простых. Иногда: попытки заменить исследование реального объекта его упрощенной моделью. Достижение: предсказание существования планеты Нептун. Но как метод мышления не является универсальным. Неудача в биологии: не могут объяснить с этой т.зр. феномен жизни. 2) Антиредукционисты: Принцип качественной несводимости или био антиред., т.е. невозможность свести законы и принципы, управляющие живой материей к элементарной сумме физико-хим и мех. процессов процесс жизнедеятельности. Т.е. физико-матем. модели не м.б. адекватными, если в них не сод-ся элементы функциональной организации живых систем. Т.е. существует предел, после которого физические представления перестают быть самодостаточным средством познания, а дальше определяющим фактором становятся некоторые био истины, без которых уже не обойтись.
|
|||||||
|
Последнее изменение этой страницы: 2016-04-07; просмотров: 1309; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.135.206.212 (0.012 с.) |

 Р 1
Р 1  Р 2
Р 2  D.
D.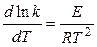 , (10.16)
, (10.16) , (10.17)
, (10.17)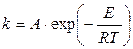 ,
, . (10.18)
. (10.18)

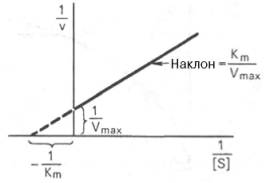 график Л-Б
график Л-Б скор р-ции
скор р-ции



