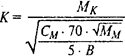Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Выявление возбудителей специфической инфекции
Хламидийная инфекция распространяется половым, бытовым путем, а также путем инфицирования детей при родах, во время прохождения плода по инфицированным родильным путям и вызывает воспалительные заболевания слизистых оболочек мочеполовых органов. Один из методов выделения хламидий основан на использовании желточных мешков куриных эмбрионов, другой – на выделении хламидий в культуре клеток. Можно использовать три метода лабораторной диагностики хламидиозов: выявление морфологических структур микроорганизмов в соскобах из уретры при окраске по Романовскому- Гимзе, определение антигенов хламидий в соскобах из уретры при окраске методом флюоресцирующих антител в прямой модификации (МПФА) по общепринятой методике и выделения микроорганизмов в культуре клеток. На протяжении последних лет широкое распространение получил метод ДНК-диагностики возбудителей специфической инфекции, основанный на применении полимеразной цепной реакции. В настоящее время считается признанным, что микобактерии туберкулеза, как другие микроорганизмы, не проникают в мочу через неповрежденные почки. Поэтому важное значение в диагностике туберкулеза почек приобретает выявление микобактерий туберкулеза в моче путем микроскопии осадка мочи, окрашенного по Цилю-Нильсону (бактериоскопический метод) и посева мочи на специальную питательную среду Прейс-Школьниковой (бактериологический метод). При негативном результате бактериоскопии обычного мазка исследуют мочу методом флотации. При исследовании под микроскопом в моче можно выявить друзы актиномицет, яйца шистосом, мелкие кисты эхинококка. Лейкоцитурия. В зависимости от количества лейкоцитов в моче, применяют два термина: пиурия и лейкоцитурия. Пиурия – наличие гноя, который макроскопически виден в моче. У здоровых людей в моче постоянно присутствует небольшое количество лейкоцитов. О лейкоцитурии принято говорить, если в осадке мочи есть 6 и больше лейкоцитов в поле зрения микроскопа. Ориентировочно установить источник пиурии можно с помощью трехстаканной пробы. В выявлении лейкоцитурии исключительно важное значение имеет методика сбора мочи. У женщин моча может быть загрязнена во время акта мочеиспускания выделениями из влагалища, у мужчин – из препуциального мешка, у девочек – с вульвы. Поэтому мочу стоит собирать после тщательной обработки внешних половых органов и внешнего отверстия уретры растворами антисептиков.
Правильно интепретировать полученные данные при небольшом количестве лейкоцитов в осадке мочи бывает нелегко. Учитывая это, в данное время в сомнительных случаях применяют количественные методы выявления лейкоцитурии. Они заключаются в подсчете количества лейкоцитов в определенном объеме мочи или в моче выделенной больным за определенный период времени. Так, например, определяют количество форменных элементов в моче, выделенной за сутки (метод Каковского-Аддиса), за 1 час (метод Рофе), за 1 мин (метод Амбюрже); количество лейкоцитов в 1 мл моче (метод Нечипоренко) или в 1 мм3 нецентрифугованой моче (метод Стансфилда-Вэбба). В основе всех количественных методов исследования лежит определение числа форменных элементов (отдельно лейкоцитов, эритроцитов и цилиндров) у 1 мм3 осадка мочи с помощью счетной камеры (гемоцитометра). Метод Каковского—Аддиса. В 1910 г. А.Ф.Каковский первым предложил заменить обычный метод исследования осадка мочи более точным количественным определением в нем форменных элементов. Через 15 лет Addis (1925) предложил методику определения форменных элементов в суточной моче, во многом аналогичную методу Каковского. Мочу собирают на протяжении 10 или 12 час, удобнее всего ночную порцию (с 22 час до 8 час утра). Метод Нечипоренко. Наибольшее распространение в нашей стране получил метод подсчета форменных элементов в 1 мл моче, предложенный в 1961г. А.З. Нечипоренко. Берут 10 мл мочи, центрифугируют и оставляют в пробирке 1 мл мочи вместе с осадком. Определяют наличие форменных элементов у 1мм3 осадка мочи, а затем вычисляют количество лейкоцитов в 1мл. Методы выявления скрытой лейкоцитурии. Отсутствие изменений в моче и клинически выраженного обострения, нередко ставит практического врача в затруднительное положение. В связи с этим и с целью выявления скрытой лейкоцитурии стали применять провокационные пробы, что позволяют получить у больных хроническим пиелонефритом увеличенное количество лейкоцитов в моче. В настоящее время применяют пирогенный, преднизолоновый, парафиновый, озокеритовый и другие провокационные тесты.
Преднизолоновый тест проводят по следующей методике. Утром собирают среднюю порцию мочи при самостоятельном мочеиспускании. После этого медленно на протяжении 3-5 мин вводят внутривенно 30-50 мг (в зависимости от массы больного) преднизолона, разведенного в 10 мл изотонического раствора хлорида натрия. Приблизительно через 3-4 час после введения преднизолона аналогичным методом собирают мочу на исследование. Определяют количество лейкоцитов и других форменных элементов в 1 мл каждой порции мочи, а также наличие в осадке мочи клеток Штернгеймера-Мальбина, или активных лейкоцитов. Тест считается положительным при наличии свыше 4000 лейкоцитов в 1 мл моче после введения преднизолона и появлении в осадке мочи клеток Штернгеймера-Мальбина, или активных лейкоцитов. Морфологические исследования лейкоцитов мочи. Штернгеймер и Мальбин показали, что лейкоциты мочи отличаются один от другого по внешнему виду и в зависимости от морфологических особенностей окрашиваются специальным красителем либо в красный, либо в бледно-голубой цвет. Лейкоциты, окрашенные в голубой цвет, бывают двух видов. Лейкоциты первого вида не отличаются от обычных сегментоядерних. Лейкоциты второго вида увеличены в размере в 2-3 раза, округлой формы, иногда с вакуолизацией протоплазмы. Лейкоциты второго вида принято называть клетками Штернгеймера-Мальбина. Они представляют собой обычные жизнеспособные сегментоядерные нейтрофильные лейкоциты, которые проникают в мочу из участков воспаления почечной паренхимы, изменяя их вид и форму. Клетки Штернгеймера-Мальбина выявляют приблизительно в 50% больных острым пиелонефритом и в 25% больных хроническим пиелонефритом. Клетки Штернгеймера—Мальбина не являются патогномоническими для пиелонефрита, поскольку могут оказываться в секрете предстательной железы, выделениях из влагалища. Если попадание в мочу секрета предстательной железы и влагалищного содержания исключено, то клетки Штернгеймера—Мальбина указывают на наличие неспецифического воспалительного процесса в почке и его активность, потому что лейкоциты данного вида практически отсутствуют в моче при остром и хроническом циститах. Активные лейкоциты. В связи с тем, что жизнеспособные лейкоциты превращаются в мочи в клетки Штернгеймера-Мальбина лишь при низкой осмотической концентрации и поэтому далеко не всегда могут быть выявлены, В.С.Рябинский и В.Е.Родоман (1966) предложили методику исследования активных лейкоцитов в осадке мочи. Метод основан на том, что жизнеспособные лейкоциты, которые попали в мочевые пути из участка воспаления в почке, обязательно превращаются в моче с низким осмотическим давлением в большие клетки с подвижными гранулами в их протоплазме. Активные лейкоциты выявляют в 87,8% больных острым пиелонефритом и в 79,8% больных хроническим пиелонефритом. Исследование профиля лейкоцитурии. При исследовании осадка мочи больных после трансплантации почек, всегда оказывается избыток лимфоцитов. При пиелонефрите у детей преобладает нейтрофильный профиль лейкоцитурии, а при гломерулонефрити – лимфоцитарный. Это позволяет использовать исследование профиля лейкоцитурии при дифференциальной диагностике разнообразных нефропатий, а также выявлении реакции отторжения при гнойно-воспалительном процессе в трансплантированной почке.
Глюкозурия. У здоровых людей соддержится 0,2 г глюкозы в 1 л мочи, что не удается выявить с помощью обычных проб. Появление глюкозы в моче (глюкозурия) может быть результатом физиологической гипергликемии (алиментарной, эмоциональной, врачебной) или различных заболеваниях (сахарный диабет, гипертиреоз, синдром Иценко-Кушинга, заболеваний печени, почек, раздражения ЦНС). Для оценки степени глюкозурии необходимо определять количество глюкозы, которое выделяется с мочой за сутки. Протеинурия. Небольшое количества белка может быть в суточной моче и у здоровых лиц. Выделения значительных количеств белка, при которых обычные качественные пробы на белок в моче становятся положительными, называются протеинурией. Различают почечную (истинную) и внепочечную (ложную) протеинурию. При почечной протеинурии белок в мочу проникает непосредственно из крови в результате увеличения фильтрации его клубочками почки или снижения канальцевой реабсорбции. Почечная (истинная) протеинурия бывает функциональной или органической. Среди функциональной почечной протеинурии наиболее часто наблюдаются такие ее виды: физиологическая протеинурия новорожденных, которая исчезает на 4-й, 10-й день после рождения, а у недоношенных несколько позже; ортостатическая альбуминурия, характерная для детей в возрасте 7-18 лет и появляется только в вертикальном положении тела; транзиторная альбуминурия, причиной которой могут быть разнообразные заболевания органов пищеварения, тяжелая анемия, ожоги, травмы или физиологические факторы: тяжелая физическая нагрузка, переохлаждение, сильные эмоции, еда, богатая белком и др. Органическая (почечная) протеинурия наблюдается в результате прохождения белка из крови через поврежденные участки эндотелия почечных клубочков при заболеваниях почек (гломерулонефрит, нефроз, нефросклероз, амилоидоз, нефропатия беременных), расстройствах почечной гемодинамики (почечная венозная гипертензия, гипоксия), трофических и токсичных (в том числе врачебных) влияниях на стенки капилляров клубочков. Внепочечная (ложная) протеинурия, при которой источником белка в моче являются примеси лейкоцитов, эритроцитов, бактерий, клеток уротелия, наблюдается при урологических заболеваниях (мочекаменная болезнь, опухоли почек и мочевых путей, туберкулез почек и др.). Большинство качественных и количественных методов определения белка в моче основано на его коагуляции в объеме мочи или на границе сред (мочи и кислоты). Среди качественных методов определения белка в моче наибольшее распространение получили унифицированная проба с сульфосалициловой кислотой и кольцевая проба Геллера. Из количественных методов наиболее часто применяются: унифицированный метод Брандберга-Робертса-Стольникова, в основу которого положена кольцевая проба Геллера; фотоэлектроколориметрический метод количественного определения белка в моче по помутнению, который образуется при добавлении сульфсалициловой кислоты; биуретовый метод. Выявления белка в моче упрощенным ускоренным методом проводят колориметрическим методом с помощью индикаторной бумаги.
Фильтрация белков плазмы крови подчиняется определенной закономерности: чем больше молекулярная масса белка, который экскретируется в мочу, тем меньше его клиренс и тем ниже концентрация его в остаточной моче. Протеинурия, которая отвечает этой закономерности, является селективной в отличие от неселективной, для которой характерным является искажение выведенной закономерности. Выявление белка в моче с относительно большой молекулярной массой свидетельствует об отсутствии избирательности почечного фильтра и указывает на выраженое его поражение. В этих случаях говорят о низкой селективности протеинурии. Поэтому в настоящее время широкое распространение получило определение белковых фракций мочи с использованием методов электрофореза в крахмальном и полиакриламидном геле. По результатам этих методов исследования можно судить о селективности протеинурии. Изучение клиренсов индивидуальных белков плазмы позволяет получить достоверные сведения о состоянии фильтрационных базальных мембран клубочков почки. Клинический интерес представляет бета-2-микроглобулин. Имея низкую молекулярную массу (относительная молекулярная масса 1800), он свободно проходит через клубочки почки и почти полностью реабсорбируется в проксимальных канальцах. Это позволяет использовать количественное определение бета-2-микроглобулина в крови и моче для определения клубочковой фильтрации и возможности почек к резорбции протеинов в проксимальных канальцах. Концентрация бета-2-микроглобулина в крови увеличивается при заболеваниях, которые сопровождаются нарушением клубочковой фильтрации, в частности при остром и хроническом гломерулонефрите, поликистозе почек, нефросклерозе, диабетической нефропатии, острой почечной недостаточности. Концентрация бета-2-микроглобулина в моче повышается при заболеваниях, которые сопровождаются нарушением реабсорбционной функции канальцев. Однако при интерпретации результатов исследования нужно учитывать, что любое повышение температуры всегда сопровождается увеличением экскреции бета-2-микроглобулина с мочой.
Порфирины – вещества, которые входят в состав сложных белков. В норме с мочой выделяется очень небольшое количество порфиринов (до 30 мг в сутки). Сюда принадлежат группы гемоглобина, миоглобина, разных цитохромов, ферментов каталазы и пероксидазы. При нарушениях порфиринового обмена, порфирины могут откладываться в костях и других тканях. Резкая порфиринурия наблюдается в случае нарушений порфиринового обмена при длительных приемах сульфаниламидных препаратов. Эти лекарственные вещества, накапливаясь в организме, могут влиять на порфириновый обмен, вызывая поражение центральной нервной системы, печени. Гематопорфирин – кровяной пигмент, который не содержит железа. От присутствия гематопорфирина моча приобретает темно-красный, а иногда и синевато-красный цвет. Гематопорфирин появляется в моче при остром отравлении свинцом. Присутствие его можно выявить спектроскопически. Увеличение выделения порфиринов с мочой наблюдается при ревматизме, полиомиелите, пневмонии, авитаминозе РР (пеллагре), заболеваниях крови (анемиях и лейкозах), аллергических состояниях, некоторых заболеваниях желудочно-кишечного тракта, поражениях печени. Значительную часть порфиринов организм человека получает с продуктами питания – мясом, овощами (экзогенные порфирины). Поступив в кишку, порфирины всасываются в кровь и через воротную вену попадают в печень. В печени они превращаются в копропорфирины. Большая их часть выделяется с желчью и входит в состав каловых масс, а более малая находится в крови и моче. С мочой выделяются в норме только уропорфирины. Порфирины эндогенного происхождения образуются в организме из продуктов расщепления гемоглобина и миоглобина, а также путем синтеза гликокола и янтарной кислоты и являются промежуточным продуктом при образовании гемоглобина, дыхательных ферментов и миоглобина. Неплазменные (тканевые) уропротеины. Кроме белков плазмы крови, в моче могут быть неплазменные (тканевые) протеины. Состав неплазменных протеинов чрезвычайно разнообразен. Среди них гликопротеины, гормоны, антигены, ферменты (энзимы). Средние молекулы (СМ), так называемые белковые токсины. Физическая структура их неизвестна. В состав СМ входят по меньшей мере 30 пептидов: окситоцин, вазопресин, ангиотензин, глюкагон, адренокортикотропный гормон и др. Избыточное накопление СМ наблюдается при снижении функции почек. Они имеют разнообразное биологическое действие, вызывают вторичную иммунодепресию, вторичную анемию, подавляют биосинтез белка и эритропоэз, тормозят активность многих ферментов, нарушают ход фаз воспалительного процесса. Уровень СМ в крови и моче определяют скрининговым тестом, а также путем спектрофотометрии. За норму принимают содержание СМ в крови, равное 0,24 ± 0,02 усл. ед., а в моче – 0,312±0,09 усл. ед. Будучи нормальными продуктами жизнедеятельности организма, они выделяются из него в норме почками путем гломерулярной фильтрации в 95%. Примиеломной болезни и макроглобулинемии Вальденстрема в моче выявляют белок Бенс-Джонса. Метод выявления названного белка в моче основан на реакции термопреципитации. С полной достоверностью он может быть выявлен в моче иммуноэлектрофоретическим методом с использованием специфических сывороток против тяжелых и легких цепей иммуноглобулинов. Исследование ферментов в крови и моче. При патологическом процессе наблюдаются глубокие нарушения жизнедеятельности клеток, что сопровождается выходом внутриклеточных ферментов в жидкостные среды организма. Исследования нефрона человека и животных показали, что в отдельных его частях есть высокая ферментативная дифференциация. В клубочках почки в наличии относительно небольшое количество разнообразных энзимов. Клетки почечных канальцев, особенно проксимальных отделов, содержат максимальное количество энзимов, высокая активность наблюдается в петле Генле, прямых канальцах и собирательных трубочках. Изменения активности отдельных энзимов при разнообразных заболеваниях почек зависят от характера, остроты и локализации процесса. Они наблюдаются до появления морфологических изменений в почках. Поскольку наличие разнообразных ферментов четко локализовано в нефронах, определение того или другого фермента в моче может способствовать топической диагностике патологического процесса в почках, дифференциальной диагностике почечных заболеваний и определению динамики процесса в почечной паренхиме. Для дифференциальной диагностики применяют определение активности в крови и моче таких ферментов как: лейцинаминопептидазы (ЛАП), кислой фосфатазы (КФ), щелочной фосфатазы (ЩФ), лактатдегидрогеназы (ЛДГ), альдолазы, глютамино-щавелеуксусной трансаминазы (ГЩТ), трансамидиназы и др. Активность ферментов в сыворотке крови и в моче определяют с помощью биохимических, спектрофотометрических, хроматографических, флуориметрическиих и хемилюминисцентных методов. Кетоновые (ацетоновые) тела состоят из ацетона, ацетоуксусной и b-оксимасляной кислот. В норме у здорового человека кетоновые тела появляются после длительного приема жирной мясной пищи и еды почти лишенной углеводов. Известно, что белки, жиры и углеводы могут расщепляться в организме к конечным продуктам обмена - углекислоты и воды. Расщепление жира в тканях происходит под действием липолитических ферментов (тканевых липаз) с образованием глицерина и высших жирных кислот. При окислении жирных кислот образуются промежуточные продукты обмена – ненасыщенные жирные кислоты, окси- и кетокислоты и простые жирные кислоты. Жирные кислоты дегидрируются и превращаются в ненасыщенные кислоты, к которым присоединяется вода, образовывая b-оксикислоту. Эта кислота опять дегидрируется, превращаясь в b-кетокислоту, которая присоединив молекулу воды, расщепляется на так называемую активную уксусную кислоту. Эта активная уксусна кислота через цикл трикарбоновых кислот окисляется в углекислоту и воду. При нарушении некоторых звеньев этого цикла ацетон может образовываться в результате декарбоксилирования ацетоуксусной кислоты. Ацетоуксусная кислота в свою очередь может образовываться путем присоединения двух молекул “активной” уксусной кислоты. Ацетон может образовываться из ацетоуксусной кислоты и при нарушении процесса расщепления некоторых аминокислот, таких, как фенилаланин, тирозин и лейцин. Образование промежуточных продуктов обмена ацетоуксусной и b-оксимасляной кислот происходит в печени. Потом эти кислоты попадают в ткани, где они окисляются к конечным продуктам обмена-углекислоты и воды. При недостаточном попадании в организм углеводов, голодании или нарушении их использования организмом (например, при диабете) изменяется процесс окисления недоокисленных продуктов обмена, в результате чего они появляются в моче. Чтобы промежуточные продукты обмена превращались в углекислоту и воду, необходимо присутствие щавелевоуксусной кислоты, которая образуется при расщеплении углеводов в печени. Отсюда выходит, что углеводы владеют антикетоногенным свойством, а жиры и белки, если они поступают в организм, могут вызвать кетонемию, то есть увеличение содержания ацетоновых тел в крови. Появление ацетоновых тел в моче называется кетонурией. В нормальной моче присутствуют лишь следы ацетоновых тел, которые не оказываются обычными качественными реакциями. Ацетонурия бывает алиментарного и патологического происхождения. Чаще всего ацетоновые тела появляются при диабете. При этом кетонурия часто соединяется с глюкозурией. При значительной кетонемии изменяется и кислотно-щелочное равновесие в организме. При кетонурии моча приобретает специфический резкий запах прелых плодов. Ацетон может выделяться также с потом и воздухом, который выделяется при дыхании. Особенно большое значение имеет выявление ацетонурии у детей раннего возраста. Часто ацетонемическая рвота и ацетон в моче наблюдается у истощенных детей, при токсичной диспепсии, дизентерии. Кетонемия и кетонурия может быть также следствием поражений желез внутренней секреции, например при тиреотоксикозе, из-за повышенного расходования углеводов, при усиленном образовании глюкокортикоидов (болезнь Кушинга), в результате увеличения мобилизации жира и уменьшения использования углеводов. Кетонурия может возникнуть также при лихорадке, голодании, сотрясениях мозга, резких эмоциональных возбуждениях, травмах черепа и др. Наиболее востребованными реакциями для качественного определения ацетоновых тел в моче являются пробы Ланге, Легаля и Герхардта. Эти пробы позволяют определить не только наличие ацетона, но и присутствие ацетоуксусной и b-оксимасляной кислот. Неорганический осадок мочи. Характер неорганического осадка мочи зависит от реакции мочи. В кислой мочы выпадают такие кристаллы, которых никогда не бывает в щелочной моче, и наоборот. Особенную группу составляет осадок, который встречается исключительно при урологических заболеваниях. В кислой моче в осадке имеющиеся аморфные ураты, кристаллы мочевой кислоты, щавелевокислого кальция, кислого фосфата кальция, мочевины, креатинина, аминокислот, индикана и пигментов. Щавелевокислый кальций (оксалат кальция) - прозрачные, бесцветные кристаллы, которые по своей форме напоминают почтовые конверты. Они встречаются в моче после приема еды, богатой щавелевой кислотой (щавель, помидоры, спаржа, зеленые бобы), при сахарном диабете, нефрите, подагре. Кислый фосфат кальция – большие призматические кристаллы, которые располагаются вроде розеток. Мочекислые соли (ураты) выпадают в виде кирпично-красного аморфного осадка при кислой реакции мочи или на холоде. Мочевина – важнейшая составная часть, которая содержит азот в моче. За сутки ее выделяется 10-35г. При микроскопии осадка мочи мочевина оказывается в виде длинных бесцветных призм. Содержание креатинина в моче составляет 0,5-2 г на сутки. Его кристаллы имеют форму блестящих призм. Гиппуровая кислота встречается в моче человека периодически. В суточной моче ее содержание колеблется от 0,1 до 1,0 г. Ее кристаллы имеют форму ромбических призм белого цвета. Мочевая кислота. Суточное выделение составляет от 0,4 до 1,0 г. В осадке мочи можно наблюдать разнообразные формы кристаллов мочевой кислоты, которые почти всегда имеют желтоватую расцветку. В щелочной моче могут быть в осадке аморфные фосфаты, фосфат-аммиак, магнезия, мочекислый аммоний и карбонат кальция. Аморфные фосфаты представляют собой фосфат извести и фосфат магнезии, которые выпадают в осадок в виде бесцветных мелких зернышек или шариков. Они напоминают ураты, но в отличие от них легко растворяются при добавлении кислот и не растворяются при нагревании. Мочекислый аммоний – единственная соль мочевой кислоты, которая встречается в щелочной моче. Чаще всего ее кристаллы имеют форму, напоминающую звезду. Фосфат аммиак-магнезия (трипельфосфат) – кристаллы ее имеют форму бесцветных трех- или шестиугольных призм. Кристаллы трипельфосфата наблюдают при приеме растительной еды, щелочных минеральных вод, воспалении мочевых путей, а также при щелочном брожении мочи. Углекислая известь (карбонат кальция) встречаются в осадке мочи в виде небольших шариков или кучек с 4-6 шариками. При добавлении к моче соляной кислоты происходит быстрое растворение кристаллов с выделением пузырьков углекислого газа. Кристаллы цистина имеют вид правильных, бесцветных шестигранных табличек. Они нерастворимы в воде, алкоголе и эфире, но растворимы в минеральных кислотах и в аммиаке, что позволяет отличить их от подобных кристаллических форм мочевой кислоты. Распознавание цистина необходимо с помощью химической реакции, которая применяется при исследовании цистинових камней. При отравлении фосфором, острой желтой атрофии печени, неукротимой рвоте беременных, скарлатине и некоторых других инфекционных болезнях в моче можно выявить лейцин и тирозин. Ксантин редко встречается в осадке мочи и получает практическое значение только тогда, когда формирование ксантиновых тел ведет к образованию почечных та пузырных камней. Кристаллы ксантина имеют форму мелких, бесцветных ромбов, которые напоминают точильный камень. Холестерин, как правило, наблюдается в моче при жировой дистрофии печени, эхинококкозе почек и хилурии. Кристаллы холестерина имеют вид тонких бесцветных ромбических табличек. Желчные пигменты. Кристаллы билирубина встречаются в моче, богатой желчными пигментами, при желтухе, вызванной тяжелыми заболеваниями или токсичными поражениями печени. Они представляют собой тонкие иглы, часто собранные в пучки, реже – ромбические таблички и, как правило, располагаются на поверхности лейкоцитов и эпителиальных клеток. Кристаллы билирубина легко растворяются в хлороформе. Желчные пигменты – билирубин и биливердин – появляются в моче только при патологии. В норме в моче здорового человека билирубин содержится в очень незначительных количествах и обычными качественными пробами не определяется. Желчные пигменты могут появиться в моче лишь в том случае, когда количество их в крови превышает так называемый почечный порог билирубина. Гипербилирубинемия и следующая за ней билирубинурия наблюдается при поражениях печени и желчных путей. Эти явления чаще всего наблюдаются при паренхиматозной и механической желтухах и являются признаком тяжелого органического поражения паренхимы печени. При паренхиматозных гепатитах интенсивность билирубинурии нарастает параллельно тяжести поражения печеночных клеток. Моча в присутствии желчных пигментов приобретает темную желто-зеленую расцветку. Пена такой мочи окрашена в желтый цвет, а капли мочи, которые попали на белье, оставляют на нем характерные желто-зеленые пятна. Билирубин и биливердин образуется в клетках ретикулоэндотелиальной системы печени, селезенки и костного мозга, при разрушении эритроцитов. Допускают, что расщепление билирубина начинается с разрыва a-метиновой связи порфиринового кольца с образованием вердогемоглобина. От молекулы вердогемоглобина происходит отщепление железа и глобина, после чего образуется полностью качественно новое соединение – гемобилирубин, или непрямой билирубин. Непрямой билирубин является пигментом оранжевого цвета, плохо растворимым в воде, циркулирующий в крови в виде тесного комплекса с альбуминами и не проходящий через почечный фильтр. С диазореактивом в реакции Ван-Ден-Берга он не дает прямой реакции. Непрямой билирубин выделяется клетками ретикуло-эндотелиальной системы и с током крови попадает в печень. В клетках печени (гепатоцитах) он теряет свой белковый компонент и превращается в прямой билирубин, или холебилирубин, связанный с глюкуроновой кислотой. Превращение непрямого билирубина в прямой заключается в его конъюгаци (связывании) с глюкуроновой кислотой под воздействием фермента уридилдифосфатглюкуронилтрансферазы с образованием двух производных билирубина: моно- и диглюкуронилбилирубинов. Оба этих соединения хорошо растворяются в воде и проходят через почечный фильтр, поэтому легко определяются прямой реакцией Ван- Ден- Берга на билирубин. Билирубин – пигмент желтовато-красного цвета, может легко окисляться с образованием по-разному окрашенных продуктов. Он имеет характер кислоты и входит в состав желчи в виде хорошо растворимых в воде солей щелочных металлов. Кальциевые соли билирубина, напротив, плохо растворяются в воде и могут выпадать из раствора в форме билирубиновой извести, которая часто является составной частью желчных камней. В норме образованный в печеночных клетках прямой билирубин поступает сначала по желчным путям в желчные протоки, а оттуда в желчный пузырь. Из желчного пузыря через общий желчный проток билирубин вместе с желчью попадает в кишку. В кишке под действием ферментов некоторых кишечных бактерий билирубин возобновляется в мезобилирубин и потом в стеркобилиноген и уробилиноген. Часть уробилиногена и стеркобилиногена всасывается кишечной стенкой и через воротную вену поступает в печень, где полностью окисляется в пропентдиопент и в дальнейшем, опять в билирубин, который выделяется в составе желчи. Большая часть образованного стеркобилиногена выделяется с калом. Стеркобилиноген легко окисляется на воздухе и превращается в стеркобилин, который является нормальным пигментом кала. Небольшая часть восстановленного билирубина всасывается из кишечника в кровь и через нижнюю половую вену поступает в почки в виде уробилиногена. Уробилиноген легко окисляется и выделяется с мочой в виде уробилина. Стеркобилиноген и стеркобилин, уробилиноген и уробилин по своим свойствам и химическим составом очень схожи между собой и соответсвуют пигментам кала и мочи. Появление желчных пигментов в моче может быть следствием повышенной билирубинемии за счет повышения количества прямого билирубина в сыворотке крови. С мочой может выделяться только прямой билирубин. Непрямой билирубин даже при очень высоком его содержании в крови с мочой не выделяется, так как связан с белками сыворотки и не может пройти через почечный фильтр. Выявление желчных пигментов в моче является диагностическим тестом в дифференциации механической и паренхиматозной желтух от гемолитической. При гемолитической желтухе в моче желчных пигментов нет, а количество уробилина и стеркобилина повышено. В норме уробилин в моче содержится в виде следов. При усиленном распаде эритроцитов образуется избыточное количество непрямого билирубина, холебилирубина и уробилиногена. В этих условиях печень не в состоянии превратить избыток уробилиногена и в крови накапливается непрямой билирубин. В моче нарастает уробилин. При паренхиматозном гепатите происходит поражение паренхимы печени и прямой уробилин может проникать через разрушенные печеночные клетки в кровь. При механической желтухе в результате обтурации общего желчного протока камнем или опухолью желчные капилляры переполняются желчью. В результате такого переполнения происходит сдавливание печеночных клеток, пропотевания желчи и всасывания ее в кровь. В этих случаях происходит усиленное выделение желчных пигментов с мочой из-за высокой гипербилирубинемии в крови. Для выявления желчных пигментов в моче применяют в основном количественные пробы. Большинство этих проб заключается в способности билирубина окисляться в биливердин под действием разных окислителей. На этом свойстве заключаются реакции Гмелина, Розенбаха и Розина. Качественными пробами на уробилин являются пробы Флоранса, Богомолова, Шлезингера и спектроскопия. Желчные кислоты появляются в моче лишь при механической желтухе, когда возникает обтурация желчевыводящих путей. Определение желчных кислот осуществляется с помощью пробы Гея.
ИССЛЕДОВАНИЕ ФУНКЦИИ ПОЧЕК Методы иследования очистительной функции почек включают исследование содержания в крови конечных продуктов белкового обмена; экскреторные пробы с нагрузкой разнообразными веществами; пробы на очищение (клиренс-тесты). Определение концентрации мочевины в крови более показательно, чем измерение остаточного азота. Содержание мочевины в крови определяют газометрами, прямыми фотометрическими и ферментативными методами. В норме в сыворотке крови уровень мочевины 2,5-8,3ммоль/л. В начальном периоде почечной недостаточности ранее других азотных веществ начинает увеличиваться концентрация в крови мочевой кислоты, потом индикана, мочевины и в конце креатинина. Поэтому определение содержания индикана в крови имеет большое значение для более раннего выявления почечной недостаточности, а определение креатинина имеет большое прогностическое значение. Содержание индикана в крови в норме незначительно и не оказывается качественными пробами. Количество индикана в крови определяют по методику Альтгаузена или Обермейера. Содержание креатинина в крови в норме составляет 0,044-0,178 ммоль/л и определяется мышечной массой. В качестве унифицированного метода определения креатинина утвержденный метод Попера, основанный на цветной реакции М.Яффе. В моче азотные вещества имеются в очень больших количествах, которые превышают их содержание в крови в 100 и больше раз. Определение мочевины и креатинина в моче проводится теми же методами, что и в крови. Для более точного определения функции почек предложили сравнивать концентрацию данного вещества в крови и в моче. Амбар предложил метод определения коэффициента отношения мочевины крови и мочевины в моче (константа Амбара) по формуле:
где К - константный коэффициент; Мк - концентрация мочевины в крови (гр/л); См – количество мочевины, выделенной с мочой за сутки (г); Мм – содержание мочевины в моче (гр/л); 70 – условная средняя масса тела взрослого человека (кг); В – масса тела больного (кг); 5 – расчетный коэффициент. При нормальной функции почек константный коэффициент колеблется от 0,06 до 0,08. При почечной недостаточности величина константы превышает 0,1. В ряде случаев константа Амбара дает более раннее представление о почечной недостаточности, что начинается, чем простое определение содержания мочевины в сыворотке крови. Оценка функции почек по нагрузке экзогенными веществами. Принцип этих методов заключается в том, что больной принимает внутрь или ему вводят парентерально определенное вещество, а затем наблюдают через сколько времени они начинает выделяться с мочой и какое количество их выделяется в определенный промежуток времени. Наиболее ценными и специфическими из всех проб для функционального исследования почек является определение коэффициента очистки или клиренса, так называемые клиренс-тесты, что позволяют исследовать важнейшую функцию почек – очистки. Впервые клиренс-тест как метод количественной оценки функции почек был введен в практику Ребергом (1926) – клиренс креатинина и Ван-Слайком (1929) – клиренс мочевины. Под сроком коэффициент очистки, или клиренс, понимают объем плазмы (в мл), который полностью освобождается от экзогенного или эндогенного вещества за 1 мин (то есть выражается в мл/мин). Таким образом, клиренс-тест характеризует степень очистки крови, которая протекает через почки в единицу времени от определенных веществ. Поскольку функция почек осуществляется путем клубочковой фильтрации, канальцевой реабсорбции и секреции, в зависимости от механизма выделения исследуемого вещества почками можно получить представление о функциональном состоянии разных отделов нефрона.
|
|||||||||
|
Последнее изменение этой страницы: 2017-01-25; просмотров: 157; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.221.187.121 (0.035 с.) |