Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Общий химический состав мышечной тканиСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
БИОХИМИЧЕСКИЕ АСПЕКТЫ ФИЗИЧЕСКИХ НАГРУЗОК
(Учебно-методическое пособиедля студентов медицинских факультетов, спортивных врачей, реабилитологов, преподавателей физической культуры)
Запорожье 2012
Утверждено на заседании Центрального методического Совета ЗГМУ (протокол № от «» ноября 2012 г.) и рекомендовано для использования в учебном процессе.
Учебно-методическое пособие составили:
Рецензенты:
Содержание
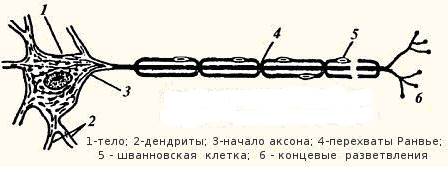
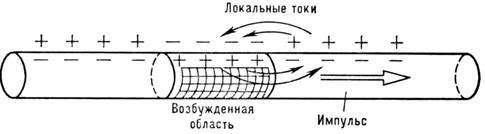
Скелетные мышцы Скелетные мышцы обеспечивают движение и поддержание позы нашего тела. Скелетная мышечная ткань представлена волокнами из длинных многоядерных клеток до 30 см длиной и диаметром от 10 до 100 микрон. Фактически это надклеточное образование – симпласт, образуется в эмбриональном периоде путем слияния 200-300 клеток миобластов. Мышечные клетки не способны к делению и численность их может увеличиваться только за счет спящих, заложенных в эмбриональный период клеток — сателлитов. К каждому мышечному волокну подходит аксон двигательного нерва (рис. 3) и присоединяется несколькими синапсами. В синапсах происходит передача нервного импульса на мышечную клетку. Двигательный нерв вместе с мышечной клеткой называется двигательной единицей. Как и любая клетка нашего организма, миоцит окружен мембраной – сарколеммой, которая способна осуществлять трансмембранный транспорт ионов или молекул. Непрерывная работа калево-натриевого насоса, потребляя около 40% энергии клетки, создаёт разность в концентрации ионов на мембране. Это приводит к разности потенциалов. Такой заряд называется потенциалом покоя (ПП). Именно он обеспечивает избирательный транспорт веществ через мембрану клетки. От сарколлемы отходит серия мембранных впячиваний, называемых поперечными трубочками (Т-трубочками). Нервный импульс, приходящий от двигательного нейрона по аксону (рис. 4), приводит к выделению из синапса нейрона нейромедиатора ацетилхолина (АХ) (рис 5). АХ вызывает на сарколлеме миоцита деполяризацию с образованием потенциала действия (ПД) (рис. 5).
Рис. 3. Периферический мотонейрон с миелинизированным аксоном.
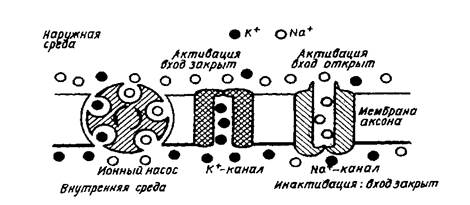
Рис. 4. Перемещение импульса по аксону
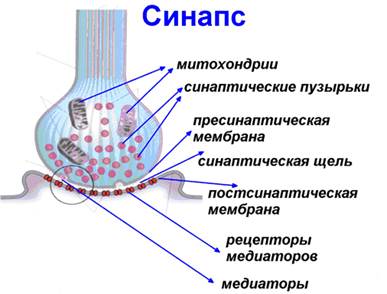
Рис. 5. Строение синапса
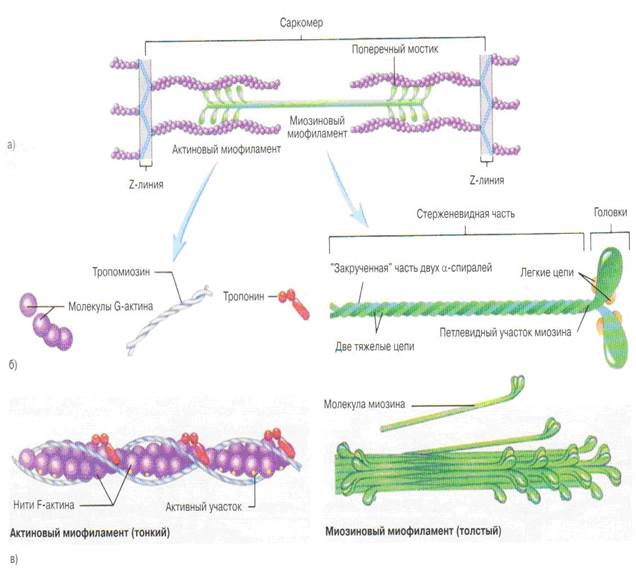
Рис. 6. Структурные компоненты мембран, участвующих в генерации потенциала действия. Потенциал действия приводит к поступлению ионов Nа+ по Т-трубочкам внутрь мышечной клетки, вытесняя ионы Са2+ из саркоплазматического ретикулума. Каждое мышечное волокно окружено сарколеммой, а внутри находятся многочисленные сократительные нити — миофибриллы. Миофибриллы состоят из саркомеров, которые в свою очередь подразделяются на филаменты. Филаменты бывают двух типов — толстые (молекулы миозина) и тонкие (белки актин, тропомиозин и тропонин). Так как они образованы различными по плотности белками, под микроскопом в миофибрилле видны чередующиеся темные и светлые полосы. Отсюда и название скелетной мышечной ткани – поперечно-полосатая. Саркомер – наименьшая единица мышечного волокна, способная к сокращению (рис. 7). Темные полосы миозиновых филаментов сменяются светлыми дисками. По середине диска имеется более светлая полоса, называемая зоной Н, в которой толстые филаменты не перекрываются тонкими. Н-зона видна только в расслабленном состоянии мышечного волокна. С обеих сторон саркомер ограничен Z дисками. Z-линия – это белковый слой в форме диска, к которому прикреплены тонкие филаменты, то есть актиновые нити. Они простираются через диск І и частично проникают в диск А. Таким образом, белки, составляющие саркомеры, образуют миофибриллы, соединяющие концы клетки, сближая их при сокращении. Сарколемму мышечных клеток покрывают коллагеновые волокна, которые к концу мышечных клеток превращаются в сухожилия. Этими сухожилиями мышцы прикрепляются и срастаются с надкостницей костей скелета. Обычно мышцы одним концом крепятся выше, а другим – ниже сустава. При таком креплении сокращение мышцы приводит в движение кости в суставах.
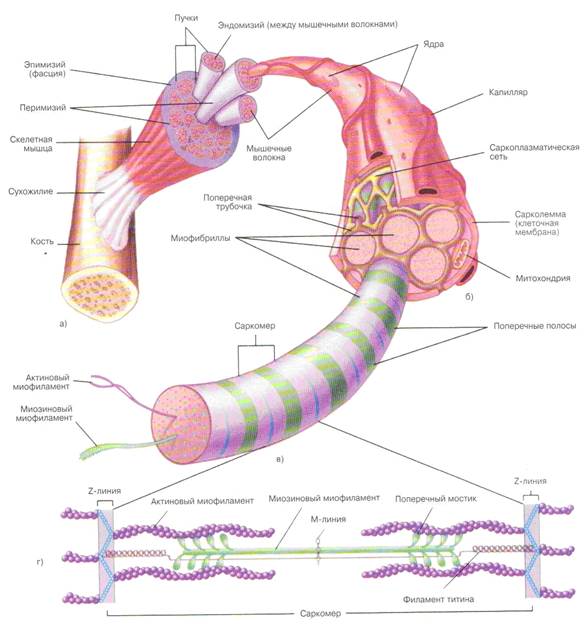
Рис. 7. Строение мышечного волокна и саркомера: а — фрагмент мышцы, прикрепленной к кости сухожилием. Мышца состоит из мышечных фасцикул, каждый из которых окружен перимизием. Фасцикулы состоят из пучков отдельных мышечных волокон (мышечных клеток), каждый из которых окружен эндомизием, б — увеличенное мышечное волокно. Мышечное волокно содержит несколько миофибрилл; в — миофибрилла простирается за конец мышечного волокна. Структура саркомеров показана в миофибрилле; г — отдельный саркомер миофибриллы состоит из актиновых и миозиновых миофиламентов, Z-линии удерживают актиновые миофиламенты, тогда как молекулы актина и М-линии удерживают на месте миозиновые миофиламенты.
Соединительная ткань проникает в полость самой мышцы, уменьшаясь при этом по толщине. В связи с этим происходит разделение мышцы на все более и более мелкие компартменты (рис. 7). Наименьшими из них являются пучки, включающие большое количество мышечных волокон, прикрепленных друг к другу соединительной тканью. Мышечную ткань пронизывает большое количество кровеносных сосудов, по которым кровь снабжает их кислородом, питательными веществами, удаляет продукты обмена веществ.
Саркоплазматические белки В основном предствлены ферментами гликолиза, азотного и липидного обменов, а также белками, локализованными в митохондриях, лизосомах рибосомах. Одним избелков мышечной клетки является внутриклеточный дыхательный пигмент миоглобин. Он обуславливает красный цвет саркоплазмы. Это глобулярный белок, осуществляющий в мышцах запасание (депонирование) молекулярного кислорода и передачу его окислительным системам клеток. Подобно гемоглобину, он вступает в реакцию с кислородом при быстром сокращении мышц. Обратимое связывание миоглобина с кислородом происходит уже при низких парциальных давлениях кислорода (PO2). Это имеет большое физиологическое значение: при сокращении мышц в результате сжатия капилляров PO2 резко падает. Именно в этот момент происходит высвобождение из миоглобина кислорода, необходимого работающей мышце Миофибрилярные белки Сократительные белки миозин и актин входят в состав нитевидных миофибрилл, толщина которых 1-3 мкм. Длина миофибрилл равна длине мышечной клетки, в которую они входят. Их количество в клетке может колебаться от 500 до 2500, что составляет основную часть мышечной клетки (до 80 процентов объёма или более половины сухого веса). В саркомере тонкие и толстые филаменты миофибриллы перекрываются (рис. 8). Тонкие нити располагаются вокруг толстого филамента по углам шестигранника таким образом, что каждая тонкая нить занимает симметричное положение между тремя толстыми нитями, а каждая толстая нить симметрично окружена шестью тонкими. На молекулярном уровне тонкие филаменты включают белки ― актин, тропомиозин и тропонин I, С, Т.
Рис. 8. Структура актина и миозина: а – саркомер состоит из актиновых (тонких) и миозиновых (толстых) миофиламентов; актиновые миофиламенты прикреплены к Z-линиям, а миозиновые миофиламенты «подвешены» между актиновыми миофиламентами; б – актиновые миофиламенты состоят из отдельных молекул (окрашены) глобулярного актина (G-актина), молекул тропомиозина (полоски) и тропонина (шары); молекула миозина представляет собой структуру, по форме напоминающую клюшку для игры в гольф и состоящую из двух молекул тяжелого миозина, сплетенных вместе и образующих стержневидную часть и двойную глобулярную головку; четыре меньшего размера молекулы легкого миозина расположены на головках миозиновой молекулы; в – молекулы G-актина, молекулы нитевидного тропомиозина и молекулы глобулярного тропонина собраны в единый миофиламент актина; активные участки находятся на молекулах G-актина; миозиновые миофиламенты состоят из множества отдельных миозиновых молекул; стержневидные части расположены параллельно, все головки обращены в одном направлении у одного конца и в противоположном направлении – у другого конца миозинового миофиламента.
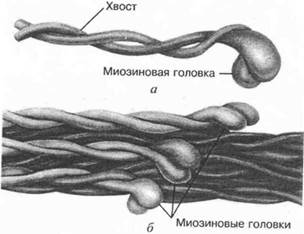
Толстые филаменты образованы белком миозином. Миозин по своему строению – сложный белок, имеющий четвертичную структуру. Молекулярная масса — 470000 Да. В его состав входят 6 субъединиц: две фибриллярной и четыре глобулярной структуры. В саркомере молекулы миозина соединены хвостиками в жгуты по 150 штук, направленные головками в противоположные стороны, образуя толстые нити – филаменты (рис. 9). Линия соединения хвостов миозина называется линией М. Глобулярные участки миозина обладают ферментативными свойствами и в присутствии активатора – ионов кальция, способны расщеплять АТФ до АДФ. Получаемая энергия используется для образования водородной связи между головкой миозина и молекулой актина и её сгибания, что приводит к смещению тонких нитей филаментов относительно толстых.
Рис. 9. Строение миозина.
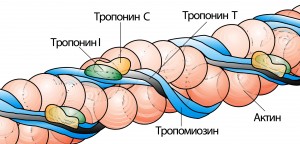
Тонкие нити состоят из трех белковых молекул (рис. 10), каждая из которых имеет четвертичную структуру. Самым высокомолекулярным из них является актин с молекулярной массой 42000 Да. В состоянии покоя одна из нитей актина находится в фибриллярном состоянии, а вторая состоит из отдельных глобулярных частей, которые, полимеризуясь, образуют вторую фибриллярную нить.
Рис. 10. Строение тонких филаментов Тропомиозин — белок, который состоит из двух полипептидных нитей и обматывает двойную спиралевидную молекулу актина. Это препятствует образованию связей между головками миозина и актином и, следовательно, препятствует самопроизвольному скольжению (своеобразный замок). Третий белок в этом комплексе — тропонин. Это белок четвертичного уровня организации, состоит из трех субъединиц ТнТ, ТнI, ТнС. Эти субъединицы обеспечивают его связь с актином и тропомиозином. Фрагмент ТнС обладает ферментативной активностью. При наличии активатора – ионов кальция, тропонин может освобождать актин от тропомиозина, а, следовательно, позволяет актину образовывать комплекс с миозином и сдвигаться относительно миозина. Типы мышечных волокон У человека скелетные мышцы состоят из волокон двух типов. Они отличаются по морфологическим, метаболическим и сократительным свойствам. Красные скелетные мышечные волокна – медленно сокращающиеся (это тип 1) и белые – быстро сокращающиеся (тип 2). Главным различием является механизм ресинтеза АТФ, используемый в них. Так называемые белые мышечные волокна подразделяются на Тип 2А (используются как аэробный, так и анаэробный ресинтез АТФ) и тип 2В (используется анаэробный ресинтез АТФ). По скорости развёртывания анаэробные пути быстрее, но по продолжительности ресинтеза АТФ – кратковременны, поэтому белые волокна сокращаются быстро, но и быстро устают. Красные волокна сокращаются в четыре раза медленнее, но за счет аэробного энергообмена практически неутомимы. В зависимости от функционального значения мышц (расположение в скелете) в них преобладают те или иные типы волокон. В мышцах спины поддерживающих позу тела, пробладают красные типы волокон, в перемещении зрачка глаза – белые волокна. Соотношение числа красных и белых волокон в конечностях передаётся генетически и обуславливает деление нас на спринтеров и стаеров. Отличие в механизме ресинтеза АТФ приводит к отличию мышечных волокон по таким характеристикам: Таблица 1 Характеристика типов мышечных волокон у человека
СЕРДЕЧНАЯ МЫШЕЧНАЯ ТКАНЬ
Кардиомиоциты (рис. 12), входящие в сердечную мышцу, представлены двумя типами клеток: обычные миоциты, которые во многом схожи с клетками скелетной мышечной ткани и образуют мышцы предсердий и мышцу желудочков и атипичные кардиомиоциты (специальные клетки), обладающие свойством ритмической автоматии и проводимости возбуждения.
Рис. 12. Клетки сердечной мышцы (кардиомиоциты). Тёмным окрашены ядра. Полное прекращение деления кардиомиоцитов (КМЦ) в сердце млекопитающих в первую неделю постнатальной жизни является неразрешенной загадкой эволюции и не преодолимым препятствием для гистотипической регенерации поврежденного миокарда у человека. Проводящие сердечные миоциты или атипичные кардиомиоциты, обеспечивают ритмичное координированное сокращение различных отделов сердца. Они способны к генерации и быстрому проведению электрических импульсов. Совокупность атипичных кардиомиоцитов формирует так называемую проводящую систему сердца. В состав проводящей системы входят: · синусно-предсердный, или синусный, узел; · предсердно-желудочковый узел; · предсердно-желудочковый пучок (пучок Гиса) и · его разветвления (волокна Пуркинье), передающие импульсы на сократительные мышечные клетки. Различают три типа миоцитов, которые в разных соотношениях находятся в различных отделах проводящей системы сердца. 1. Первый тип проводящих миоцитов - это P-клетки, или пейсмейкерные миоциты, - водители ритма. Они светлые, мелкие, отросчатые. Эти клетки встречаются в синусном и предсердно-желудочковом узле и в межузловых путях. Они служат главным источником электрических импульсов, обеспечивающих ритмическое сокращение сердца. При слабом развитии саркоплазматической сети высокое содержание свободного кальция в цитоплазме этих клеток обусловливает способность клеток синусного узла генерировать импульсы к сокращению. Поступление необходимой энергии обеспечивается преимущественно процессами анаэробного гликолиза. 2. Второй тип проводящих миоцитов - это переходные клетки. Они составляют основную часть проводящей системы сердца. Это тонкие, вытянутые клетки, встречаются преимущественно в узлах (их периферической части), но проникают и в прилежащие участки предсердий. Функциональное значение переходных клеток состоит в передаче возбуждения от Р-клеток к клеткам пучка Гиса и рабочему миокарду. 3. Третий тип проводящих миоцитов - это клетки Пуркинье. Они часто лежат пучками. Они светлее и шире сократительных кардиомиоцитов, содержат мало миофибрилл. Эти клетки преобладают в пучке Гиса и его ветвях. От них возбуждение передается на сократительные кардиомиоциты миокарда желудочков. Сердечная мышца работает в определенном ритме, чередуя сокращение (систола) около 0,4 сек. и расслабление (диастола) около 0,6 сек. Сердечная мышца за время жизни среднего человека успевает совершать около трёх миллиардов циклов сокращения и расслабления. Работа миокарда не подвластна воле человека и частота сердечных сокращений (ЧСС) регулируется симпатической, парасимпатической нервной системами и гормонально. При микроскопии с небольшим увеличением видно, что сердечная мышечная ткань представляет собой единую сеть, состоящую из высокоорганизованных сильно ветвящихся и воссоединяющихся вновь мышечных клеток. Эти клетки длиной ~110 мкм и шириной ~15 мкм связаны друг с другом по преимуществу из конца в конец (рис. 13) особыми соединениями – вставочными дисками.
Рис. 13. Строение кардиомиоцита
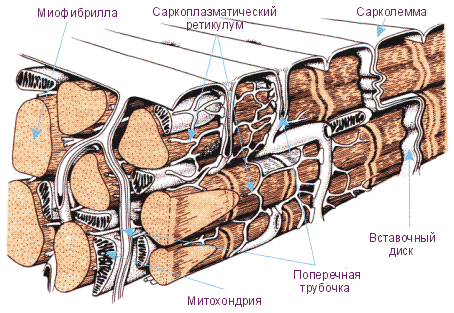
Важными компонентами каждой клетки кардиомиоцита, обеспечивающими любые её функции, являются внешняя мембрана (сарколемма), система поперечных трубочек, связанных с Z‑дисками, продольный саркоплазматический ретикулум и терминальные цистерны, а также митохондрии (рис. 14). По периферии клетки и между митохондриями находится множество частичек гликоген. Строение главной структуры кардиомиоцита – миофибриллы подобно строению миофибриллы скелетной поперечнополосатой мышечной ткани. Как и скелетная, сердечная мышечная ткань имеет поперечную исчерченность. При большем увеличении видно, что эта исчерченность, также как и в миоцитах скелетной мышечной ткани, обусловлена упорядоченным положением актиновых и миозиновых нитей, собранных в пучки в миофибриллах. Толстые (миозиновые) и тонкие (актин, тропонин и тропомиозин) белковые нити упорядочены в сократительные единицы (саркомеры, простирающиеся от одного до другого Z‑диска) с поперечной исчерченностью, подобной той, что есть в скелетной мышечной ткани. Темные полосы, пересекающие миофибриллы - это соединения отдельных клеток. Их называют вставочными дисками. Они образованы мембранами соседних кардиомиоцитов, образующих сердечное мышечное волокно. Электрическое сопротивление такого соединения составляет ~1/400 сопротивления сарколеммы волокна сердечной мышечной ткани. Через соединение осуществляются хорошо управляемые ионные потоки. Потенциал действия, движущийся по оси одной клетки, легко переходит через вставочный диск на соседний кардиомиоцит. Эффективное взаимодействие кардиомиоцитов через многочисленные вставочные диски позволяет считать, что сердечная мышечная ткань образует два функциональных синцития: предсердный синцитий и желудочковый синцитий. Хотя морфологическими синцитиями они не являются. Эти функциональные синцитии отделены друг от друга соединительной тканью, окружающей клапанные отверстия. Однако синцитии могут эффективно взаимодействовать друг с другом через специальную проводящую систему (атриовентрикулярный пучок).
Рис. 14. А. Сердечная мышечная ткань. Б. Сокращение и расслабление миофибрилл происходит в результате изменения концентрации ионов кальция (Са2+) в цитозоле кардиомиоцитов. Ионы кальция входят в расслабления кардиомиоцита. Небольшое количество ионов кальция транспортируется через сарколемму из цитозоля посредством кальций-натриевого насоса и заменяется ионами натрия (Na+). Кальций-натриевый насос имеет меньшее значение в трансмембранных потоках ионов кальция, чем кальциевый насос. В. Нити актина и миозина вдвигаются друг в друга. Степень перекрытия нитей актина и миозина определяет сокращение и расслабление кардиомиоцитов во время систолы и диастолы. Г. Глобулярные части (головки) нитей миозина взаимодействуют с нитями актина и обеспечивают скольжение (вдвижение или выдвижение) нитей вдоль их главных осей и сокращение или расслабление кардиомиоцитов.
Возникновение мембранного потенциала кардиомиоцитов обусловлено избирательной проницаемостью их мембраны для ионов калия. Его величина у сократительных кардиомиоцитов составляет 80-90 мВ а у клеток синоатриального узла 60-65 мВ. Возбуждение кардиомиоцитов проявляется генерацией потенциалов действия, которые имеют своеобразную форму. В них выделяются следующие фазы: 1. Фаза деполяризации 2. Фаза быстрой начальной реполяризации 3. Фаза замедленной реполяризации 4. Фаза быстрой конечной реполяризации. Длительность ПД кардиомиоцитов составляет 200-400 мсек. Это во много раз больше, чем у нейронов или скелетных миоцитов. Амплитуда ПД около 120 мВ. Фаза деполяризации связана с открыванием натриевых и кальциевых каналов мембраны, по которым эти ионы входят в цитоплазму. Фаза быстрой начальной реполяризации обусловлена инактиваиией натриевых, а замедленной кальциевых каналов. Одновременно активируются калиевые каналы. Ноны калия выходят из кардиомиоцитов, развивается фаза быстрой конечной реполяризации. Автоматия, т.е. генерация спонтанных ПД пейсмекерными клетками обусловлена тем, что их мембранный потенциал не остается постоянным. В период диастолы в Р-клетках синоатриального узла происходит его медленное уменьшение. Это называется медленной диастолической деполяризацией МДД. Когда ее величина достигает критического уровня, генерируется ПД, который по проводящей системе распространяется на все сердце. Возникает систола предсердий, а затем желудочков. Медленная диастолическая деполяризация связана с постепенным нарастанием натриевой проницаемости мембраны атипических кардиомиоцитов. Истинными пейсмекерами является лишь небольшая группа Р-клеток синоатриального узла. Остальные Р-клеткн проводящей системы являются латентными водителями ритма. Пока спонтанные ПД поступают из синоатриального узла, латентные пейсмекеры подчиняются его ритму. Это называется усвоением ритма. Но как только проведение нарушается, в них начинают генерироваться собственные спонтанные ПД. Поэтому при некоторых заболеваниях возникает патологическая импульсация в клерках проводящей системы, миокарде предсердий и желудочков. Такие очаги автоматии называют эктопическими т.е. смешенными. Сокращение кардиомиоцитов, как и других мышечных клеток является следствием генерации ПД. В них как и в скелетных миоцитах, имеется система трубочек саркоплазматического ретикулума содержащих ионы кальция. При возникновении ПД эти ионы выходят из трубочек в саркоплазму. Начинается скольжение миофибрилл. Нов. сокращении кардиомиоцитов принимают участие и ионы кальция, входящие в них в период генерации ПД. Они увеличивают длительность сокращения и обеспечивают пополнение запасов кальция в трубочках.
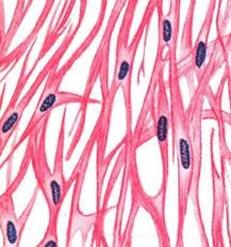
Гладкие мышцы Структурно-функциональной единицей гладкой мышечной ткани внутренних органов и сосудов является миоцит. Представляет собой чаще всего веретенообразную клетку (длиной 20-500 мкм, диаметром 5-8 мкм), покрытую снаружи базальной пластинкой, но встречаются и отростчатые миоциты. В центре располагается вытянутое ядро(Рис 15), по полюсам которого локализуются общие органеллы: зернистая эндоплазматическая сеть, пластинчатый комплекс, митохондрии, цитоцентр. В цитоплазме содержатся толстые (17 нм) миозиновые и тонкие (7 нм) актиновые миофиламенты, которые располагаются в основном параллельно друг другу вдоль оси миоцита и не образуют А и I диски, чем и объясняется отсутствие поперечной исчерченности миоцитов. В цитоплазме миоцитов и на внутренней поверхности плазмолеммы встречаются многочисленные плотные тельца, к которым прикрепляются актиновые, миозиновые, а так же промежуточные филаменты. Плазмолемма образует небольшие углубления - кавеолы, которые рассматриваются как аналоги Т-канальцев. Под плазмолеммой локализуются многочисленные везикулы, которые вместе с тонкими канальцами цитоплазмы являются элементами саркоплазматической сети. Механизм сокращения в миоцитах в принципе сходен с сокращением саркомеров в миофибриллах в скелетных мышечных волокнах. Он осуществляется за счет взаимодействия и скольжения актиновых миофиламентов вдоль миозиновых. Для такого взаимодействия также необходимы энергия в виде АТФ, ионы кальция и наличие биопотенциала. Биопотенциалы поступают от эфферентных окончаний вегетативных нервных волокон непосредственно на миоциты или опосредованно от соседних клеток через щелевидные контакты и передаются через кавеолы на элементы саркоплазматической сети, обуславливая выход из них ионов кальция в саркоплазму. Под влиянием ионов кальция развиваются механизмы взаимодействия между актиновыми и миозиновыми филаментами, аналогичные тем, которые происходят в саркомерах скелетных мышечных волокон, в результате чего происходит скольжение названных миофиламентов и перемещение плотных телец в цитоплазме. В миоцитах, кроме актиновых и миозиновых филаментов, имеются еще промежуточные, которые одним концом прикрепляются к цитоплазматическим плотным тельцам, а другим - прикрепительным тельцам на плазмолемме и таким образом передают усилия взаимодействия актиновых и миозиновых филаментов на сарколемму миоцита, чем и достигается его укорочение. Миоциты окружены снаружи рыхлой волокнистой соединительной тканью - эндомизием и связаны друг с другом боковыми поверхностями. При этом, в области тесного контакта соседних миоцитов базальные пластинки прерываются. Миоциты соприкасаются непосредственно плазмолеммами и в этих местах имеются щелевидные контакты, через которые осуществляется ионная связь и передача биопотенциала с одного миоцита на другой, что приводит к одновременному и содружественному их сокращению. Цепь миоцитов, объединенных механической и метаболической связью, составляет функциональное мышечное волокно. В эндомизии проходят кровеносные капилляры, обеспечивающие трофику миоцитов, а в прослойках соединительной ткани между пучками и слоями миоцитов в перимизии проходят более крупные сосуды и нервы, а также сосудистые и нервные сплетения. Эфферентная иннервация гладкой мышечной ткани осуществляется вегетативной нервной системой. При этом, терминальные веточки аксонов эфферентных вегетативных нейронов, проходя по поверхности нескольких миоцитов, образуют на них небольшие варикозные утолщения, которые несколько прогибают плазмолемму и образуют мионевральные синапсы. При поступлении нервных импульсов в синаптическую щель выделяются медиаторы (ацетилхолин или норадреналин), и обуславливают деполяризацию мембран миоцитов и последующее их сокращение. Через щелевидные контакты биопотенциалы переходят из одного миоцита на другой, что сопровождается возбуждением и сокращением и тех гладкомышечных клеток, которые не содержат нервных окончаний. Возбуждение и сокращение миоцитов обычно продолжительны и обеспечивают тоническое сокращение гладкой мышечной ткани сосудов и полых внутренних органов, в том числе гладкомышечных сфинктеров. В этих органах содержатся и многочисленные рецепторные окончания в виде кустиков, деревцев или диффузных полей.
1 2 Рис. 15. Гладкомышечные клетки: 1 – общий вид; 2 – А – в расслабленном состоянии; Б – в сокращенном состоянии; 1 – ядро; 2 – плотные тельца, прикрепленные к цитолемме (тельца прикрепления); 3 – промежуточные миофиламенты.
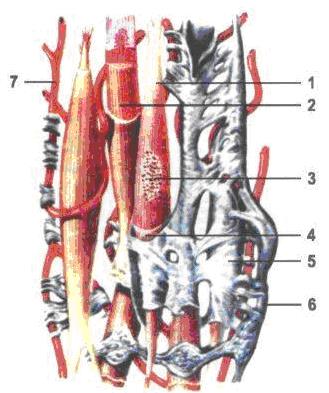
Автоматия. Многим внутренним органам и сосудам присуща автоматия гладких мышц, т.е. способность к автоматической (спонтанной) деятельности. Потенциал действия гладких мышечных клеток имеет авторитмический (пейсмекерный) характер, подобно потенциалам проводящей системы сердца. Пейсмекерные потенциалы регистрируются в различных участках гладкой мышцы. Это свидетельствует о том, что любые клетки висцеральных гладких мышц способны к самопроизвольной автоматической активности. Реакция на растяжение. Уникальной особенностью клеток гладких мышц является их связь мостиками из внутриклеточных белков. Через эти мостики в основном передается сила сокращения от одной клетки к другой. В мышечном волокне среди актиновых нитей разбросаны миозиновые нити. Их диаметр более чем в 2 раза превышает диаметр актиновых нитей. На электронных микрофотографиях актиновых нитей обычно обнаруживают в 5-10 раз больше, чем миозиновых. На рис. 16 представлена предполагаемая структура отдельной сократительной единицы внутри гладкомышечной клетки, где видно большое число актиновых нитей, исходящих от двух плотных телец; концы этих нитей перекрывают миозиновую нить, расположенную посередине между плотными тельцами. Эта сократительная единица похожа на сократительную единицу скелетной мышцы, но без специфической регулярности ее структуры. В сущности, плотные тельца гладкой мышцы играют ту же роль, что и Z-диски в скелетной мышце.
Рис. 16. Построение гладкой мышечной ткани: 1 – миоцит; 2 – миофибриллы в саркоплазме; 3 – ядро миоцита; 4 – сарколема; 5 – ендомизий; 6 – нерв; 7 – кровеносный капилляр.
Существует и другое различие. Большинство миозиновых нитей имеют поперечные мостики с так называемой боковой полярностью. Мостики организованы следующим образом: на одной стороне они шарнирно фиксируются в одном направлении, а на другой — в противоположном направлении. Это позволяет миозину тянуть актиновую нить с одной стороны в одном направлении, одновременно продвигая с другой стороны другую актиновую нить в противоположном направлении. Такая организация позволяет гладкомышечным клеткам сокращаться с укорочением до 80% их длины, в отличие от 30% укорочения, характерного для скелетной мышцы. Висцеральные гладкие мышцы характеризуются нестабильным мембранным потенциалом. Колебания мембранного потенциала независимо от нервных влияний вызывают нерегулярные сокращения, которые поддерживают мышцу в состоянии постоянного частичного сокращения — тонуса. Тонус гладких мышц отчетливо выражен в сфинктерах полых органов: желчном и мочевом пузырях, в месте перехода желудка в двенадцатиперстную кишку и тонкой кишки в толстую, а также в гладких мышцах мелких артерий и артериол. Мембранный потенциал гладкомышечных клеток не является отражением истинной величины потенциала покоя. При уменьшении мембранного потенциала мышца сокращается, при увеличении — расслабляется. Платообразные потенциалы действия (ПД) обеспечивают поступление в цитоплазму миоцитов значительного количества внеклеточного кальция, участвующего в последующем в активации сократительных белков гладкомышечных клеток. Ионная природа ПД гладкой мышцы определяется особенностями каналов мембраны гладкой мышечной клетки. Основную роль в механизме возникновения ПД играют ионы Са2+. Кальциевые каналы мембраны гладких мышечных клеток пропускают не только ионы Са2+, но и другие двухзарядные ионы (Bа 2+, Mg2+), а также Na+. Вход Са2+ в клетку во время формирования ПД необходим для поддержания тонуса и развития сокращения. Поэтому блокирование кальциевых каналов мембраны гладких мышц, приводящее к ограничению висцеральной гладкой мышцы, является ее реакция на растяжение. В ответ на растяжение гладкая мышца сокращается. Это вызвано тем, что растяжение уменьшает мембранный потенциал клеток, увеличивает частоту ПД и в конечном итоге — тонус гладкой мускулатуры. В организме человека это свойство гладкой мускулатуры служит одним из способов регуляции двигательной деятельности внутренних органов. Например, при наполнении желудка происходит растяжение его стенки. В ответ на его растяжение увеличивается тонус стенки желудка. Этоспособствует сохранению объема органа и лучшему контакту его стенок с поступившей пищей. В кровеносных сосудах растяжение, создаваемое колебаниями кровяного давления, является основным фактором миогенной саморегуляции тонуса сосудов. Наконец, растяжение мускулатуры матки растущим плодом служит одной из причин начала родовой деятельности. Пластичность. Еще одной важной специфической характеристикой гладкой мышцы является изменчивость напряжения без закономерной связи с ее длиной. Так, если растянуть висцеральную гладкую мышцу, то ее напряжение будет
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2017-01-24; просмотров: 455; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 13.59.129.141 (0.021 с.) |



 Белкимышечного волокна
Белкимышечного волокна