
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
При составлении уравнений окислительно-восстановительных реакций в основном используют 2 метода: метод электронного баланса и метод электронно-ионного баланса.Содержание книги
Поиск на нашем сайте
Метод электронного баланса реализуется в несколько стадий: 1) установление формул исходных веществ и продуктов реакции; 2) определение степеней окисления элементов в реагентах и продуктах реакции; 3) определение числа электронов, отданных восстановителем и принятых окислителем; 4) определение коэффициентов перед формулами реагентов и продуктов реакции. Метод электронно-ионного баланса более универсален по сравнению с методом электронного баланса и имеет неоспоримое преимущество при подборе коэффициентов во многих окислительно-восстановительных реакциях, особенно протекающих с участием органических соединений, в которых процедура определения степеней окисления является очень сложной. Составление уравнений этим методом осуществляется через ряд стадий: 1) определение окислителя и восстановителя, а также продуктов окисления и восстановления; 2) составление ионно-молекулярных уравнений полуреакций (окисления и восстановления) с учетом электронов; 3) определение на основе требования электронного баланса коэффициентов перед строками уравнений полуреакций; 4) суммирование левых и правых частей уравнений полуреакций и составление на этой основе уравнения окислительно-восстановительной реакции в ионно-молекулярной форме; 5) переход от ионно-молекулярной формы окислительно-восстановительной реакции к молекулярной. При реализации этой последовательности необходимо придерживаться ряда правил. К ним относятся: 1) Участники реакции (реагенты и продукты) записываются в уравнениях полуреакций в той форме, в которой они присутствуют в растворе. Например, если в качестве окислителя используется сильный электролит дихромат калия, то в качестве окислителя в уравнении полуреакции записывают анион Cr2O72-, реально присутствующий в растворе и осуществляющий функцию окисления. В то же время восстановитель, сульфид железа (II) FeS, записывается в молекулярной форме, поскольку он нерастворим и практически не диссоциирует на ионы. То же самое справедливо для газообразных участников реакции. 2) Если между реагентами и продуктами в уравнениях полуреакций происходит перераспределение кислорода, то для осуществления такого перераспределения используется: – в кислой среде пара H+ – H2O; – в нейтральной среде пары H2O – H+ , H2O – OH– ; – в щелочной среде пара OH– – H2O. При этом в случае нейтральной среды в левой части уравнений полуреакций всегда должна фигурировать вода. 3) В уравнениях полуреакций помимо баланса элементов должен соблюдаться зарядовый баланс, который устанавливается путем прибавления к левой части уравнения или вычитания из нее соответствующего количества электронов. 4) При переходе от ионно-молекулярной к молекулярной форме уравнения следует иметь в виду, что добавление в левую часть уравнения новых частиц (например, к дихромат-аниону Cr2O72– добавляют стехиометрическое количество противоионов К+ или Na+), эти частицы должны быть перенесены и в правую часть. Принципиальная возможность осуществления окислительно-восстановительных реакций в стандартных условиях выявляется на основе разности электродных потенциалов окислителя и восстановителя
связанной с изменением энергии Гиббса соотношением DG=–nF Из последнего выражения следует, что процесс принципиально осуществим при
Примеры решения типовых задач.
Пример 1. Составление уравнений окислительно-восстановительных реакций методом электронного баланса. Задача 1. Составьте уравнение окислительно-восстановительной реакции окисления дисульфида серы (II) кислородом. Решение. Продуктами этой реакции являются SO2 и Fe2O3. Соответственно степень окисления железа изменяется от +2 до +3, степень окисления серы – от –1 до +4, степень окисления кислорода – от 0 до –2. Можно видеть, что функцию восстановителя в этой реакции выполняют совместно Fe2+ и S22 -, функцию окислителя – О2. В этой связи представим реакции окисления и восстановления схемой:
4 FeS2 + 11О2 По числу принятых кислородом и отданных FeS2 электронов определяем коэффициенты перед окислителем и восстановителем. С учетом поэлементного баланса находим коэффициенты перед формулами продуктов реакции.
Пример 2. Составление уравнений окислительно-восстановительных реакций методом электронно-ионного баланса. Задача 1. Составьте уравнение окислительно-восстановительной реакции между перманганатом калия и сульфитом натрия в среде серной кислоты. Решение. KMnO4 и Na2SO3 – сильные электролиты, поэтому в растворе они практически полностью диссоциируют на ионы. Окисляющим началом является анион MnO4– , в котором марганец находится в степени окисления +7. В то же время у серы в сульфит-анионе имеется ресурс окисления до сульфат-аниона, поэтому он является восстановителем. Известно, что в кислой среде перманганат-анион восстанавливается до Mn2+. Поэтому уравнения полуреакций записываются в виде:
2MnO4 – + 16Н+ + 5SО32– +5Н2О
Можно видеть, как пара Н+ – Н2О осуществляет перераспределение кислорода между реагентами и продуктами реакции. Коэффициенты перед строками уравнений полуреакций отражают требования электронного баланса: количество электронов, принятых окислителем должно быть равно количеству электронов, отданных восстановителем. Суммирование левых и правых частей уравнений реакций с учетом умножения их на указанные коэффициенты дает уравнение окислительно-восстановительной реакции в ионно-молекулярной форме, приведенное под чертой. Сокращение подобных членов в этом уравнении приводит к более компактной его форме
Переход к молекулярной форме приводит к окончательному виду уравнения: Пример 3. Составление уравнений окислительно-восстановительных реакций, протекающих в нейтральной среде. Задача 1. Составьте уравнение окислительно-восстановительной реакции между сульфатом марганца(II) и перманганатом калия. Решение. Продуктомэтой реакции является MnO2, следовательно, в роли окислителя выступает анион
2MnO4 – + 10Н2О + 3Mn2+
Суммирование левых и правых частей уравнений полуреакций с учетом умножения их строк на приведенные коэффициенты дает ионно-молекулярное уравнение, представленное под чертой. С учетом того, что рекомбинация 8Н + и 8ОН – в правой части этого уравнения дает 8 молекул воды, сокращаем воду в левой и правой частях и получаем уравнение
2MnO4 – + 2Н2О + 3Mn2+ Переход к молекулярной форме приводит к окончательному виду уравнения:
Пример 4. Составление уравнений окислительно-восстановительных реакций с участием органических соединений. Задача 1. Составьте уравнение реакции окисления этилбензола перманганатом калия в нейтральной среде. Решение. Роль окислителя в этой реакции выполняет перманганат-анион, а восстановителя – этилбензол,
4MnO4 – + 12Н2О +
Сокращая воду в левой и правой частях полученного уравнения и учитывая взаимодействия
приходим к уравнению 4MnO4 – + Переходим к молекулярной форме уравнения: 4КМnO4 +
Пример 5. Определение окислительно-восстановительных молярных масс эквивалентов. Задача 1. Чему равен эквивалент окислителя в реакции Решение. Молярная масса эквивалента окислителя (восстановителя) равна его молярной массе, деленной на число принятых (или отданных) электронов. В приведенной реакции окислителем является Следовательно, молярная масса эквивалента окислителя равна
Пример 6. Определение направления окислительно-восстановительной реакции по величине окислительно-восстановительных потенциалов (Red-Ox-потенциалов). Задача 1. Возможно ли в качестве окислителя в кислой среде использовать а) б) в) г) Стандартный окислительно-восстановительный потенциал системы
Решение. Для определения направления окислительно-восстановительной реакции необходимо определить ЭДС (
где Реакция возможна, если Для выяснения возможности протекания окислительно-восстановительных реакций определяем ЭДС следующих систем: а)
б)
в)
г)
Таким образом, дихромат калия
Пример 7. Определение возможности протекания окислительно-восстановительной реакции по величине изменения энергии Гиббса (изобарно-изотермического потенциала). Задача 1.Определите возможность протекания окислительно-восстановительной реакции
если стандартные значения энергии Гиббса равны:
Решение. Определяем
=2(-79,91) + 86,69 – 3(51,84) – (-237,5)=8, 65кДж. Так как
1.8. ЭЛЕКТРОХИМИЧЕСКИЕ ПРОЦЕССЫ
Электрохимическими процессами называют процессы взаимного превращения химической и электрической форм энергии. Электрохимические процессы можно разделить на две основные группы: 1)процессы превращения химической энергии в электрическую (в гальванических элементах); 2) процессы превращения электрической энергии в химическую (электролиз). Простейшая электрохимическая система состоит из двух электродов, соединенных друг с другом металлическим проводником (внешней цепи) и ионного проводника между ними (растворы или расплавы электролитов).
1.8.1. Гальванические элементы При окислительно-восстановительных реакциях происходит переход электронов от восстановителя к окислителю. Эту реакцию можно проводить таким образом, чтобы процессы окисления и восстановления были пространственно разделены, а электроны перемещались от восстановителя к окислителю по внешней цепи. Устройства, при помощи которых химическая энергия превращается в электрическую, называются гальваническими элементами, или химическими источниками электрической энергии. Одним из первых гальванических элементов был сконструирован гальванический элемент Якоби-Даниэльса. Это устройство состоит из двух электродов - металлических пластин (цинковой и медной), помещённых в раствор электролитов (солей цинка и меди), разделенных пористой перегородкой, и соединённых проводником. Электрод, на котором протекает процесс окисления, называется анодом. Электрод, на котором протекает процесс восстановления, называется катодом.
Используют специальную форму записи гальванического элемента, в которой указывают анод, поверхность раздела, первый электролит, электролитический ключ, второй электролит, катод и направление движения электронов во внешней цепи:
анод катод
Т.о., цинковая пластина начинает растворяться, а на медной пластине начинает осаждаться медь, пока равновесие не восстановится. Электрический ток, протекающий по внешней цепи, может совершать полезную работу, которая равна произведению количества прошедшего электричества на напряжение: Amax = nF∆E, где: n – число электронов, участвующих в окислительно-восстановительном процессе; F – число Фарадея (F = 96500 Кл/моль); DE – электродвижущая сила гальванического элемента (ЭДС). В то же время максимальная полезная работа равна изменению свободной энергии Гиббса реакции: Amax = - ∆G. Работа гальванического элемента процесс самопроизвольный (∆G<0). ∆G = - nF∆E ЭДС гальванического элемента – это максимальное значение напряжения гальванического элемента.
где:
Электродные потенциалы возникают на границе раздела фаз металл – электролит. При погружении металла в раствор, содержащий одноименный ион, начинается сложное взаимодействие металла с компонентами раствора, в результате чего происходит окисление металла, и его гидратированные ионы переходят в раствор, оставляя в металле электроны, заряд которых не скомпенсирован положительно заряженными ионами в металле: М + m H2O
Металл становится заряженным отрицательно, а раствор – положительно. Положительно заряженные ионы из раствора притягиваются к отрицательно заряженной поверхности металла, в результате чего на границе металл–раствор возникает двойной электрический слой (рис.1). Между металлом и раствором возникает разность потенциалов, которая называется электродным потенциалом. Наряду с окислением металла протекает обратная реакция – восстановления ионов металла до атомов. При некотором значении электродного потенциала, который называется равновесным электродным потенциалом, устанавливается равновесие М + m H2O или без учета гидратационной воды: М
|
|||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-15; просмотров: 312; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.64.210 (0.013 с.) |

 (1)
(1) (2)
(2) 2 О2-
2 О2-

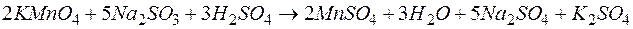 .
. , а восстановителя –
, а восстановителя –  . Составляем уравнение полуреакции, учитывая, что в левой части этих уравнений в качестве перераспределителя кислорода выступает вода.
. Составляем уравнение полуреакции, учитывая, что в левой части этих уравнений в качестве перераспределителя кислорода выступает вода. .
. . В нейтральной среде перманганат-анион переходит в
. В нейтральной среде перманганат-анион переходит в  , а этилбензол деструктивно окисляется до бензойной кислоты и углекислого газа. В этой связи уравнение полуреакций записывается в виде
, а этилбензол деструктивно окисляется до бензойной кислоты и углекислого газа. В этой связи уравнение полуреакций записывается в виде +
+ 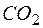 + 12Н+
+ 12Н+

 + ОН –
+ ОН – 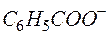 + Н2О
+ Н2О  + Н2О,
+ Н2О,  +
+  +
+  +2Н2О+ + КОН.
+2Н2О+ + КОН. ?
? (Мr=158, М=158г/моль), а процесс восстановления идет по схеме
(Мr=158, М=158г/моль), а процесс восстановления идет по схеме  .
. (г/моль).
(г/моль). в следующих процессах при стандартных условиях:
в следующих процессах при стандартных условиях: ;
; ;
;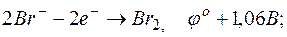
 .
. .
. E,
E,  ):
): ,
, – потенциал окислителя;
– потенциал окислителя;  – потенциал восстановителя.
– потенциал восстановителя.


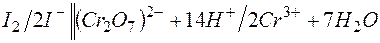

 .
. ,
, ;
;  ;
; ;
;  .
. процесса
процесса +
+  – 3
– 3  –
–  =
= окисление
окисление восстановление
восстановление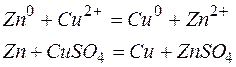




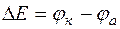 ,
, - электродный потенциал катода;
- электродный потенциал катода; - электродный потенциал анода.
- электродный потенциал анода. M(H2O)mn+ + ne
M(H2O)mn+ + ne M(H2O)mn+ + ne
M(H2O)mn+ + ne


