

Мы поможем в написании ваших работ!
ЗНАЕТЕ ЛИ ВЫ?
|
Ядра состоят из нуклонов (протоны и нейтроны) и других частиц.
Содержание книги
- Опасные и вредные факторы для человека, экономики и природной среды в Беларуси.
- Системный анализ проблем безопасности. Уровни безопасности. Принципы, методы, способы и средства обеспечения безопасности. Понятие комплексной безопасности.
- Физиологические и психологические возможности выживания в чрезвычайных ситуациях
- Философия и психология выживания
- Лекция 2. ЧС и их Классификация. Природные и биолого-социальные чрезвычайные ситуации
- Чрезвычайные ситуации, вызванные опасными метеорологическими процессами и явлениями
- Грозы, молнии и другие опасные атмосферные явления
- Чрезвычайные ситуации, вызванные опасными гидрологическими явлениями и процессами
- Чрезвычайные ситуации, вызванные опасными геологическими процессами и явлениями
- Чрезвычайные ситуации, вызванные опасными космическими явлениями и процессами
- При желудочно-кишечных поражениях названия доз аналогичны и измеряются в кг/см , кг/м ,мг/кг.
- Последствия отравления химически опасными веществами.
- Ядерное оружие и его характеристики. Поражающие факторы ядерного взрыва. Возможные последствия ядерной войны.
- Краткая характеристика поражающих факторов ядерного взрыва
- Химическое оружие и возможные последствия его применения
- Биологическое оружие и возможные последствия его применения
- Государственная система предупреждения и ликвидации ЧС(ГСЧС)
- Организация гражданской обороны объекта
- Прогнозирование некоторых природных процессов и
- Предупреждение ЧС, вызванных террористическими действиями. Меры безопасности при проведении массовых общественных мероприятий.
- Безопасность транспортных средств
- Основными мероприятиями по защите населения в ЧС являются
- Лекция 9. Ликвидация чрезвычайных ситуаций и их последствий силами гсчс и ГО.
- Правила поведения и способы выживания людей при авариях и катастрофах на транспорте
- Правила поведения людей при инфекционных заболеваниях. Рассмотрим особенности поведения человека при возникновении некоторых наиболее опасных инфекционных болезней.
- Псевдочума птиц – инфекционное заболевание семейства куриных.
- Особенности защиты населения и объектов в условиях чрезвычайного положения. Правила поведения граждан.
- Лекция 11. Обеспечение пожарной безопасности на объектах производственного и социального назначения.
- Системы обеспечения пожарной безопасности и организационно-технические мероприятия по обеспечению пожарной безопасности
- Технические средства противоаварийной защиты
- Надзор и контроль в области обеспечения пожарной безопасности
- Форма информационной карточки
- Лекция1. Физическая природа ионизирующих излучений
- Ядра состоят из нуклонов (протоны и нейтроны) и других частиц.
- Взаимодействие радиоактивных излучений с веществом
- Базовые, нормируемые и рабочие величины в радиационной безопасности
- Экспозиционная доза – это величина отношения суммарного заряда всех ионов одного знака, которые образуются рентгеновским или гамма – излучением в некотором объёме, к массе воздуха в этом объёме.
- Источники ионизирующего излучения
- Методы и приборы для обнаружения и измерения характеристик ионизирующих излучений
- Тема 2. Основы радиационной безопасности живых организмов
- Реакции органов и систем человека на облучение
- Действие больших доз радиации на организм человека. Детерминированные эффекты. Лучевая болезнь
- Принципы радиационной безопасности
- Основные нормативно – правовые акты, отражающие радиационную безопасность Республики Беларусь
- Нормирование облучения для практической деятельности человека
- Постоянный мониторинг радиационно – гигиенической и радиоэкологической обстановки
- Ее последствия для Республики Беларусь
- Лекция 7. Мероприятия по противорадиационной защите
- Способы защиты от ии делят на физические и химические, защиту от внешнего облучения и защиту от внутреннего облучения.
- Употребление продуктов, слабо аккумулирующих радионуклиды
Нуклоны (от лат. nucleus – ядро) – общее наименование для протонов и нейтронов, из которых построены все атомные ядра.
Нуклиды, общее название атомных ядер, отличающихся числом протонов, нейтронов. Условно каждый химический элемент (нуклид) записывается как  , где М – массовое число, Z – заряд ядра или порядковый номер элемента. , где М – массовое число, Z – заряд ядра или порядковый номер элемента.
Нуклиды с одинаковым числом в ядре химического, элемента протонов и разным количеством нейтронов называются изотопами.
Термин изотопы следует применять только в тех случаях, когда речь идет об атомах одного и того же элемента. Например, изотопы урана  , ,  , ,  , изотопы углерода , изотопы углерода  и и  . Когда речь идет об атомах различных элементов (включая изотопы), рекомендуется использовать термин нуклиды. . Когда речь идет об атомах различных элементов (включая изотопы), рекомендуется использовать термин нуклиды.
НУКЛИДЫ – разновидности атомов с данным массовым числом и атомным номером. Например, смесь нуклидов  , ,  , ,  , , 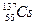 , ,  , ,  . .
• Протон (от греч. protos – ядро) – относительно стабильная элементарная частица с положительным зарядом, равным заряду позитрона и массой ~ 1836 mе (m – масса электрона). Вместе с нейтронами протоны образуют атомные ядра всех химических элементов, при этом число протонов в ядре равно атомному номеру данного элемента и, следовательно, определяет место элемента в периодической системе Д.И. Менделеева. Среднее значение жизни протона более 1030 лет.
• Позитрон – элементарная частица, которая по массе равна массе электрона, но имеет положительный заряд, равный по величине отрицательному заряду электрона.
• Нейтрон – электрически нейтральная элементарная частица с массой ~ 1840 mе, незначительно превышающей массу протона. Среднее время жизни нейтрона в свободном состоянии (вне ядра) ~ 15,3 мин. При слабом взаимодействии в ядре нейтрон может превратиться в протон через бета – распад с выбросом электрона (условно заряд равен минус единице) и антинейтрино.
Если просуммировать массы протонов и нейтронов в атомном ядре (масса протона 1,007277 АЕМ, нейтрона – 1,086652 АЕМ), то обнаружится, что эта сумма больше массы ядра, в состав которого они входят. Данное явление получило название ДЕФЕКТА МАССЫ ∆М. Дефект массы всех известных ядер – положительная величина. Дефект массы, переведенный в эквивалентную энергию, согласно знаменитому уравнению Эйнштейна Е = ∆М*С2, где С – скорость света, дает значение энергии, выделяемой при синтезе ядра данного нуклида из протонов и нейтронов. Такую же энергию необходимо затратить при расщеплении ядра на составляющие его нуклоны. Это определяет понятие энергии связи ядра.
ЭНЕРГИЯ СВЯЗИ (Ес) – это та энергия, которую необходимо затратить, чтобы разделить ядро на его составляющие нуклоны или та энергия, которая выделится при объединении протонов и нейтронов в ядро.
Энергия связи измеряется в электрон – вольтах (эВ). Один ЭЛЕКТРОН – ВОЛЬТ – это энергия, которую приобретает электрон, проходя разность потенциалов в один вольт. Так, например, электроны в кинескопе телевизора за счет напряжения по трубке 16000 вольт разгоняются, соответственно, до энергии в 16 кило – электрон – вольт (кэВ) или 0,016 мега – электрон – вольт (МэВ). Один электрон – вольт равен 1,6·10 – 19 джоулей.
Если дефект массы ∆М выражен в атомных единицах массы, то Ес = 931*∆М МэВ.
Величина энергии связи ядра зависит от его массового числа М и меняется от 2,224 миллиона электрон – вольт (МэВ) для дейтерия до сотен МэВ для тяжелых элементов таблицы Менделеева. Сами по себе значения Ес сравнительно невелики, но соотнесем их с энергией химических превращений. При сгорании килограмма самого высококалорийного топлива – водорода, выделяется 1,2·108 джоулей, что в переводе на один атом вещества составит всего лишь 12 эВ. Из сравнения рассмотренных величин видно, что ЯДЕРНЫЕ СИЛЫ, проявлением которых и является энергия связи, имеют иную природу, нежели силы, определяющие химическое взаимодействие атомов. Ядерные силы в миллионы раз превышают силы химического взаимодействия атомов в молекуле, действуют на коротком расстоянии, не зависят от электрического заряда и определяют взаимодействие между нуклонами в ядре атома. Эти силы являются силами притяжения, компенсируют кулоновское отталкивание протонов в ядре и определяют стабильность или НЕСТАБИЛЬНОСТЬ ЯДЕР.
|