Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Ферменти біологічного окислення, особливості протікання реакцій за їх участю: над(ф)-залежні дегідрогенази;флавін залежні дегідрогенази; koq; цитохроми.Содержание книги
Поиск на нашем сайте
Коферментами НАД(Ф)-залежних дегідрогеназ є нуклеотиди НАД+ або НАДФ+, у структурі молекул яких міститься нікотинамід.У ході ферментативної реакції субстрат відщеплює два атоми водню, один з яких у формі гідрид-іону приєднується до піридинового кільця, а другий у вигляді протону надходить у реакційне середовище:
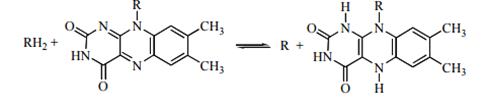
Під час реакції до четвертого вуглецевого атома нікотинаміду приєднується атом водню, а додатковий електрон гідрид-іону взаємодіє з азотом піридинового кільця. Флавінзалежні дегідрогенази. Дегідрогенази цього типу за хімічною природою є флавопротеїнами, просте- тичними групами в яких є ФАД та ФМН.Активною частиною молекули ФАД або ФМН, що бере участь в окислювально-відновлювальній реакції, є ізоалоксазинове кільце рибофлавіну, яке акцептує два атоми водню від субстрату:
Цитохроми — залізовмісні білки мітохондрій, що належать до класу гемо- протеїнів. У цитохромах іон заліза входить до складу металопорфіринового комплексу.Цитохроми виконуютьфункцію транспорту електронів у ланцюгах біологічного окислення в аеробних клітинах: Цитохром (Fe3+) + e– -------> Цитохром (Fe2+) Залежно від характерних особливостей спектрів поглинання, розрізняють три класи цитохромів (a, b, c) Коензим Q (убіхінон) — ліпідорозчинний хінон з ізопреноїдним бічним ланцюгом, що містить у тканинах ссавців десять п’ятивуглецевих ізопреноїдних залишків (Q10). Убіхінон виконує функцію колектора відновлювальних еквівалентів, акцептуючи протони та електрони не тільки від ФМН-залежної НАДН-дегідрогенази, а й від ФАД-залежних дегідрогеназ мітохондрій. Білет 6 1. Властивості ферментів: залежність активності ферментів від рH середовища, залежність активності ферментів від температури. Ферменти значно підвищують швидкість перебігу біохімічних реакцій, але не входять до складу кінцевих продуктів реакції; ферменти забезпечують перебіг лише тих біохімічних реакцій, які можливі згідно з законами термодинаміки; ферменти прискорюють швидкість як прямої, так і зворотної реакції перетворення субстрату, не змінюючи константи рівноваги (Кр) реакції та зменшуючи термін часу до досягнення стану рівноваги (або стаціонарного стану у відкритій метаболічній системі); протягом реакції фермент певним чином взаємодіє із субстратом, що перетворюється, але до складу кінцевих продуктів реакції не входить. Під час перебігу біохімічної реакції, що каталізується, відбувається циклічний процес, в ході якого фермент та субстрат підлягають ступінчастому перетворенню з утворенням продукту реакції та регенерацією ферменту; ферменти є високоспецифічними каталізаторами, тобто діють, як правило, на структурно близькі субстрати, що мають певний хімічний зв’язок, структурно подібні радикали або функціональні групи. Проявом високої специфічності ферментів є їх стереоспецифічність, тобто здатність перетворювати тільки певні стереоізомери, наприклад L- або L- амінокислоти, D- або L-моносахариди; відповідно до білкової природи, каталітична активність ферментів дуже чутлива до змін фізико- хімічних властивостей середовища (рН, температури), які можуть впливати на структурну організацію молекул ферментів, спричиняючи в певних умовах їх денатурацію; активність ферментів може суттєво змінюватися під впливом певних хімічних сполук, що збільшують (активатори) або зменшують (інгібітори) швидкість реакції, яка каталізується. Вплив температури на активність ферментів Ферменти, відповідно до своєї білкової природи, є термочутливими та термола- більними утвореннями: – зростання температури до оптимальних значень (для більшості ферментів — у межах 37-40 °C) cупроводжується збільшенням швид- кості ферментативної реакції відповідно за рів- нянням Арреніуса (за рахунок частіших ефек- тивних зіткнень між молекулами); cтупінь збільшення швидкості реакції при зростанні t° на 10 °C позначають, як температурний коефіцієнт Q10; – при збільшенні температури вище опти- мального значення швидкість ферментативної реакції різко зменшується за рахунок конфор- маційних (денатураційних) змін у структурі ферментного білка. Вплив рН на активність ферментів Кожен фермент має свій рН-оптимум, тобто значення рН середовища, при якому його каталітична активністьмаксимальна. “Дзвоно- подібна” залежність активностейферментів від змін рН визначається їх білковою природою, зсувами в дисоціації іоногенних груп та (при екcтремальних значеннях рН) розвитком кон- формаційних змінмолекул. Більшість внутрішньоклітинних та тканин- нихферментів організму людини найактивніші в нейтральному, слаболужному або слабокис- лому середовищі (звичайно, вмежах рНміж 5,0 та 9,0). Ферментами з оптимумами при екстре- мальних значеннях рН є пепсин (рНопт = 1-2) і аргіназа (рНопт = 10-11). Коферменти та кофактори Кофактори та коферменти Кофактори. Багато ферментів потребують для реалізації своєї каталітичної активності наявності певних низькомолекулярних небілкових сполук кофакторів. Роль кофакторів можуть відігравати біоорганічні сполуки різної хімічної природи або іони металів (Mg2+, Ca2+, Fe3+, Fe2+, Cu2+, Cuj+ та ін.). Іони металів зв'язані з апоферментом або входять до складу небілкової простетичної групи - найчастіше порфіринового кільця гемінових ферментів (цитохромів, пероксидаз, каталази). Ферменти, які міцно зв'язані з іонами металів і не втрачають цього зв'язку за умов виділення та фракціонування ферменту, назваються металоферментами. У деяких випадках іони металів не входять до складу ферментів як інтегральні структурні компоненти, а виконують лише функцію їх активаторів. Коферменти (коензими) — біоорганічні сполуки небілкової природи, що є необхідними для дії ферменту, тобто перетворення субстрату в каталітичному акті. Коферменти можуть сполучатися з білковою частиною (апоферментом) нековалентними фізико-хімічними або ковалентними зв'язками (в останньому випадку вони є простетичними групами ферментного білка - флавінові коферменти, піридоксаль-фосфат, ліпоєва кислота тощо); інколи коферменти утворюють комплекси з апоферментом лише в ході каталітичного процесу (НАД, НАДФ). За хімічною природою коферменти підрозділяють на: - похідні вітамінів, зокрема: вітаміну В, - тіаміндифосфат; вітаміну В2 - флавінмононуклеотид (ФМН); вітаміну В6 - піридоксальфосфат, піридоксамінфосфат; пантотенової кислоти - коензим А; вітаміну В12 - метилкобаламін, дезоксиаденозилкобаламін; вітаміну Н (біотину) - карбоксибіотин; фолієвої кислоти - тетрагідрофолієва кислота; - динуклеотиди (похідні нікотинаміду - НАД, НАДФ; похідна рибофлавіну - ФАД); - нуклеотиди - похідні пуринів та піримідинів (АТФ, АДФ, ЦТФ, ЦДФ, УТФ, УДФ); - комплекси порфіринів з іонами металів.
|
||||
|
Последнее изменение этой страницы: 2016-12-12; просмотров: 389; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.119.135.67 (0.009 с.) |