
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Расчет рН в растворах сильных и слабых основанийСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
1. Диссоциация сильного основания (LiOH, NaOH, KOH, RbOH, CsOH, FrOH, Ca(OH)2, Sr(OH)2, Ba(OH)2) протекает практически полностью: NaOH Можно считать, что [ОH-] = Сщел, где Сщел - молярная концентрация сильного основания (щелочи). Расчет рН раствора сильного основания проводят по схеме: рОН = - lg а ОН- = - lg f ОН-[ОH-]; рН = 14 – рОН. 2. Диссоциация слабого основания протекает незначительно, частично: NH3∙H2O Молярную концентрацию гидроксид – ионов [ОH-] в растворе слабого основания рассчитывают по закону разведения Оствальда:
молярная концентрация основания, Косн – константа диссоциации основания, характеризует силу основания: чем меньше константа диссоциации, тем слабее основание. Лекция 13. Произведение растворимости. Ионно-обменные реакции
Насыщенный раствор находится в равновесии с твердой фазой растворяемого вещества. Гетерогенное равновесие «осадок то выражение для константы равновесия – произведения растворимости (
Следовательно, для насыщенного водного раствора малорастворимого электролита произведение равновесных молярных концентраций его ионов в степенях, равных стехиометрическим коэффициентам, есть величина постоянная при данной температуре, и называемая произведением растворимости. Зная произведение растворимости (ПР), можно вычислить растворимость вещества (S) при данных условиях, т.е. концентрацию насыщенного раствора в [моль/л] и в [г/л]. Например, для бинарных электролитов (ВaSO4, СaСO3, AgI и др.) растворимость [моль/л] численно равна: В ненасыщенном растворе возможно растворение дополнительного количества вещества, так как концентрация меньше, чем в насыщенном. Из перенасыщенного раствора осадок образуется, так как его концентрация больше, чем в насыщенном. Отсюда вытекают условия образования и растворения осадка: 1) если [An+]m·[Bm-]n = ПРAmBn, то осадок находится в равновесии с раствором (насыщенный раствор); 2) если [An+]m·[Bm-]n > ПРAmBn, то осадок выпадает (перенасыщенный раствор); 3) если [An+]m·[Bm-]n < ПРAmBn, то осадок растворяется (ненасыщенный раствор). Важным следствием является правило, используемое для более полного удаления из раствора какого-либо иона: растворимость малорастворимого электролита уменьшается при введении хорошо растворимого электролита, имеющего одноименный (общий) ион с малорастворимым электролитом. В водных растворах электролитов химические реакции протекают с участием ионов, такие реакции называются ионно-обменными, а уравнения этих реакций – ионными уравнениями. В ионных уравнениях реакций формулы сильных электролитов записываются в виде ионов, формулы слабых электролитов, осадков и газов – в виде молекул. Направление ионно-обменной реакции между двумя электролитами в растворе определяется возможностью образования их ионами осадка, газа или слабого электролита. 1. Образование малорастворимого соединения, выпадающего в виде осадка: AgNO3 + NaCl = AgCl↓ + NaNO3 (молекулярное уравнение) Ag+ + NO3 – + Na+ + Cl – = AgCl↓ + Na+ + NO3 – (полное ионное уравнение) Ag+ + Cl – = AgCl↓ (сокращенное ионное уравнение). 2. Образование газообразного вещества, удаляемого из раствора: Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2↑ 2Na+ + CO32 – + 2H+ + SO42 – = 2Na+ + SO42 – + H2O + CO2↑ CO32 – + 2H+ = H2O + CO2↑ 3. Образование растворимого, но мало диссоциированного вещества, например, воды, слабой кислоты или слабого основания: CH3COONa + H2SO4 = Na2SO4 + CH3COOH CH3COO –+ Na+ = 2Na+ +SO42 –+ CH3COOH CH3COO – + H+ = CH3COOH; 4. Образование устойчивой комплексной частицы – молекулы или иона: HgI2 + 2KI = K2[HgI4] Hg2+ + 2I – + 2K+ + 2I – = 2K+ + [HgI4]2 – Hg2+ + 4I – = [HgI4]2 – Реакциями нейтрализации называются обменные реакции взаимодействия кислот и оснований, в результате которых образуются соль и вода, например: NaOH + HCl = NaCl + H2O или OH – + H+ = H2O. При нейтрализации сильного основания сильной кислотой равновесие практически полностью смещено в сторону образования воды. Реакции нейтрализации при взаимодействии кислот и оснований, различающихся по силе, не доходят до конца вследствие протекания обратной реакции гидролиза соли, например: СН3СООН + NaOH СН3СООН + ОН- Реакции нейтрализации экзотермические и протекают с выделением тепла. Лекция 14. Гидролиз солей. Буферные растворы
Гидролиз солей -это ионно-обменное взаимодействие соли с водой. Реакция протекает, если в продуктах образуется слабая кислота и/или слабое основание. Она основана на поляризующем действии ионов соли на молекулы воды, в результате которого нарушается равновесие диссоциации воды: Н2О Соли, образованные сильными основаниями и сильными кислотами (NаСl, КNO3, Rb2SO4), не содержат ионов, способных к взаимодействию с водой, поэтому гидролизу не подвергаются. Реакция среды в растворе таких солей нейтральная (рH=7). Гидролиз по катиону характеризует соли, образованные сильной кислотой и слабым основанием (NH4Cl, ZnSO4, Al(NO3)3). В результате катион соли связывает ионы ОН- из воды. В растворе увеличивается концентрация ионов Н+ и реакция среды становится кислой (рH<7).Например: NH4+ + HOH NH4Cl + HOH Количественно гидролиз характеризуется константой гидролиза (Кг) и степенью гидролиза (h). Константа гидролиза соли сильной кислоты и слабого основания рассчитывается по формуле Кг = [ Кв ∕ Косн], где Кв – ионное произведение воды, Косн – константа диссоциации слабого основания. Расчет рН в растворе соли слабого основания и сильной кислоты осуществляют по формуле рН = 7 + ½ lgKосн - ½ lgСсоли, где Ссоли – молярная концентрация соли. Гидролиз по аниону характеризует соли, образованные слабой кислотой и сильным основанием (NаF, Na2CO3, Rb3PO4). Анион соли связывает катион Н+ воды и в растворе накапливаются ионы ОН-, среда щелочная (рH > 7). F- + H2O NaF + HOH Константа гидролиза соли сильного основания и слабой кислоты рассчитывается по формуле Кг=[ Кв ∕ Ккисл], где Ккисл – константа диссоциации слабой кислоты. Расчет рН в растворе соли сильного основания и слабой кислоты осуществляют по формуле рН = 7 - ½ lgKкисл + ½ lgСсоли. Гидролиз по катиону и аниону протекает в растворах солей, образованных слабой кислотой и слабым основанием (NH4CN, NH4СH3COO). Реакция среды в растворах таких солей близка к нейтральной. Может быть слабокислой или слабощелочной и определяется способностью к диссоциации продуктов гидролиза: слабой кислоты и слабого основания. NH4F + HOH Константа гидролиза соли слабого однокислотного основания и слабой одноосновной кислоты: Кг = [ Кв /(Ккисл∙Косн)]. Расчет рН в растворе соли слабого основания и слабой кислоты: рН=7 - ½ lgKкисл + ½ lgКосн. Соли, образованные слабым основанием и слабой кислотой (Al2S3, Cr2S3, Al2(СО3)3), могут подвергаться необратимому разложению водой, если в продуктах образуются осадки или выделяется газ. Водные растворы таких солей не существуют. Например: Al2S3 + 6 HOH Степень гидролиза соли (h) - это отношение количества вещества соли, подвергшегося гидролизу, к общему количеству вещества соли. Константа гидролиза (Кг) и степень гидролиза (h) связаны соотношением Кг=Ссоли.h2/(1-h), где Ссоли - молярная концентрация соли в растворе. Если h<<1, то Кг = Ссоли.h2; Степень гидролиза соли определяется следующими факторами: 1. Так как гидролиз - процесс эндотермический, то повышение температуры усиливает гидролиз. 2. Чем слабее кислота и/или основание, образующиеся при гидролизе, тем выше степень гидролиза их солей. 3. Чем меньше молярная концентрация соли, тем степень гидролиза выше, т.е. с разбавлением гидролиз усиливается. 4. По принципу Ле-Шателье, добавление продуктов гидролиза его подавляет. Буферный раствор - это раствор, содержащий равновесную систему, способную поддерживать практически постоянное значение рН при разбавлении или при добавлении небольших количеств кислоты или щелочи. Буферные растворы обладают амфотерными свойствами, взаимодействуют с сильными кислотами и основаниями. Их характеризуют рабочей областью рH и буферной емкостью. Лекция 15. Окислительно-восстановительные реакции
Окислительно-восстановительными реакциями (ОВР) называют реакции, протекающие с изменением степеней окисления участвующих в них элементов. Степень окисления элемента – формальный заряд, который был бы на атоме, если бы все связи в соединении были ионными. Характерные степени окисления элемента определяются конфигурацией валентного электронного слоя. Окислитель – акцептор электронов, то есть «принимает электроны» и восстанавливается. Восстановитель является донором электронов, то есть «отдает электроны» и окисляется. В окислительно-восстановительных реакциях восстановитель переходит в соответствующую окисленную форму, и наоборот, окислитель – в соответствующую восстановленную форму. Каждый из реагентов со своим продуктом образует сопряженную окислительно-восстановительную пару. Окисление – процесс, в котором степень окисления элемента повышается вследствие отдачи электронов. Восстановление – процесс, в котором степень окисления элемента понижается вследствие присоединения электронов. Процессы окисления и восстановления протекают одновременно. Окислительно-восстановительные реакции подразделяют на межмолекулярные, внутримолекулярные, диспропорционирования (или самоокисления-самовосстановления), конпропорционирования. В уравнениях окислительно-восстановительных реакций должен быть отражен «электронный» и «материальный» баланс. Электронный баланс: число электронов, «отданных» восстановителем, должно быть равно числу электронов, «принятых» окислителем. Материальный баланс: число атомов одного элемента в левой и правой части уравнения должно быть одинаковым. Метод электронного баланса применяют для составления уравнений реакций ОВР любого типа. Он включает определение степеней окисления элементов, наименьшего общего кратного числа «отданных» восстановителем и «принятых» окислителем электронов, определение коэффициентов электронного баланса: K2Cr2O7 + 6KI + 7H2SO4 → Cr2(SO4)3 + 3I2 + 4K2SO4 + 7H2O Сr+6 + 3e → Cr+3 1 I– – 1e → Io 3 Метод ионно-электронного баланса применяют для составления уравнений ОВР, протекающих в водных растворах с учетом диссоциации сильных хорошо растворимых электролитов на ионы. Он включает составление полуреакций окисления и восстановления. Причем материальный баланс подбирается с использованием частиц H2O и H+ - для реакций в кислой среде и частиц H2O и OH– - для реакций в щелочной среде. MnO4– + 8H+ + 5e → Mn2+ + 4H2O 2 (процесс восстановления) SO32– + H2O – 2e → SO42– + 2H+ 5 (процесс окисления) Далее определяют заряд каждой из систем до и после превращения; рассчитывают число «отданных» восстановителем и «принятых» окислителем электронов и определяют коэффициенты электронного баланса; проводят сложение полуреакций окисления и восстановления, умноженных на соответствующие коэффициенты электронного баланса и «приведение подобных членов». В итоге получают краткое ионное уравнение: 2MnO4– + 6H+ + 5SO32– →2Mn2+ + 5SO42– + 3H2O (краткое ионное уравнение) Коэффициенты, полученные в кратком ионном уравнении, переносятся в молекулярное уравнение (с учетом состава соединений): 2KMnO4 + 3H2SO4 + 5Na2SO3 → 2MnSO4 + 5Na2SO4 + 3H2O + K2SO4 Определяют коэффициенты перед элементами, не участвовавшими в ОВР (например, К). Свойства сопряженной окислительно-восстановительной пары характеризует окислительно-восстановительный потенциал(φок./вос., В). Окислительно-восстановительная реакция протекает самопроизвольно, если изменение свободной энергии Гиббса (∆G) отрицательно: ∆G < 0. Для окислительно-восстановительных реакций, протекающих в водной среде, изменение свободной энергии Гиббса связано со значениями окислительно-восстановительных потенциалов соотношением ∆ G = -nF (φок - φвос) < 0, где n - число электронов, F - постоянная Фарадея [Кул/моль], φок и φвос – окислительно-восстановительные потенциалы (В) системы окислителя и восстановителя соответственно. Разность окислительно-восстановительных потенциалов окислителя и восстановителяназывают электродвижущей силой реакции (ЭДС) и измеряют в вольтах (В). Таким образом, ОВР между данным окислителем и данным восстановителем протекает самопроизвольно в прямом направлении, если ЭДС положительна: ЭДС = [φок – φвос ] > 0 или φок > φвос. Лекция 16. Понятие «Электродный потенциал». Электрохимические процессы
Если металлическую пластинку (электрод) опустить в воду, то катионы металла на ее поверхности гидратируются молекулами воды и переходят в жидкость. При этом электроны, остающиеся в металле, заряжают его поверхность отрицательно. В итоге установится равновесие между катионами и поверхностью металла: Ме0 – n ē + m H2O где n — число отдаваемых электронов. На границе «металл – жидкость» возникает двойной электрический слой, характеризующийся определенным скачком потенциала – электродным потенциалом. Каждый металл обладает при равновесии определенным электродным потенциалом. При погружении металлов в раствор их солей знак заряда металлической пластинки зависит от природы металла. Если металл является активным (например, Zn в растворе ZnSO4), то равновесие обратимой реакции смещено в прямом направлении, т.е. в сторону окисления. Возникающий электродный потенциал имеет знак «минус». Для малоактивного металла (например, Cu в растворе CuSO4) равновесие реакции смещено в обратном направлении, т.е. в сторону восстановления. Возникающий потенциал имеет знак «плюс». Если удалять из металла избыточные электроны, то равновесие (1) будет смещено вправо. Такие условия создаются в гальванических элементах. Гальванический элемент (ГЭ) - это прибор, в котором химическая энергия окислительно-восстановительной реакции превращается в электрическую. Возьмем два сосуда. В один из них, содержащий раствор ZnSO4, опустим цинковый электрод, в другой, содержащий раствор CuSO4, - медный электрод. Состояние равновесия для обоих электродов выражается уравнениями: Zn Cu Способность отдавать ионы в раствор у Zn больше, чем у Cu, поэтому концентрация электронов на цинковом электроде больше. Если соединить электроды внешним проводником, а растворы солей электролитическим мостиком, то электроны с цинка будут переходить на медь. Этот переход нарушит равновесие (2) и (3). Происходящие процессы выражаются уравнениями: Zn0 – 2 ē → Zn2+ - процесс окисления (протекает на аноде); Cu2+ + 2 ē → Cu0 - процесс восстановления (протекает на катоде). Анодом является металл с более низким значением электродного потенциала. Суммарно: Zn0 + Cu2+ → Zn2+ + Cu0. Электродвижущая сила (ЭДС) ГЭ равна разности электродных потенциалов между катодом и анодом. Электрохимическая цепь для медно-цинкового элемента имеет вид: (–) Zn│Zn2+║Cu2+│Cu (+) анод катод Так как методов прямого измерения электродных потенциалов не существует, то возможно только измерение ЭДС ГЭ и вычисление неизвестного потенциала по известному. Поэтому определяют относительные электродные потенциалы в определенных условиях – стандартные электродные потенциалы (φ0). За нулевой потенциал принят потенциал стандартного водородного электрода, представляющего собой платиновую пластину, опущенную в раствор с [H+] = 1 моль/л при T = 298 K (25 oC) и стандартном давлении H2 (P = 1,01·105 Па (1атм)). Процессы, происходящие на водородном и металлическом электродах описываются уравнениями: H+aq + ē Определяемая в вольтах разность потенциалов и есть относительный электродный потенциал металла. Стандартным электродным потенциалом металла называют его электродный потенциал, возникающий при погружении металла в раствор собственного иона с концентрацией 1 [моль/л] и при T = 298 K (t = 25 oC), измеренный по сравнению со стандартным водородным электродом. Располагая металлы в ряд по мере возрастания их стандартных электродныхпотенциалов (φoМеn+/Me), получаем так называемый ряд стандартных электродных потенциалов. Положение металла в ряду стандартных электродных потенциалов характеризует его восстановительную способность, а также окислительные свойства его ионов в водных растворах. Чем меньше значение φoМеn+/Me, тем больше восстановительная способность металла и тем меньше окислительная способность его ионов. Выводы по ряду стандартных электродных потенциалов: 1. Каждый металл способен вытеснить из растворов солей те металлы, которые стоят после него в ряду стандартных электродных потенциалов, т.е. имеют большую алгебраическую величину стандартного потенциала. 2. Водород может быть вытеснен из разбавленного раствора H2SO4 и HCl теми металлами, которые имеют стандартные потенциалы со знаком «минус». Лекция 17. Электролиз расплавов и растворов солей
Электролиз -окислительно-восстановительный процесс, протекающий на электродах при пропускании постоянного тока через систему, включающую электролит. Химические реакции, протекающие при электролизе, осуществляются при помощи энергии электрического тока, подведённого извне. Следовательно, при электролизе происходит преобразование электрической энергии в химическую. Процессы окисления и восстановления в этом случае протекают раздельно, т.е. на различных электродах. Электрод, на котором происходит восстановление, называется катодом, а электрод, на котором происходит окисление, - анодом. Катод подключён к отрицательному полюсу, и поэтому к нему движутся катионы, анод – к положительному полюсу, к нему движутся анионы. Минимальный потенциал (В), при котором процесс электролиза становится возможным, называется потенциалом (напряжением) разложения. Его находят вычитанием электродного потенциала катиона из соответствующего значения электродного потенциала аниона, единица измерения вольт (В). Электролиз расплава. Рассмотрим электролиз расплава СuCl2, который диссоциирует на ионы Сu2+ и Cl⁻. При подключении напряжения к электродам через расплав начинает протекать электрический ток. Так, при электролизе расплава хлорида меди (II) электродные процессы могут быть выражены полуреакциями: на катоде (–): Сu2+ + 2e → Cu0 – катодное восстановление на аноде (+): 2 Cl– – 2e → Cl2 – анодное окисление Общая реакция электрохимического разложения вещества представляет собой сумму двух электродных полуреакций, и для хлорида меди она выразится уравнением Cu2+ + 2 Cl– → Cu + Cl2 Электролиз растворов осложняется участием в электродных процессах ионов Н⁺ и ОН⁻. Кроме того, молекулы воды сами могут подвергаться электродному окислению или восстановлению. Катодные процессы в водных растворах при электролизе не зависят от материала катода, а только от природы катиона (табл. 1). Анодные процессы в водных растворах зависят от материала анода и природы аниона. При рассмотрении анодных процессов следует иметь в виду, что материал анода в ходе электролиза может окисляться. В связи с этим различают электролиз с инертным анодом и электролиз с активным анодом (растворимым). Инертным называется анод, материал которого не претерпевает окисления в ходе электролиза. Таблица 1 Процессы, происходящие на катоде
Активным называется анод, материал которого может окисляться в ходе электролиза. В качестве материалов для инертных анодов чаще применяют графит, уголь, платину; для активных – медь, цинк, алюминий и т.д. (табл. 2). Таблица 2 Процессы, происходящие на аноде
В случае электролиза растворов возможны конкурирующие реакции. Критерием, определяющим преимущество того или иного электродного процесса, служит величина его электродного потенциала. Чем выше потенциал, тем легче происходит восстановление на катоде и труднее осуществляется окисление на аноде.
Лекция 18. Общие свойства металлов
Из 110 известных к настоящему времени элементов только 22 относятся к неметаллам, большинство же элементов – металлы. К металлам относят все s-, d-, f-элементы, а также p-элементы, условно располагающиеся в нижней части периодической системы от диагонали, проведенной от бора к астату. Металлы – это элементы, между атомами которых осуществляется металлическая связь. Это сильно нелокализованная связь, когда свободные электроны (электронный газ) связывают положительные ионы металла, находящиеся в узлах кристаллической решетки. Для осуществления металлической связи необходимо, чтобы атомы имели свободные орбитали на валентном уровне. Металлическая связь не насыщена и не направлена: она объединяет очень большое число атомов, и при дальнейшем их увеличении делокализация электронов усиливается. Перекрывание s-орбиталей зависит только от расстояния между ними и не зависит от направлений, по которым они сближаются. Металлам присущи характерные признаки, проявляющиеся, как правило, одновременно: 1. Твердость – сопротивление к царапанью, вдавливанию. 2. Пластичность – способность необратимо деформироваться под действием механических нагрузок. 3. Блеск – способность компактного куска металла отражать свет. 4. Большая электро- и теплопроводность. Все эти физические свойства можно объяснить наличием электронного газа в компактном куске металла. 5. Тугоплавкость – если Тпл>1359 0C – тугоплавкие (Ti, Zr, V, Cr, Mo, W) – это связано с прочностью кристаллических решеток этих металлов.
|
||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-10; просмотров: 2095; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.138.60.175 (0.009 с.) |

 Na+ + OH– (сильное основание - сильный электролит)
Na+ + OH– (сильное основание - сильный электролит) , где α – степень диссоциации основания, Сосн –
, где α – степень диссоциации основания, Сосн – ) – будет иметь вид: Кр =
) – будет иметь вид: Кр =  Ca2+ + SO42–
Ca2+ + SO42– = 3,72∙10-5 [моль2/л2] (при 25оС)
= 3,72∙10-5 [моль2/л2] (при 25оС) .
. CH3COONa + Н2О
CH3COONa + Н2О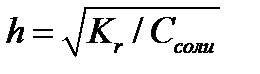 .
.


