Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Химическая организация клетокСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте В состав клетки входит около 70 химических элементов периодической системы Д.И. Менделеева. В зависимости от того, в каком количестве химические элементы входят в состав веществ, образующих живой организм, принято выделять несколько их групп. Одну группу (около 98% массы клетки) образуют четыре легких элемента: водород, кислород, углерод, азот. Их называют макроэлементами. Это главные компоненты всех органических соединений. Другую группу составляют элементы, входящие в клетку в меньших количествах. Из них сера и фосфор наряду с макроэлементами входят в состав жизненно важных органических соединений – нуклеиновых кислот, белков, жиров, углеводов, гормонов, калий, натрий, магний, марганец, железо, хлор также выполняют важные функции в клетке. Элементы, содержащиеся в клетке в очень малых количествах, носят название микроэлементов. Содержание тех или иных элементов зависит от их функциональной роли в клетке и организме, типа клеток, а также от биохимических особенностей различных групп организмов. В обмене веществ, которых эти элементы учувствуют. Большое значение имеет также способность организмов регулировать свой ионный состав. Так, растительные клетки содержат больше калия, чем животные. Во внеклеточной среде животных преобладает натрий. Содержание воды – самого распространенного неорганического соединения в живых организмах – колеблется в широких пределах, в среднем в многоклеточном организме вода составляет около 80% массы тела. Полярность молекул и способность образовывать водородные связи делают воду хорошим растворителем для огромного количества неорганических и органических веществ. Такие вещества носят название гидрофильных. Кроме того, вода обеспечивает как приток веществ в клетку, так и удаление из нее продуктов жизнедеятельности. Вода обладает хорошей теплопроводностью и большой теплоемкостью, что позволяет температуре внутри клетки оставаться неизменной при изменяющейся температуре окружающей среды. Большая часть неорганических веществ клетки находится в виде солей – либо диссоциированных на ионы, либо в твердом состоянии. Среди первых большое значение имеют катионы K, Na, Ca, которые обеспечивают раздражимость живых организмов. От концентрации солей внутри клетки зависят буферные свойства клетки. Буферность – способность клетки поддерживать слабощелочную реакцию своего содержимого на постоянном уровне в меняющихся условиях среды. Органические соединения в среднем составляют 20 – 30% массы клетки. К ним относятся биологические полимеры: белки, нуклеиновые кислоты, углеводы, а также липиды и ряд небольших молекул – гормонов, пигментов, АТФ и др. Белки. Белки среди органических веществ занимают первое место, как по количеству, так и по значению. Белки состоят из 20 видов различных аминокислот. Общая их формула
R │ H2N─HC─COOH,
где R – радикал различного строения. В левой части молекулы расположена аминная группа H2N, которая обладает свойствами основания; справа – карбоксильная группа COOH – кислотная, характерная для всех органических кислот. Следовательно, аминокислоты – амфотерные соединения, совмещающие свойства и кислоты, и основания. Соединяясь, молекулы аминокислот образуют связи между углеродом кислотной и азотом основной групп. Такие связи называют ковалентными, в данном случае – пептидными связями: R2 O H R2 R1 O H R2 │ // \ │ │ ││ │ │ H2N─HC─C + N─HC─COOH → H2N─HC─C─N─HC─COOH + H2O \\ / OH H
Соединение, состоящее из 20 и более аминокислотных остатков, носит название полипептида. Последовательность аминокислот в полипептидной цепи принято называть первичной структурой белка. Однако молекула белка в виде цепи аминокислот, последовательно соединенных между собой пептидными связями, еще не способна выполнять специфические функции. Для этого необходима более высокая структурная организация. Посредством образования водородных связей между остатками карбоксильной и аминной групп разных аминокислот белковая молекула принимает вид спирали. Это вторичная структура белка. Но в большинстве случаев только молекула, обладающая третичной структурой, может выполнять биологическую роль. Третичная структура образуется благодаря взаимодействию радикалов, в частности радикалов аминокислоты цистеина, которые содержат серу. Атомы серы двух аминокислот, находящихся на некотором расстоянии друг от друга соединяются, образуя так называемые дисульфидные, или S – S-связи. Укладка полипептидных спиралей в глобулы (шары) и называется третичной структурой белка (рис.1). Некоторые функции организма выполняются с участием белков с еще более высоким уровнем организации – четвертичной структурой. Например, гемоглобин, инсулин. Утрата белковой молекулы структурной организации называется денатурацией (от лат. denaturare – лишить природных свойств). Ренатурация – это свойство белков полностью восстанавливать утраченную структуру, если изменение среды не привело к разрушению первичной структуры. Одна из важнейших функций белков в клетке – строительная: белки учувствуют в образовании всех клеточных мембран в органоидах клетки, а также внеклеточных структур. Исключительно важное значение имеет каталитическая функция белков. Все биологические катализаторы – ферменты- вещества белковой природы. Они ускоряют химические реакции, протекающие в клетке, в десятки и сотни тысяч раз. Фермент катализирует только одну реакцию, т.е. он узкоспецифичен. Двигательная функция организма обеспечивается сократительными белками. Эти белки учувствуют во всех видах движения, к которым способны клетки и организмы: мерцание ресничек и биение жгутиков у простейших, сокращение мышц у животных. Транспортная функция белков заключается в присоединении химических элементов (например, кислорода) или биологически активных веществ (гормонов) и переносе их к различным тканям и органам тела. При поступлении в организм чужеродных - белков или микроорганизмов в белых кровяных тельцах – лейкоцитах - образуются особые белки – антитела. Они связывают и обезвреживают несвойственные организму вещества. В этом выражается защитная функция белков. Белки служат и одним из источников энергии в клетке, т.е. выполняют энергетическую функцию. При полном расщеплении 1г белка выделяется 17,6 кДж энергии. Углеводы. Углеводы, или сахариды, - органические вещества с общей формулой Cn(H2O)m. Углеводы подразделяются на простые и сложные. Простые углеводы представляют собой моносахариды. В зависимости от числа атомов углерода в молекуле моносахариды называются триозами, тетрозами, пентозами (рибоза и дезоксирибоза), гексозами (глюкоза, галактоза). Сложные углеводы, образованные многими моносахаридами, называются полисахаридами. Углеводы выполняют две основные функции: строительную (хитин) и энергетическую (крахмал у растений и гликоген у животных – энергетический резерв). Углеводы – основной источник энергии в клетке. В процессе окисления 1г углеводов освобождается 17,6 кДж энергии. Липиды. Липиды, или жиры, представляют собой соединение высокомолекулярных жирных кислот и трехатомного спирта глицерина. Жиры не растворяются в воде – они гидрофобны. В клетках всегда есть и другие жироподобные вещества – липоиды. Одна из основных функций жиров – энергетическая. В ходе расщепления 1г жиров освобождается 38,9 кДж энергии. Содержание жира в клетке составляет 5-15% массы сухого вещества. Липиды и липоиды выполняют и строительную функцию: они входят в состав клеточных мембран. Вследствие плохой теплопроводности жир способен выполнять функцию теплоизолятора. Образование некоторых липоидов предшествует синтезу ряда гормонов. Следовательно, этим веществам присуща и функция регуляции обменных процессов. Нуклеиновые кислоты. Нуклеиновые (от лат. nucleus — ядро) кислоты — сложные органические соединения. Они состоят из углерода, водорода, кислорода, азота и фосфора. Существуют два типа нуклеиновых кислот — ДНК и РНК. Они могут находиться как в ядре, так и в цитоплазме и ее органоидах. ДНК — дезоксирибонуклеиновая кислота. Это биологический полимер, состоящий из двух полинуклеотидных цепей, соединенных друг с другом. Мономеры — нуклеотиды, составляющие каждую из цепей ДНК, представляют собой сложные органические соединения. ДНК состоит из четырех азотистых оснований: производных пуринов — аденина (А) и гуанина (Г) и производных пиримидинов — цитозина (Ц) и тимина (Т), пятиатомного сахара пентозы — дезоксирибозы, а также остатка фосфорной кислоты (рис.2). В каждой цепи нуклеотиды соединяются между собой ковалентными связями: дезоксирибоза одного нуклеотида соединяется с остатком фосфорной кислоты последующего нуклеотида. Две цепи объединяются в единую молекулу водородными связями, возникающими между азотистыми основаниями, входящими в состав нуклеотидов, образующих разные цепи. Пространственная конфигурация азотистых оснований различна и количество таких связей между разными азотистыми основаниями неодинаково. Вследствие этого они могут соединяться только попарно: азотистое основание аденин (А) одной цепочки пол и нуклеотида всегда связано двумя водородными связями с тимином (Т) другой цепи, а гуанин (Г) — тремя водородными связями с азотистым основанием цитозином (Ц) противоположной полинуклеотидной цепочки. Такая способность к избирательному соединению нуклеотидов, в результате которого формируются пары А—Т и Г—Ц, называется комплементарностью (рис. 15). Если известна последовательность оснований в одной цепи (например, Т —Ц—А—Т—Г), то благодаря принципу комплементарности (дополнительности) станет, известна и противоположная последовательность оснований (А-Г-Т-А-Ц).
Рис.2 Участок молекулы ДНК. Комплементарное соединение нуклеотидов разных цепей. Цепи нуклеотидов образуют правозакрученные объемные спирали по 10 оснований в каждом витке. Последовательность соединения нуклеотидов одной цепи противоположна таковой в другой, т.е. цепи, составляющие одну молекулу ДНК, разнонаправленны, или антипараллельны: последовательность межнуклеотидных связей в двух цепях направлена в противоположные стороны: 5' —3' и 3' —5'. Сахаро-фосфатные группировки нуклеотидов находятся снаружи, а азотистые основания — внутри. Цепи, закрученные друг относительно друга, а также вокруг общей оси, образуют двойную спираль. Такая структура молекулы поддерживается в основном водородными связями (рис. 3). Вторичную структуру ДНК впервые установили американский биолог Дж.Уотсон и английский физик Ф. Крик.
Рис.3 Схема строения двойной спирали ДНК: А — плоскостная модель, жирной чертой обозначен сахаро-фосфатный остов; Б — объемная модель При соединении ДНК с определенными белками (гистонами) степень спирализации молекулы повышается - возникает суперспиральДНК, толщина которой существенно возрастает, а длина сокращается (рис. 4). Единицей компактизации молекулы ДНК служит нуклеосома, основу которой составляют 8 молекул гистонов, по 2 каждого типа (Н2А, Н2В, НЗ и Н4). Поверхности этих белковых молекул несут положительные заряды и образуют остов, вокруг которого может закручиваться отрицательно заряженная молекула ДНК. В каждую нуклеосому входит от 146 до 200 пар нуклеотидов. Гистон пятого типа - Н1 - соединяется с участками ДНК, связывающими одну нуклеосому с другой.. Такая ДНК носит название линейной или соединительной — линкерной. Нуклео сомы расположены вдоль ДНК на определенном расстоянии,неодинаковом в зависимости от типа клеток — от 20 до 50 нм. Так образуется структура, похожая на бусы, где каждая бусина — нуклеосома. Рис. 4 Схема образования суперспирали ДНК. 30 нм
Линейная ДНК
Белок Нуклеосомы и линкерная ДНК в свою очередь упакованы в фибриллы, которые в хромосоме образуют петли. Более высокие уровни спирализации позволяют значительно сократить длину молекулы ДНК. Достаточно сказать, что общая длина молекул ДНК, входящих в состав хромосом человека, составляет 1,74 м, располагаются они в клетках, имеющих диаметр 5 -7 мкм. Такую молекулу, тщательно «упакованную» белками, можно наблюдать в световой микроскоп во время деления клеток в виде хорошо окрашивающегося вытянутого тельца -х ромосомы. РНК — рибонуклеиновая кислота. РНК,так же как и ДНК, представляет собой полимер, мономерами которого являются нуклеотиды, близкие к нуклеотидам ДНК. Азотистые основания трех нуклеотидов те же самые, что входят в состав ДНК(аденин, гуанин, цитозин), четвертое основание - урацил (У) присутствует только в молекуле РНК(вместо тимина). Нуклеотиды РНК отличаются от нуклеотидов ДНК и по строению входящего в их состав углевода: они включают другую пентозу — рибозу (вместо дезо-ксирибозы). В цепочке РНКнуклеотиды соединяются благодаря образованию ковалентных связей между рибозой одного нуклео-гида и остатком фосфорной кислоты другого. По структуре различают двухцепочечные и одноцепочечные РНК. Двухцепочечные РНК— хранители генетической информации у ряда вирусов, т.е. выполняют у них функции хромосом. Одноцепочечные иРНК переносят информацию о последовательности аминокислот в белках (т.е. о структуре белков) от хромосом к месту их синтеза и участвуют в синтезе белков.
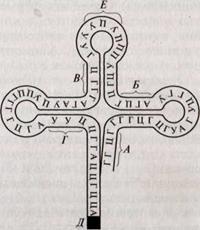
Рис.5 Схема строение тРНК: А,Б, В, Г— участки комплементарного соединения внутри одной молекулы РНК; Д — участок (активный центр) соединения с аминокислотой; Е — участок (активный центр) комплементарного соединения с молекулой и РНК (антикодон)
Существует несколько видов одноцепочечных РНК. Их названия обусловлены выполняемой функцией или местонахождением в клетке. Большую часть РНК цитоплазмы (до 80 — 90%) составляет рибосомная РНК (рРНК), содержащаяся в рибосомах. Молекулы рРНК относительно невелики и состоят из 3 — 5 тыс. нуклеотидов. Другой вид РНК — информационная (иРНК), переносящая к рибосомам информацию о последовательности аминокислот в белках, которые должны синтезироваться. Размеры этих РНК зависят от длины участка ДНК, на котором они синтезированы. Молекулы и РНК могут состоять из 300 — 30 000 нуклеотидов. Транспортные РНК (тРНК) включают 76 — 85 нуклеотидов (рис.) и выполняют несколько функций. Они доставляют аминокислоты к месту синтеза белка и осуществляют точную ориентацию аминокислоты (по принципу комплементарности) на рибосоме. тРНК имеют два активных центра, один из которых соединяется с определенной аминокислотой, а другой, состоящий из трех нуклеотидов, служит для комплементарного соединения с молекулой иРНК. Этот участок называется антикодоном.
|
|||
|
Последнее изменение этой страницы: 2016-09-20; просмотров: 751; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.169 (0.015 с.) |