Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Качественные реакции – это химические превращения, сопровождающиеся характерными признаками, с помощью которых проводят распознавание веществ.Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте Качественная реакция должна сопровождаться каким-то характерным эффектом. Это может быть изменение окраски, выпадение осадка, характерный звук, выделение газа, которое можно увидеть или почувствовать по появлению запаха. Такие явления при проведении качественных реакций называют аналитическим эффектом. Демонстрационный эксперимент. В пробирки, наполненные кислородом и углекислым газом, учитель поочередно опускает тлеющую лучинку. В одной из пробирок лучинка гаснет (рис. 54), а в другой – ярко вспыхивает (рис. 55). В каком из стаканов находится кислород? Почему вы пришли к такому выводу?
Проведенный учителем опыт позволяет отличить кислород от других газов. А как доказать, что во втором стакане находится именно углекислый газ, а, допустим, не азот, который тоже не поддерживает горение? Есть ли качественная реакция на углекислый газ? Да, такая реакция существует. Демонстрационный эксперимент. Приоткрыв крышку стакана, наполненного углекислым газом, учитель добавляет в него небольшое количество прозрачной жидкости – известковой воды. Закрыв крышку, встряхивает жидкость в стакане. При этом она мутнеет. Это качественная реакция на углекислый газ. С помощью раствора гашеной извести в воде (гашеная известь применяется в строительстве и сельском хозяйстве) – так называемой известковой воды – можно обнаружить углекислый газ. Ученический эксперимент. В выданную вам учителем пробирку с прозрачной известковой водой опустите стеклянную трубку и аккуратно продувайте через нее выдыхаемый воздух. Через некоторое время раствор помутнеет. Вещество, с помощью которого проводят качественную реакцию, называется реактивом на определяемое вещество. Известковая вода служит реактивом на углекислый газ. Однако верно и обратное: с помощью углекислого газа можно провести качественную реакцию на известковую воду. Ученический эксперимент. В четыре одинаковых сосуда налейте равные объемы обычной воды, раствора поваренной соли, сахара и известковой водой. Попросите кого-нибудь перепутать сосуды. Определите, в каком из сосудов находилась известковая вода с помощью качественной реакции: пропусканием через жидкости выдыхаемого углекислого газа. Чтобы реакцию можно было считать качественной, реактив должен давать аналитический эффект только с одним или по крайней мере немногими веществами. Иначе трудно будет сделать вывод о том, какое вещество мы обнаружили с помощью данного реагента. Примером такой специфической пары определяемое вещество–реактив могут служить крахмал и раствор йода. Как вы знаете из предыдущего параграфа, крахмал с йодом и только с ним дает сине-фиолетовое окрашивание.
2. Какие реакции называют качественными? 3. Что такое реактив на определяемое вещество? 4. Как с помощью тлеющей лучинки распознать кислород и углекислый газ?
6. С помощью йодной настойки из домашней аптечки проведите обнаружение крахмала в картофеле, хлебе, макаронных изделиях.
|
|||||||||
|
Последнее изменение этой страницы: 2016-08-25; просмотров: 1691; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.214 (0.011 с.) |



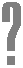 1. Сравните следующие вещества: а) медь и алюминий; б) уксусную кислоту и этиловый спирт.
1. Сравните следующие вещества: а) медь и алюминий; б) уксусную кислоту и этиловый спирт. Давайте внимательно посмотрим на таблицу Д.И.Менделеева и выберем один из элементов. Например, обитатель шестой «квартиры» – углерод. Что изображено в этой клетке? Знак (символ) химического элемента и его название. В верхнем левом углу – порядковый номер элемента, под символом элемента – его название. А что означает записанное под названием число 12,011?
Это число называется относительной атомной массой элемента, в нашем случае – углерода.
Как вы помните, одно из важнейших свойств атомов химических элементов – их масса.
Размерность массы вам хорошо известна: ее выражают в граммах, килограммах, миллиграммах. Существуют, конечно, и другие единицы массы: тонны, например, или центнеры. Однако в повседневной жизни бывает удобно оперировать не точной массой предмета, а сравнением ее с чем-либо. Поскольку массы атомов и молекул чрезвычайно малы, их сравнивают с массой атома самого легкого элемента – водорода. Такое сравнение позволяет утверждать, что масса атома углерода в 12 раз больше массы атома водорода. Масса атома кислорода больше массы атома водорода в 16 раз, а масса атома железа – в 56 раз.
Величина, показывающая, во сколько раз масса атома данного элемента больше массы атома водорода, принятой за единицу, называется относительной атомной массой элемента.
Относительную атомную массу элемента обозначают символом Аr. Подстрочная буква r – это первая буква английского слова relative, что значит относительный. Например: Аr (Н) = 1, Аr (С) = 12, Аr (N) = 14, Аr (О) = 16, Аr (Fe) = 56, Аr (Cl) = 35,5.
Обычно относительные атомные массы всех элементов округляют до целых чисел, кроме хлора (Аr (Cl) = 35,5), хотя в таблице Д.И.Менделеева они приведены с большей точностью.
Обратите внимание, что относительная атомная масса хотя массой и называется, но размерности не имеет.
Обладают ли массой молекулы веществ? Конечно! Можете ли вы ответить на вопрос, во сколько раз молекула воды тяжелее атома водорода? Это очень просто: надо сложить относительные атомные массы всех атомов, входящих в состав молекулы (рис. 56):
Mr (H2O) = 2 Ar (H) + Ar (O) = 2•1 + 16 = 18.
Давайте внимательно посмотрим на таблицу Д.И.Менделеева и выберем один из элементов. Например, обитатель шестой «квартиры» – углерод. Что изображено в этой клетке? Знак (символ) химического элемента и его название. В верхнем левом углу – порядковый номер элемента, под символом элемента – его название. А что означает записанное под названием число 12,011?
Это число называется относительной атомной массой элемента, в нашем случае – углерода.
Как вы помните, одно из важнейших свойств атомов химических элементов – их масса.
Размерность массы вам хорошо известна: ее выражают в граммах, килограммах, миллиграммах. Существуют, конечно, и другие единицы массы: тонны, например, или центнеры. Однако в повседневной жизни бывает удобно оперировать не точной массой предмета, а сравнением ее с чем-либо. Поскольку массы атомов и молекул чрезвычайно малы, их сравнивают с массой атома самого легкого элемента – водорода. Такое сравнение позволяет утверждать, что масса атома углерода в 12 раз больше массы атома водорода. Масса атома кислорода больше массы атома водорода в 16 раз, а масса атома железа – в 56 раз.
Величина, показывающая, во сколько раз масса атома данного элемента больше массы атома водорода, принятой за единицу, называется относительной атомной массой элемента.
Относительную атомную массу элемента обозначают символом Аr. Подстрочная буква r – это первая буква английского слова relative, что значит относительный. Например: Аr (Н) = 1, Аr (С) = 12, Аr (N) = 14, Аr (О) = 16, Аr (Fe) = 56, Аr (Cl) = 35,5.
Обычно относительные атомные массы всех элементов округляют до целых чисел, кроме хлора (Аr (Cl) = 35,5), хотя в таблице Д.И.Менделеева они приведены с большей точностью.
Обратите внимание, что относительная атомная масса хотя массой и называется, но размерности не имеет.
Обладают ли массой молекулы веществ? Конечно! Можете ли вы ответить на вопрос, во сколько раз молекула воды тяжелее атома водорода? Это очень просто: надо сложить относительные атомные массы всех атомов, входящих в состав молекулы (рис. 56):
Mr (H2O) = 2 Ar (H) + Ar (O) = 2•1 + 16 = 18.