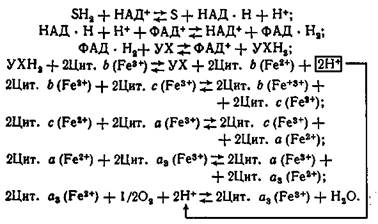Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Сучасне уявлення про механізм біологічного окисненняСодержание книги
Поиск на нашем сайте
Окиснення субстрату починається шляхом його дегідрування з участю ферментів дегідрогеназ. Дегідрогенази (їх відомо більше 150) складні ферменти, до складу молекул яких завжди входять коферменти. Існує дві групи дегідрогеназ, що різняться своїми коферментами. Ферменти першої групи містять коферментами динуклеотиди НАД або НАДФ, тому їх називають НАД або НАДФ-зале-жними дегідрогеназами. Оскільки в складі цих коферментів міститься нікотинамід (водорозчинний вітамін РР), що являє собою похідне піридину, їх називають ще піридинзалежними дегідрогеназами. Активною частиною коферментів, що входять до складу НАД- і НАДФ-залежних дегідрогеназ, є піридинове кільце нікотинаміду. Окиснені форми нікотинамідних коферментів, що позначаються НАД* (НАДФ+), відщеплюють від субстрату два атоми водню, один з яких приєднується до кільця піридину в положення відносно азоту, а другий дисоціює на протон і електрон. Останній приєднується до атома азоту кільця піридину, а протон переходить у середовище у вигляді іона Н*. Надалі відновлені форми дегідрогеназ, що утворилися, служать для окнснення їх іншою групою дегідрогеназ, оскільки вони не здатні передавати свої атоми водню безпосередньо на кисень. Дегідрогенази другої групи коферментами містять ФМН і ФАД і називаються відповідно ФМН- і ФАД-залежними дегідрогеназами. Ці дегідрогенази об'єднують під загальною назвою флавопротеїди. Активною частиною зазначених коферментів є ізоалоксазинове кільце рибофлавіну (вітаміну В2), здатне зворотно приєднувати атоми водню. Приєднання атомів водню є прямим перенесенням пари атомів водню від субстратів (ними можуть бути розглянуті вище відновлені форми піридинзалежних дегідрогеназ) на ФМН або ФАД з утворенням відновленої форми. Скорочено на прикладі ФАД це можна записати так: ФАД++2Н → ФАДН2. Відновлені форми більшості флавінових дегідрогеназ, так само, як і піридинзалежні дегідрогенази, не окиснюються киснем. Вони передають атоми водню іншій проміжній сполуці – убіхінону (УХ), або коферменту Q (KoQ), який, приєднуюча два атоми водню, перетворюється у відновлену форму гідрохінон. Дослідженнями ряду вчених установлено, що убіхінон виконує роль човника між флавопротеїдами і системою залізовмісних ферментів, які переносять електрони і називаються цитохромами. Від убіхінону відбувається розділення шляхів руху електронів і протонів атомів водню до кисню. Ланцюгом цитохромів, а їх відкрито і вивчено десятки, відбувається передача електронів атомів водню, які, перетворюючись у протони, підкислюють середовище.
Цитохроми–це група залізовмісних білків, що переносять електрони в процесі тканинного дихання від убіхінону (або від флавопротеїдів) до молекулярного кисню й активують його. Свою каталітичну функцію цитохроми виконують завдяки наявності в складі їх молекул заліза. Приєднуючи електрони, цитохроми відновлюються, віддаючи їх – окиснюються, тобто в процесі каталітичного процесу ступінь окиснення заліза зворотно змінюється. Скільки цитохромів бере участь у процесі окиснення, точно не відомо. Проте серед них добре вивчені цитохроми b, с, а і а3. Останні цитохроми (а й а3) є не що інше, як дихальний фермент Варбурга, дуже чутливий до дії ціанідів. Отже, ланка цитохромів, здійснюючи перенесення електронів, розміщується в ланцюзі окиснення між убіхіноном і киснем. Піридинзалежні дегідрогенази, флавопротеїди, убіхінон і цитохроми знаходяться в мітохондріальній мембрані і міцно з нею зв'язані в зазначеному порядку, утворюючи так званий "дихальний ланцюг". Його можна зобразити такою схемою:
Окиснювальне фосфорилювання Для різних життєвих процесів організму необхідна енергія. Під час біологічного окиснення, або тканинного дихання, яке ми розглянули вище, відбувається виділення вільної енергії, яка використовується в організмі у двох напрямках: частина її споживається для різних реакцій біосинтезу, частина використовується для підтримки постійної температури тіла, тобто перетворюється в тепло. Для того щоб вільна енергія окиснення субстратів могла бути використана для реакцій синтезу, скорочення м'язів і т.д., необхідно, щоб вона набула доступної для цього форми. На початку 1930-х років академік В.О. Енгельгардт висловив ідею про те, що при кисневому диханні відбувається фосфорилювання аденозиндифосфатної кислоти (АДФ) з утворенням аде-нозинтрифосфатної кислоти (АТФ). Пізніше, у 1939-1940 pp., радянський біохімік В.О. Беліцер установив, що при окисненні різних субстратів, зокрема, янтарної і лимонної кислот, відбувається споживання неорганічної фосфатної кислоти й утворення АТФ.
Аденозинтрифосфатна кислота являє собою універсальне рухливе джерело хімічної енергії в клітинах. Ця енергія зосереджується, або акумулюється, у пірофосфатних хімічних зв'язках молекул АТФ:
Кількість енергії, акумульованої в одному макроергічному зв'язку АТФ, складає 33,5-41,9 кДж. При гідролізі АТФ хімічна енергія макроергічних зв'язків звільняється і може бути використана для різних життєвих процесів. Таким чином, вільна енергія окиснення субстратів перетворюється в доступну для організму хімічну форму, акумульовану в пірофосфатних зв'язках АТФ, молекули якої є формою накопичення цієї енергії. Для здійснення процесу фосфорилювання, тобто з'єднання АДФ з неорганічною фосфатною кислотою, неорганічний фосфат має бути активований. Джерелом енергії для його активації служить енергія окиснення субстратів. Таким чином, процес фосфорилювання АДФ, що супроводжується утворенням АТФ, пов'язаний з процесом окиснення, тому називається окиснювальним фосфорилюванням. Саме таким шляхом в організмі синтезується значна кількість АТФ. У цьому процесі бере участь дихальний ланцюг ферментів, за допомогою яких атоми водню й електрони, відняті від субстратів, передаються на кисень. Сам же субстрат у цьому процесі участі не бере. Як показав В.О. Беліцер, при перенесенні однієї пари електронів (або двох атомів водню) від субстрату до кисню утворюється три молекули АТФ. На даний час відомо, в яких місцях дихального ланцюга відбувається активування неорганічного фосфату і фосфорилювання АДФ. Перше активування відбувається на ділянці між НАД і флавопротеїдом, друге - між цитохромами b и с, і трете – між цитохромом а3 і молекулярним киснем: < і
|
||||||
|
Последнее изменение этой страницы: 2016-08-16; просмотров: 437; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.17.78.182 (0.01 с.) |