Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Аеробне окиснення вуглеводівСодержание книги
Поиск на нашем сайте
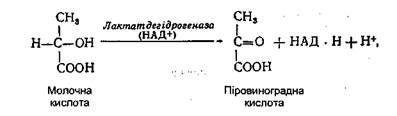
Дихання. Аеробне окиснення вуглеводів відбувається за участі кисню повітря, тому його часто називають диханням. На відміну від гліколізу (глікогенолізу), де кінцевим акцептором атомів водню й електронів служить піровиноградна кислота, при диханні роль такого акцептора виконує кисень. У першому випадку як кінцевий продукт утворюється молочна кислота, в якої сумарний ступінь окиснення вуглецю залишився таким самим, як і в глюкози, у другому випадку утворюється вуглекислий газ - більш проста сполука, в якої єдиний атом вуглецю повністю окиснений. Водночас дихання і гліколіз мають багато спільних ланок. Дихання, як і гліколіз, супроводжується утворенням фосфорних ефірів глюкози і фруктози, фосфотріоз – діоксіацетонфосфату і гліцеральдегід-3-фосфату, а також таких проміжних продуктів, як 1,3-дифоефогліцеринова кислота, 3-фосфогліцерат, фосфоенолпіруват і піровиноградна кислота. Багато реакцій гліколізу і дихання каталізуються тими самими ферментами. Іншими словами, при диханні перетворення глюкози до молочної кислоти проходить усі ті етапи, що і при гліколізі. Проте при цьому атоми водню, відщеплені від гліцеральдегід-3-фосфату, не відновлюють піровиноградну кислоту, а передаються на кисень, подолавши складну систему ферментів дихального ланцюга. Молочна кислота, що утворюється в процесі гліколізу, як уже зазначалося, містить ще досить значний запас (приблизно 93%) потенційної енергії. Проте, незважаючи на це, перші живі організми, що добували енергію в анаеробних умовах, виділяли її в навколишнє середовище. З появою в атмосфері Землі кисню живі організми виробили нові, більш досконалі механізми окиснення, в результаті яких кількість звільненої енергії виявилася набагато більшою, ніж при гліколізі, оскільки кінцевим продуктом дихання є С02, атом вуглецю якого повністю окиснений. Поряд з цим природа створила нові механізми доокиснення кінцевого продукту гліколізу, який виводиться в навколишнє середовище. Іншими словами, вона наче створила надбудову над гліколізом для окиснення його кінцевого продукту в аеробних умовах, зберігши багато попередніх його етапів. У процесі дихання не утворюється молочна кислота. Тому піровиноградна кислота є тим загальним субстратом, або центральною ланкою, де закінчується гліколіз і починається дихання (або ж розходяться шляхи гліколізу і дихання - анаеробного й аеробного окиснення глюкози). Зберігши попередні етапи гліколізу, клітини організму людини і вищих тварин зберегли здатність окиснювати глюкозу в анаеробних умовах, у результаті чого за умови нестачі кисню вони мають можливість одержувати енергію таким шляхом. Однак молочна кислота, що утворилася в анаеробних умовах, містить ще досить великий запас енергії, не викидається в навколишнє середовище, а накопичується в м'язах. Із м'язів вона током крові транспортується в печінку, де знову перетворюється в глюкозу. При надходженні в клітину достатньої кількості кисню частина молочної кислоти окиснюється далі до СО2 і Н2О. Перетворення молочної кислоти. Утворена в анаеробних умовах при окисненні глюкози, молочна кислота окиснюється до СО2 і Н2О в такий спосіб. Спочатку під дією ферменту лактатдегідрогенази, коферментом якої є НАД*, вона окиснюється до піровиноградної кислоти:
Остання під впливом піруватдекарбоксилази, що являє собою складний поліферментний комплекс, піддається окиснювальному декарбоксилюванию з утворенням активної форми оцтової кислоти - ацетил-КоА:
У тому випадку, коли тканинам добре постачається кисень, піровиноградна кислота піддається окиснювальному декарбо-ксилюванню відразу, не відновлюючись до молочної кислоти. Відновлений же кофермент НАД Н + Н+, що утворився при окисненні гліцеральдегід-3-фосфату, передає водень через ферменти аеробного обміну (тобто дихальний ланцюг) на кисень, утворюючи воду. Перетворення піровиноградної кислоти в ацетил-КоА є підготовчою, або перехідною, стадією, завдяки якій вуглеводи через піровиноградну кислоту, а потім через ацетил-КоА включаються в новий етап - кисневе окиснення. Іншими словами, цей процес - сполучна ланка між гліколізом і власне диханням. Проте вже в результаті окиснювального декарбоксилювання піровиноградної кислоти до ацетил-КоА звільняється близько 9% усієї енергії окиснення глюкози, тобто більше, ніж при гліколізі в цілому, де звільняється всього 5-7% енергії. Якщо врахувати 5-7% енергії гліколізу і 9% енергії окиснювального декарбоксилювання піровиноградної кислоти, то разом виділяється 14-16% енергії, акумульованої у вуглеводах. Отже, інші 84-86% енергії зберігаються ще в молекулі оцтової кислоти. Цикл трикарбонових кислот (цикл Кребса) являє собою новий, більш досконалий механізм окиснення вуглеводів, вироблений живими організмами з появою на Землі кисню. За допомогою цього механізму відбувається подальше перетворення оцтової кислоти у формі ацетил-КоА до С02 і Н2 О в аеробних умовах зі звільненням енергії. Оскільки першими субстратами в процесі окиснення оцтової кислоти є трикарбонові кислоти, а гіпотезу про механізм цього окиснення висунув Х.А. Кребс, процес назвали циклом трикарбонових кислот, або циклом Кребса. Першою реакцією циклу є реакція конденсації ацетил-КоА з щавлево-оцтовою кислотою, яку каталізує фермент цитрат- синтаза. У результаті утворюється активна форма лимонної кислоти - цитрил-КоА:
Гідролізуючись, цитрил-КоА перетворюється в лимонну кислоту: і Остання під дією ферменту перетворюється в цис-аконітову кислоту, яка, приєднуючи виду, перетворюється в ізолимонну кислоту:
Ізолимонна кислота далі окиснюється шляхом відщеплення двох атомів водню, перетворюючись у щавлево-янтарну. Цією реакцією починається відщеплення С02 і перше окиснення ацетил-КоА в трикарбоновому циклі. Щавлево-янтарна кислота, декарбоксилюючись, перетворюється в α-кетоглутарову кислоту. Дегідрування ізолимонної і декарбоксилювання щавлево-янтарної кислот каталізується ферментом ізоцитратдегідрогеназою за участю коферменту НАД+:
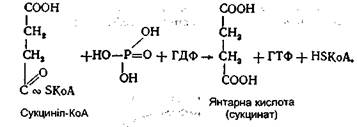
Наступним етапом циклу трикарбонових кислот є реакція окисяювального декарбоксилювання а-кетоглутарової кислоти, у результаті якої утворюється янтарна кислота. Цей процес здійснюється у дві стадії. Спочатку α-кетоглутарова кислота піддається окиснювальному декарбоксилюванню з утворенням активної форми янтарної кислоти - сукциніл-КоА - і СО2. Ця реакція нагадує реакцію перетворення піровиноградної кислоти до ацетил-КоА і каталізується також складним поліфермент-ним комплексом - α-кетоглутаратдегідрогеназою. У результаті цієї реакції відбувається друге відщеплення вуглекислого газу і дегідрування оцтової кислоти, що вступила в цикл:
Активна На наступній стадії ця енергія використовується для утворення ГТФ (гуанозинтрифосфатної кислоти) із ГДФ і неорганічної фосфатної кислоти і запасається у фосфатних зв'язках цієї сполуки. Реакція каталізується ферментом сукцинілтіокіназою:
Утворений у результаті цієї реакції ГТФ взаємодіє з АДФ, утворюючи АТФ: ГТФ + АДФ → 2 ГДФ + АТФ, Синтез АТФ, спряжений з окисненннм субстрату, є ще одним прикладом субстратного фосфорилювання. Надалі в ході циклу трикарбонових кислот відбувається ще два дегідрування. Янтарна кислота під дією сукцинатдегідроге-нази за участю коферменту ФАД+ втрачає два атоми водню і перетворюється у фумарову кислоту, а ФАД+ відновлюється до ФАД · Н2. Потім фумарова кислота, приєднуючи молекулу води, утворює яблучну кислоту (малат), яка за допомогою малатдегідрогенази і коферменту НАД+ знову піддається дегідруванню. При цьому утворюється щавлево-оцтова кислота, тобто субстрат, з якого почався цикл трикарбонових кислот:
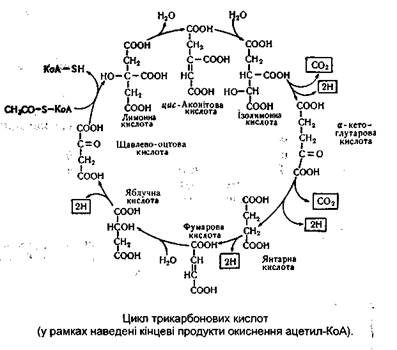
Регенерована щавлево-оцтова кислота може знову вступати в реакцію з новою молекулою ацетил-КоА, і процес почнеться в тому ж порядку. Загальну схему циклу три карбонових кислот можна представити таким чином:
З даної схеми видно, що основна функція циклу Кребса полягає в дегідруванні оцтової кислоти. Якщо підвести баланс ферментативного дегідрування одного циклу, можна легко підрахувати, що в результаті реакцій утворюється вісім атомів водню: шість атомів використовується для відновлення НАД+ і два - на відновлення ФАД+ сукцинатгідрогенази. Сумарна реакція цього циклу описується таким рівнянням:
із якого випливає, що чотири атоми водню належать воді. Отже, інші чотири утворилися при дегідруванні оцтової кислоти, тобто це весь водень, що був у складі її молекули. Одночасно з цим у вигляді оксиду вуглецю (IV) двічі виділилося два атоми вуглецю (один раз при декарбоксилюванні щавлево-янтарної кислоти, другий - при декарбоксилюванні а-кетоглутарової кислоти), тобто саме стільки, скільки їх надійшло в цикл у формі ацетильної групи. З наведеного вище рівняння також випливає, що в циклі не використовуються ні кисень, ні АТФ, ні неорганічна фосфатна кислота. Всі ці метаболіти взаємодіють у дихальному ланцюзі, куди залучаються неорганічна фосфатна кислота, відщеплені при дегідруванні атоми водню і кисень, а як результат окиснювального фосфорилювання утворюється АТФ. Енергія для цього процесу виділяється під час окисно-відновних реакцій при переході атомів водню та електронів від відновлених форм НАД - Н2 і ФАД · Н2 на кисень. На кожну пару електронів (пару атомів водню) у дихальному ланцюзі шляхом окиснювального фосфорилювання утворюється три молекули АТФ (одна при перенесенні атомів водню від НАД · Н + Н+ до ФАД, друга - при перенесенні пари електронів від цитохрому b до цитохрому с і третя - від цитохрому а3 до атома кисню). Таким чином, кожна окиснювальна стадія перетворення глюкози до СO2 і Н2O, пов'язана з НАД, супроводжується утворенням трьох молекул АТФ, пов'язана з ФАД - утворенням двох молекул АТФ. Енергетичний баланс окиснення вуглеводів. Спочатку підіб'ємо підсумок енергетичного балансу за рахунок дегідрування оцтової кислоти в циклі Кребса. Як ми вже встановили, у цьому циклі відбувається чотири дегідрування, у результаті яких утворюється три відновлені форми НАД, одна - ФАД і шляхом субстратного фосфорилювання синтезувалася одна молекула АТФ:
Таким чином, у циклі Кребса синтезується в шість разів більше АТФ, ніж при гліколізі. Якщо врахувати ще дві відновлені молекули НАД, які утворилися при окисненні молочної і піровиноградної кислот, то це складе ще 6 молекул АТФ, а в сумі -18. Оскільки глюкоза розпадається на дві фосфотріози, кількість АТФ збільшується у 2 рази і складе 36 молекул. Додавши до цього 2 молекули АТФ, що утворилися в процесі гліколізу, одержимо загальний баланс енергії, акумульованої в макроергічних зв'язках АТФ при окисненні глюкози до СО2 і Н2О: 36+2=38. Установлено, що повне окиснення 1 моля глюкози до С02 і Н20 супроводжується виділенням 2872 кДж. У 38 молекулах АТФ акумулюється 1270-1560 кДж, тобто біля 50% усієї енергії, звільненої в процесі окиснення. Отже, решта 50% енергії розсіюється в організмі у формі тепла для підтримання постійної температури. З розглянутих вище фаз окиснення глюкози надзвичайно важливе значення має аеробна фаза. Якщо за умов анаеробного окиснення, тобто при утворенні молочної кислоти, виділяється всього 197 кДж енергії, з яких 40% акумулюється в макроергі-чних зв'язках двох молекул АТФ, то в аеробній фазі виділяється 2872 -197 = 2675 кДж, що складає близько 93% усієї енергії. Таким чином, основну масу енергії організм одержує в процесі дихання. Алотомічне окиснення глюкози. Поряд з циклом Кребса в багатьох клітинах існує й інший шлях розщеплення глюкози, який має назву апотомічний, або пентозофосфатний. Експериментально встановлено, що в аеробних умовах в еритроцитах, печінці, нирках глюкоза може окиснюватись до 6-монофосфо-глкжонової кислоти, причому фруктозо-1,6-дифосфат під час цього процесу не утворюється. У результаті такого окиснення глюкози утворюється значна кількість пентоз. Цей спосіб був відкритий радянським біохіміком В.О. Енгельгардтом, а окремі його етапи вивчені О- Варбургом, Ф. Диккенсом, І.Д. Головаць-ким І Ін. Пентозофосфатний шлях не є головним шляхом окиснення глюкози. Основне його призначення полягає в тому, щоб постачати клітини відновленими формами НАДФ, необхідними для біосинтезу жирних кислот, холестерину, пуринових і піримі-динових основ, стероїдів і ін. Друга функція цього шляху полягає в тому, що він поставляє пентози, головним чином D-рибозу, для синтезу нуклеїнових кислот. Пентозофосфатний шлях розщеплення глюкози сумарно можна представити таким рівнянням:
Пентози, не використані для біосинтезу нуклеїнових кислот і нуклеотидів, витрачаються на біосинтез інших сполук і регенерацію глюкози. БІОСИНТЕЗ ВУГЛЕВОДІВ Існує два основні шляхи біосинтезу вуглеводів із відносно нескладних метаболітів. Один із них полягає у відновленні вуглекислого газу до глюкози. Цей процес, характерний для зелених рослин і названий фотосинтезом, здійснюється за рахунок енергії сонячних променів за допомогою хлорофілу згідно з рівнянням:
Уловлюючи сонячні промені і перетворюючи їх енергію в енергію вуглеводів, зелені рослини забезпечують зберігання і розвиток життя на Землі. У цьому полягає, за словами К.А. Тимірязєва, космічна роль зелених рослин як посередника між сонцем і всім живим на Землі. Останнім часом роботи групи вчених Інституту біохімії ім. О.В. Палладіна НАН України під керівництвом академіка М.Ф. Гулого показали, що тканини вищих тварин також здатні фіксувати вуглекислий газ, хоча механізм його фіксації відрізняється від такого ж у фотосинтезуючих клітинах. Він полягає в нарощуванні вуглецевого скелета оксидом вуглецю (IV) таких субстратів, як кетокислоти, жирні кислоти, амінокислоти й ін. У печінці, нирках і скелетних м'язах людини І вищих тварин існує інший шлях біосинтезу вуглеводів, який називають глюконеогенезом. Це синтез глюкози з піровиноградної або молочної кислоти, а також із так званих глікогенних амінокислот, жирів і інших попередників, що в процесі метаболізму можуть перетворюватися в піровиноградну кислоту або метаболіти циклу трикарбоновых кислот. Глюконеогенез - це шлях, обернений гліколізу. Проте цей шлях має три стадії, що в енергетичному відношенні не можуть бути використані при перетворенні піровиноградної кислоти в глюкозу. Ці три стадії гліколізу замінені "обхідними" реакціями з меншою витратою енергії. Першою обхідною реакцією є перетворення піровиноградної кислоти у фосфоенолпіровиноградну. Оскільки розщеплення глюкози відбувається в мітохондріях, а синтез - у цитоплазмі, на першому етапі мітохондріальна піровиноградна кислота перетворюється спочатку в щавлево-оцтову. Каталізує це перетворення фермент піруваткарбоксилаза, яка активується ацетил-КоА за участю АТФ. Щавлево-оцтова кислота, що утворилася, відновлюється потім за участю НАД Н + Н+ в яблучну:
Яблучна кислота дифундує в цитоплазму, окиснюється цитоплазматичною малатдегідрогеназою з утворенням цитоплазматичної щавлево-оцтової кислоти, з якої утворюється фосфоенол-піровиноградна кислота. Цю реакцію каталізує фосфоенолпіру-ваткарбоксикіназа. Донором фосфатної кислоти виступає ГТФ;
Далі відбувається ціла серія обернених реакцій, які закінчуються утворенням фруктозо-1,6-дифосфату. Перетворення фруктозо-1,6-дифосфату у фруктозо-6-фосфат - друга незворотна реакція гліколізу. Тому вона каталізується не фосфофруктокіназою, а фруктозодифосфатазою. Цей фермент каталізує незворотний гідроліз 1-фосфатної групи: Фруктозо-1,6-дифосфат + Н2О → Фруктозо-6-фосфат + Н3РО4 На наступній (оборотній) стадії біосинтезу глюкози фруктозо-6-фосфат перетворюється в глюкозо-6-фосфат під дією фосфоглюкоізомерази гліколізу. Розщеплення глюкозо-6-фосфату до глюкози - третя незворотна реакція, яка не здійснюється шляхом обернення гексокіназою. Вільна глюкоза утворюється за допомогою глюкозо-6-фосфатази, що каталізує реакцію гідролізу: Глюкозо-6-фосфат + Н2O → Глюкоза + Н3РO4. У більшості клітин глюкозо-6-фосфат, який утворюється в процесі глікогенолізу, використовується як попередник для біосинтезу оліго- і полісахаридів. Велику роль у біосинтезі цих складних сахаридів відіграє сполука уридиндифосфоглюкоза, яка виконує роль проміжного переносника глюкози. Під час біосинтезу глікогену, наприклад, глюкозо-6-фосфат, перетворившись у глюкозо-1-фосфат під дією фосфоглюкомута-зи, взаємодіє з уридинтрифосфатною кислотою (УТФ) - сполукою, аналогічною АТФ, в яку замість аденіну входить азотиста основа урацил. У результаті цієї взаємодії за допомогою глюкозо-1-фосфатуридилтрансферази утворюється уридилдифосфо-глюкоза:
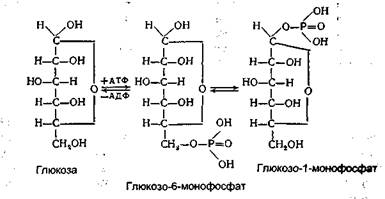
На заключному етапі біосинтезу глікогену в реакції, що каталізується глікогенсинтетазою, залишок глюкози з УДФ-глюкози переноситься на кінцевий залишок глюкози амілазного ланцюга з утворенням 1,4-глікозидного зв'язку. Розгалуження глікогену шляхом утворення 1,6-зв'язків завершується аміло-1,4-1,6-трансглюкозидазою. Біосинтез глікогену здійснюється не тільки з глюкозо-6-фосфату, який утворився шляхом глюконеогенезу. Як уже зазначалося вище, для його біосинтезу використовується також частина глюкози після всмоктування. Синтез глікогену як процес утворення рухливого резерву вуглеводів в організмі має велике біологічне значення. Головна роль у цьому належить печінці. Завдяки синтезу і відкладанню глікогену в печінці підтримується постійна концентрація глюкози в крові й інших тканинах, а також запобігаються втрати її з сечею при вживанні їжі, особливо вуглеводної. Крім того, відкладання глікогену в печінці сприяє поступовому використанню вуглеводів залежно від умов існування організму. Використанню глюкози для синтезу глікогену передує утворення глкжозофосфорних ефірів. Спочатку утворюється глюкозо-6-монофосфат. Джерелом енергії і донатором фосфату є АТФ. Каталізує цю реакцію гексокіназа. Під дією ферменту фосфо-глюкомутази глюкозо-6-монофосфат перетворюється в глюкозо-1-монофосфат:
Подальше перетворення глюкозо-1-монофосфату в глікоген відбувається вже знайомим нам шляхом.
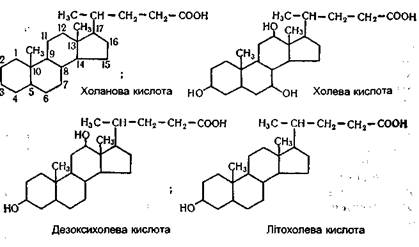
Обмін ліпідів Ліпіди являють собою велику групу органічних сполук. Всі вони різняться за своїм хімічним складом і структурою, але мають одну загальну для них властивість - нерозчинність у воді. Оскільки ферменти, які діють на ці органічні сполуки, водорозчинні, розщеплення й усмоктування ліпідів у харчовому каналі характеризуються деякими особливостями. Наявність же ліпідів різної структури зумовлює різноманітні шляхи їх розщеплення і синтезу. Зупинимося на обміні жирів, фосфатидів і стеридів, які мають найбільш важливе біологічне значення. Обмін ліпідів, як і вуглеводів, - багатоступінчатий процес, що складається з травлення, усмоктування, транспортування кров'ю, внутрішньоклітинного окиснення і біосинтезу. ТРАВЛЕННЯ ЛІПІ ДІВ Перетравлення тригліцеридів. Тригліцериди, або нейтральні жири, є концентрованими джерелами енергії в організмі. При окисненні 1 г жиру звільняється близько 38,9 кДж енергії. Як гідрофобні сполуки жири резервуються в компактній формі, займаючи порівняно мало місця в організмі. Разом із їжею в організм людини щодоби надходить до 70 г жирів рослинного і тваринного походження. За своєю хімічною природою вони є головним чином триглі церидами. Розщеплення жирів відбувається за допомогою ферментів, які називають ліпазами. Слина не містить таких ферментів, тому в ротовій порожнині жири ніяких змін не зазнають. У шлунку активність ліпази дуже слабка. Це викликано тим, що в шлунку реакція середовища дуже кисла (рН=1,5 -2,5), у той час як оптимум дії ліпази знаходиться при рН=7,8 - 8,1. У зв'язку з цим у шлунку перетравлюється всього 3-5% жирів, що надходять. Перетравлювання жирів у шлунку відбувається тільки в новонароджених і дітей грудного віку. Це пов'язано з тим, що рН середовища в шлунку новонароджених становить 5,6, а за цих умов ліпаза проявляє велику активність. Крім того, жир молока матері, який є основним продуктом харчування дітей у цей період, знаходиться в сильно емульгованому стані, а саме молоко містить ліполітичний чинник, що бере участь у перетравлюванні жирів. Проте шлунок усе не відіграє певну роль у процесі перетравлювання жирів у дорослих. Він регулює надходження жиру в кишки і перетравлює білки, звільняючи таким шляхом жир з ліпопротеїдних комплексів їжі. Основним місцем перетравлювання жирів є дванадцятипала кишка і відділи тонкої кишки. Оскільки жири нерозчинні у воді, а ферменти, що розщеплюють їх, є водорозчинними сполуками, необхідною умовою для гідролітичного розщеплення жирів на складові частини є їх диспергування (подрібнення) з утворенням тонкої емульсії. Диспергування й емульгування жиру відбувається в результаті дії декількох чинників: жовчних кислот, вільних вищих жирних кислот, моно- і дигліцеридів, а також білків. Цьому сприяють також перистальтика кишок і вуглекислий газ, що постійно утворюється при взаємодії кислих компонентів їжі, що надходять із шлунка, з карбонатами кишок, які створюють лужне середовище. Вуглекислий газ, що утворюється, "пробулькує" через харчові маси, беручи участь таким чином у диспергуванні жиру. Нейтралізації вмісту шлунку сприяє також надходження в просвіт тонкої кишки жовчі, яка має лужний характер. Жовч - густа рідина світло-жовтого кольору зі специфічним запахом, гірка на смак. До складу жовчі входять жовчні кислоти, жовчні пігменти, продукти розпаду гемоглобіну, холестерин, лецитин, жири, деякі ферменти, гормони й ін. Жовч сприяє перистальтиці тонкої кишки, здійснює бактеріостатичну дію на її мікрофлору. З жовчю виділяються з організму отрути. Вона є також активатором ліполітичних ферментів і підвищує проникність стінки кишок. Головною складовою частиною жовчі є жовчні кислоти. Вони утворюються в печінці з холестерину і знаходяться в жовчі як у вільному, так і зв'язаному стані, а також у вигляді натрієвих солей. У жовчі людини містяться в основному три жовчні кислоти. Основну масу складають холева (3,7,12-тригідрокси-холанова) і дезоксихолева (3,12-дигідроксихоланова), невелику частину - літохолева (3-гідроксихоланова) кислоти, які є похідними холанової кислоти:
Холева кислота може знаходитися в жовчі також у зв'язаному стані у вигляді парних сполук з гліцином і похідним цистеїну таурином- відповідно глікохолевої і таурохолевої кислот:
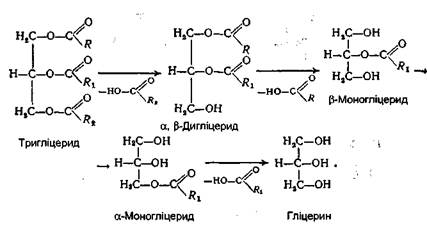
Завдяки наявності жовчних кислот відбувається зменшення поверхневого натягу ліпідних крапель, що сприяє утворенню дуже тонкої і стійкої емульсії, діаметр часток якої становить близько 0,5 мкм. Утворенню емульсії сприяють також моногліцериди і вищі жирні кислоти. Емульгування жиру призводить до колосального збільшення поверхні дотикання ліпази з водним розчином. Таким чином, чим тонша емульсія жирів, тим краще і швидше вони розщеплюються ліпазою. Крім того, у вигляді тонкої емульсії жири можуть навіть усмоктуватися стінкою кишок безпосередньо, не розщеплюючись на складові частини. За наявності жовчних кислот під дією ліпази в просвіті тонкої кишки відбувається гідролітичне розщеплення жирів. У результаті цього утворюються продукти часткового і повного розщеплення жирів - моно- і дигліцериди, вільні вищі жирні кислоти і гліцерин:
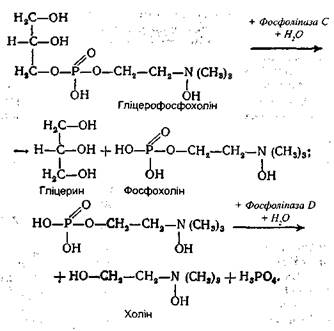
Тут же міститься і частина нерозщепленого жиру у вигляді дуже тонкої емульсії. Всі ці продукти надалі всмоктуються стінками кишок. У суміші тригліцериди складають близько 10%, моно- і дигліцериди - також 10%, а основна маса (близько 80%) продукти повного розщеплення жирів (гліцерин і вищі жирні кислоти). Перетравлення фосфогліцеридів. Основним місцем перетравлювання фосфатидів також є дванадцятипала кишка. Емульгування цих ліпідів відбувається під впливом тих же речовин, що і три гліцеридів. Проте гідролітичне розщеплення фосфатидів здійснюється під дією фосфоліпаз А, В, С і D. Кожний фермент діє на певний складноефірний зв'язок фосфоліпіду. Гідролітичне розщеплення, наприклад, лецитину відбувається в такий спосіб:
Такому повному розщепленню підлягає незначна частина фосфатидів, оскільки проміжні продукти розщеплення добре розчинні у воді і легко всмоктуються стінками кишок. До того ж фосфогліцериди легко утворюють емульсії, які також можуть усмоктуватися кишковою стінкою.
Перетравлення стеридів. Стериди, що входять до складу їжі, емульгуються під впливом тих же чинників, що і жири, після чого піддаються гідролітичному розщепленню до вільних стеринів і вищих жирних кислот. Цей процес здійснюється під дією ферменту холестеринестерази. УСМОКТУВАННЯ ЛІПІДІВ У результаті травлення жирів, фосфатидів, стеридів у просвіті тонкої кишки утворюється значна кількість продуктів їх часткового і повного гідролітичного розщеплення; моно- і дигліцериди, вищі жирні кислоти, стерини, азотисті основи, фосфатна кислота. Міститься також невелика кількість три-гліцеридів, які знаходяться в тонкоемульгованому стані. Всі ці продукти всмоктуються стінкою тонкої кишки. Такі продукти розщеплення, як жирні кислоти і холестерин, погано розчиняючись у воді, утворюють з жовчними кислотами водорозчинні комплекси - так звані холеїнові кислоти. Ці кислоти легко проникають в епітеліальні клітини стінки кишок, де розщеплюються на складові частини. Звільнені жовчні кислоти повертаються в просвіт кишок і знову використовуються для транспортування нерозчинних у воді продуктів розщеплення жирів. Частина продуктів розщеплення (гліцерин, гліцеринфосфатна кислота, азотисті основи) добре розчинні у воді і легко проникають в епітеліальні клітини. Фосфатна кислота всмоктується в клітини епітелію стінки тонкої кишки у вигляді натрієвих і калієвих солей. В основі всмоктування ліпідів лежить ряд складних фізико-хімічних і біологічних процесів, для здійснення яких витрачається енергія макроергічних зв'язків АТФ. В епітеліальних клітинах слизистої оболонки кишок із продуктів гідролітичного розщеплення, що всмокталися, знову синтезуються ліпіди. Проте цей ресинтез призводить до утворення специфічних жирів, характерних для даного організму. Для утворення нейтральних жирів використовуються вищі жирні кислоти, гліцерин, моно- і дигліцериди. Одночасно відбувається і синтез фосфатидів, для яких використовуються головним чином гліцеринфосфатна кислота, гліцериди і дигліцериди, а також у невеликій кількості моногліцериди. З холестерину і вищих жирних кислот утворюються стериди. В епітеліальних клітинах стінок кишок із синтезованих ліпідів, а також крапель тригліцеридів, що всмокталися, вітамінів (A, D, Е, К) і білків утворюються комплекси розміром 150-200 нм, які називаються хіломікронами, Хіломікрони наповнені різного роду ліпідами, утвореними переважно тригліцеридами, зовнішня білкова оболонка дозволяє хіломікронам добре розчинятися у воді. Хіломікрони дифундують спочатку в міжклітинну рідину, потім у лімфатичні капіляри і зрештою потрапляють у кров'яне русло, де під дією гепарину розпадаються на дрібні частинки. З током крові вони розносяться по всьому організму і відкладаються в резерв у жирових депо - під шкірою, навколо нирок, сальнику, брижі, м'язовій тканині. Частина жирів крові використовується для пластичних цілей, як джерело хімічної енергії і т.д. Таким чином, хіломікрони є переносниками утворених епітеліальними клітинами тонкої кишки ліпідів. При цьому вони транспортують у крові головним чином тригліцериди. Поряд з хіломікронами існують і інші форми транспорту ліпідів кров'ю, наприклад α- і β-ліпопротеїди. Найбільш рухливою формою ліпідів є вільні вищі жирні кислоти. Важлива роль в активному транспортуванні ліпідів належить форменим елементам крові. Еритроцити, наприклад, беруть участь у перенесенні фосфатидів і холестерину, лейкоцити - тригліцеридів. Велика роль в обміні ліпідів належить жировим депо. Дослідження показали, що в жирових депо відкладається не тільки знов синтезований в організмі специфічно видовий жир, але й у невеликих кількостях чужорідний, тобто той, що входив до складу їжі. Досліди, проведені на собаках, які голодували, показали, що харчові жири після всмоктування надходять спочатку в жирові депо, з яких переходять у плазму крові. Таким чином, жирова тканина не є пасивним депо жирів, склад її постійно поновлюється за рахунок ліпідів, що всмоктуються з кишок або синтезуються в організмі.
|
||||
|
Последнее изменение этой страницы: 2016-08-16; просмотров: 900; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.217.89 (0.016 с.) |






 форма янтарної кислоти, що утворилася, сукциніл-КоА на відміну від ацетил-КоА являє собою макроергічну тіо-ефірну сполуку, в якій акумульована енергія окиснення α-кетоглутарової кислоти.
форма янтарної кислоти, що утворилася, сукциніл-КоА на відміну від ацетил-КоА являє собою макроергічну тіо-ефірну сполуку, в якій акумульована енергія окиснення α-кетоглутарової кислоти.