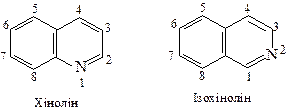Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Гетероциклічні ароматичні сполукиСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
РОЗДІЛ 9. ГЕТЕРОЦИКЛІЧНІ АРОМАТИЧНІ СПОЛУКИ Гетероциклічні сполуки - речовини, що містять у молекулах цикли, у яких один або більше атомів є елементами, відмінними від вуглецю, (O, S, N, P тощо). Гетероциклічні сполуки, як правило, мають ароматичний характер. Їх класифікують: 1. За загальним числом атомів у циклі (три-, чотири-, п’ятичленні, тощо); 2. За кількістю гетероатомів (1, 2, 3 тощо); 3. За природою гетероатомів НОМЕНКЛАТУРА За номенклатурою IUPAC назви гетероциклів складаються з префікса, кореня та закінчення. Назва = префікс + корінь + суфікс. Префікс означає природу гетероатома: -O- окса, окс- -S- тіа-, ті- -N- аза-, аз- -P- фосфа-, фосф- Корінь означає розмір циклу:
Суфікс означає ступінь насиченості циклу: насичений -ідін з атомом N, - ан - без атома N; ненасичений –ін; Приклади назв гетероциклів за номенклатурою IUPAC
Азирідин Оксиран Азолідин (етиленімін) (етиленоксид) (піролідин)
Нумерація атомів у циклі починається з гетероатома. Застосовується позначення положення замісника: α,β,γ тощо.
Пірол 1,4-Дигідро- Піран (азол або азоци- піридин клопентадієн)
Нумерація атомів у конденсованих циклах починається від місця, сусіднього з місцем конденсації циклів так, щоб гетероатом отримав мінімальне значення локанта
Ізохінолін Індол (α, β-бензопірол)
Для багатьох гетероциклічних сполук широко застосовуються тривіальні назви.
П'ятичленні гетероцикли з одним гетероатомом
Пірол Фуран Тіофен
П'ятичленні гетероцикли можна розглядати, як продукт заміщення в бензеновому ядрі фтагмента —СН=СН— на гетероатом з неподіленою парою електронів. ρ-Обіталь гетероатома, на якій розташована неподілена пара електронів вступає у спряження з π-орбіталями двох π-зв’язків, утворюючи циклічну спряжену π-електронну систему, у якій на 5-ти спряжених орбіталях знаходяться 6 електронів (4 р-електрони від двох подвійних зв'язків і два від гетероатома). Така циклічна спряжена система відповідає правилу Хюккеля, а значить має ароматичний характер. Вказані гетероцикли мають досить високу енергію резонансної стабілізації, хоч і меншу, ніж у бензену. Так, енергія спряження для тіофону складає приблизно 120 кДж/моль, піролу 110, а для фурану – 80 кДж/моль. Нагадаємо, що енергія спряження бензену становить 152 кДж/моль. Зрозуміло, що середня електронна густина в їх молекулах вища, ніж в молекулі бензену, і кожен атом циклу несе частковий негативний заряд. Причому, на α-атомах вуглецю він більший, ніж на β. (δ- > δ′-).
Цікаво відмітити, що в результаті спряження електронної пари азоту пірол втрачає основні властивості, притаманні іншим амінам. З тієї ж причини фуран не проявляє властивостей етерів, а тіофен – сульфідів. Так, останній не окиснюється за атомом сірки, що характерно для аліфатитчних сульфідів. Розглянемо окремі п’ятичленні гетероцикли. Фуран та його похідні Фуран - безбарвна рідина із запахом хлороформу. Одержання Основний промисловий метод добування фурану - декарбонілування фурфуролу
Фурфурол Декарбоксилювання2-фуранкарбонової (пірослизової) кислоти
Фурфурол і пірослизову кислоту одержують, відповідно, з альдопентоз і цукрової кислоти.
Альдопентоза Фурфурол
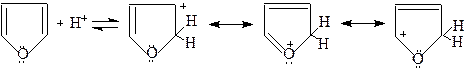
Цукрова 2-Фуранкарбонова кислота (пірослизова) кислота Хімічні властивості Ацидофобні властивості Фуран під дією кислот легко протонується за α-вуглецевим атомом, втрачаючи при цьому ароматичні властивості. Утворений спряжений катіон далі обсмолюється або полімеризується з розривом циклу. Таке руйнування структури під дією кислот називається ацидофобністю.
При введенні у фурановий цикл електроноакцепторних замісників стійкість гетероциклу до дії кислот підвищується. Сульфування Комплекс піридину з сірка(VI)оксидом є доволі активним сульфуючим агентом, здатним сульфувати фуран.
2.2.4. Ацилювання фурану здійснюють у присутності кислот Льюїса (ZnCI2 або SnCI4 . Як ацилюючі агенти, використовують, переважно, ангідриди кислот.
Реакції приєднання При каталітичному гідруванні фуран перетворюється у тетрагідрофуран
Тетрагідрофуран
Реакції дієнового синтезу Фуран може реагувати як 1,3-дієн, тобто, виявляє проміжні властивості між ароматичними і дієновими сполуками.
Малеїновий ангідрид Ангідрид 3,6-ендоксо- 1,2,3,6--тетрагідрофталевої кислоти
Реакція окиснення При окисненні фурану отримують малеїновий ангідрид.
Тіофен та його похідні Тіофен є найстійкішим із п'ятичленних гетероциклів. Він не має ацидофобних властивостей (не боїться кислот). Підвищена стабільність тіофену пояснюється здатністю атома сірки надавати вакантні d-орбіталі для делокалізації π-електронів, а також великим атомним радіусом атома сірки, завдяки чому утворюється цикл з меншими викривленнями валентних кутів, а значить і з меншим напруженням циклу. Одержання Тіофен виділяють із кам'яновугільної смоли або синтезують із бутану і сірки
При взаємодії ацетилену з сірководнем також утворюється тіофен.
Хімічні властивості Реакції дієнового синтезу
Диціанацетилен о -Фталодинітрил
Пірол і його похідні Одержання Пірол одержують із фурану та аміаку (Ю.К.Юр'єв,1936)
Аналогічним шляхом вдається замінити один гетероатом на інший (взаємне перетворення циклів за Юр'євим)
Хімічні властивості Ацидофобні властивості Пірол ацидофобний. Він легко протонується, що веде до руйнування його спряженого циклу, аналогічно до фурану. Реакції приєднання. Пірол приєднує водень у момент виділення з утворенням піроліну або каталітично збуджений водень, в результаті чого утворюється піролідин.
Індол Одержання Індол міститься у кам'яновугільній смолі. Синтетично його отримують реакцією циклізації фенілгідразонів
або конденсацією аніліну з ацетиленом за методом О.Чічібабіна.
За своєю будовою і властивостями він нагадує нафтален. Хімічні властивості Індол виявляє ацидофобні властивості, а під дією лугів утворює металічні похідні індолу
На відміну від піролу, в індолі реакції електрофільного заміщення протікають не біля другого, а біля третього атома вуглецю, що зумовлено впливом бензенового кільця. Індол та його похідні відіграють надзвичайно важливу роль у живій природі. Велике значення має β-індолілоцтова кислота (гетероауксин) – стимулятор росту рослин:
β-Індоліланін (триптофан) – одна з найважливіших незамінимих амінокислот.
Індоксил Найважливішим з кисневмісних похідних індолу є індоксил (3-оксоіндол), який отримують циклізацією феніламінооцтової кислоти (метод Геймана):
або з орто -амінобензоатної кислоти
Індоксил у розчинах здатний до кето-енольної таутомерії.
Індиго При окисненні індоксилу на повітрі утворюється барвник синього кольору - індиго:
Транс -форма індиго
Раніше індиго добували з тропічної рослини “indigofera”. Він здавна відомий, але й сьогодні не втратив свого значення. Ним традиційно фарбують джинсові тканини. Хоч тепер замість натурального індиго майже всюди використовують синтетичний барвник. Індиго не розчиняється у воді. Тому, щоб пофарбувати ним волокно, треба перевести його у водорозчинну форму. Для цього індиго відновлюють і одержують у воді безбарвну форму – “біле індиго”. Волокно просочують розчином “білого індиго” і потім сушать на повітрі. Під дією кисню повітря “біле індиго” окиснюється до “синього індиго” і волокно набуває забарвлення. Такий процес фарбування, при якому нерозчинний барвник переводять у розчинну форму, наносять у вигляді розчину на тканину або волокно і потім знову роблять нерозчинним – називають кубовим фарбуванням.
Кетонна форма Єнольна форма “біле індиго”
Гетероатомом Одним з головних представників такого типу гетероциклів є піридин.
Піридин
1. Одержання 1.1. Основним джерелом піридину для промисловості служитькам'яновугільна смола. Гомологи піридину можна одержувати синтетичними методами. Метод Реппе
5-Етил-2-метилпіридин 5-Вініл-2- метилпіридин З альдегідів
Акролеїн 3-Метилпіридин (β-Піколін) Хімічні властивості Основність піридину. У молекулі піридину кожен атом циклу надає у спряжену систему один електрон, тому неподілена пара електронів атома азоту не приймає участь в ароматичному секстеті. В результаті азот проявляє електронодонорні властивості, що робить піридин доволі сильною основою. Основність піридину близька до основності аніліну. З кислотами він утворює солі піридинію.
2.2. Гідрування піридину Піридин гідрується легше, ніж бензен. Водень для процесу гідрування зручно добувати при взаємодії спирту з металічним натрієм.
Піперидин (гексагідропіридин)
2.3. Реакції∙ електрофільного заміщення. Оскільки атом азоту характеризується більшою електронегативністю ніж вуглець і стягує на себе електронну густину ядра, реакції електрофільного заміщення протікають набагато важче, ніж для бензену, причому електрофіл заміщує водень переважно у третьому положенні, де залишається найбільша електронна густина.
Увести замісник α-положення у такий спосіб неможливо. Здійснити пряме електрофільне заміщення в γ-положення також неможливо. Однак для одержання γ-заміщених похідних піридину часто використовують N-оксид піридину (див.стор.). Похідні піридину. 5-Вініл-2-метилпіридин одержують дегідруванням 5-етил-2-метилпіридину. Використовують як кополімер при одеранні вінілпіридинових каучуків і як проміжний продукт при сннтезі медичного препарату – димебону. Нікотинова кислота та її похідні використовуються як лікарські засоби. Сама нікотинова кислота володіє протипеларгічною дією, спричиняє судинорозширюючу дію, покращує вуглеводневий обмін. Її амід – нікотинамід видомий як вітамін РР.
Водний розчин N,N-діетиламіду нікотинової кислоти (25%) – ефективний кардіологічний препарат – кордіамін (корамін, некетамід, тонокард). Нікотинова кислота міститься у молоці, м’ясі, рибі, дріжджах тощо. Добова потреба людини в нікотиновій кислоті становить 20-30 мг. Вітамін В6 (піридоксин) міститься в таких природних продуктах, як дріджджі, бобові, печінка.
Серед похідних піридину зустрічаються ефективні гербіциди. Так, 2 г 4-аміно-3,5,6-трихлоропіридин-2-карбонової кислоти (“Піклорам “, або “Гордон”) достатньо для того, щоб знищити всю рослинність на площі 1 Га. Поняття про алкалоїди Алкалоїди – це група речовин (азотистих основ), які виділяються з рослин. Вони спричиняють сильну фізіологічну дію на організми тварин і людини, переважно на нервову систему, тому ця група речовин набула важливого значення в якості ліків. Багато алкалоїдів використовули ще задовго до їх відкриття у вигляді настоянок і екстрактів для лікувальних цілей. Ще раніше соки алкалоїдних рослин застосовувались як отрута (кураре, стрихнін) для нанесення на кінчики стріл. Одним із найпростіших алкалоїдів є гігрин, виділений з листків чагарника кока (Південна Америка).
2-(2-Оксопропіл)-N-метилпіролідин (гігрин) Велике значення мають піридинові алкалоїди:
Сьогодні багато алкалоїдів виділені у чистому вигляді, а для деяких із них розроблені ефективні методи одержання синтетичним шляхом. Хінолін та ізохінолін
Хінолін та ізохінолін виділяють із кам’яновугільної смоли, де вони зустрічаються разом із своїми гомологами. Синтетично хінолін одержують за реакцією Скраупа з аніліну та гліцерину у присутсності сірчаної кислоти і слабих окиснювачів.
Ізохінолін можна добути конденсацією фосгену з 2-фенілетиламіном за схемою:
Хінолін та ізохінолін є слабкими основами і утворють солі з сильними кислотами. Вступають в реакції електрофільного заміщення за участю бензенового ядра. Структурні елементи хіноліну входять у склад деяких алкалоїдів (наприклад, морфіну).
РОЗДІЛ 9. ГЕТЕРОЦИКЛІЧНІ АРОМАТИЧНІ СПОЛУКИ Гетероциклічні сполуки - речовини, що містять у молекулах цикли, у яких один або більше атомів є елементами, відмінними від вуглецю, (O, S, N, P тощо). Гетероциклічні сполуки, як правило, мають ароматичний характер. Їх класифікують: 1. За загальним числом атомів у циклі (три-, чотири-, п’ятичленні, тощо); 2. За кількістю гетероатомів (1, 2, 3 тощо); 3. За природою гетероатомів НОМЕНКЛАТУРА За номенклатурою IUPAC назви гетероциклів складаються з префікса, кореня та закінчення. Назва = префікс + корінь + суфікс. Префікс означає природу гетероатома: -O- окса, окс- -S- тіа-, ті- -N- аза-, аз- -P- фосфа-, фосф- Корінь означає розмір циклу:
Суфікс означає ступінь насиченості циклу: насичений -ідін з атомом N, - ан - без атома N; ненасичений –ін; Приклади назв гетероциклів за номенклатурою IUPAC
Азирідин Оксиран Азолідин (етиленімін) (етиленоксид) (піролідин)
Нумерація атомів у циклі починається з гетероатома. Застосовується позначення положення замісника: α,β,γ тощо.
Пірол 1,4-Дигідро- Піран (азол або азоци- піридин клопентадієн)
Нумерація атомів у конденсованих циклах починається від місця, сусіднього з місцем конденсації циклів так, щоб гетероатом отримав мінімальне значення локанта
Ізохінолін Індол (α, β-бензопірол)
Для багатьох гетероциклічних сполук широко застосовуються тривіальні назви.
|
||||
|
Последнее изменение этой страницы: 2016-08-15; просмотров: 1190; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.242.20 (0.009 с.) |

 - ір –
- ір – - -ет –
- -ет – -ол -
-ол - -ан -
-ан - -ен-
-ен-























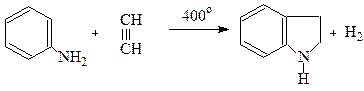








 Піридин можна розглядати як бензен, у якого один атом вуглецю замінений на азот. Оскільки електронегативність азоту вища, ніж вуглецю, він стягує на себе електронну густину і на вуглецевих атомах виникає частковий позитивний заряд.
Піридин можна розглядати як бензен, у якого один атом вуглецю замінений на азот. Оскільки електронегативність азоту вища, ніж вуглецю, він стягує на себе електронну густину і на вуглецевих атомах виникає частковий позитивний заряд.