
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Межфазная поверхность, ее силовое поле. Поверхностное натяжение как характеристика этого поляСодержание книги
Поиск на нашем сайте
На межфазной поверхности существует поле нескомпенсированных межмолекулярных сил из-за различия в составе и структуре контактирующих фаз, избыточные значения плотностей термодинамических функций, их “сгущение”. Межфазная поверхность – конечный по толщине слой, в котором свойства и термодинамические функции отличаются от таковых в объеме. Молекулы, прилегающие к поверхности по энергетическому состоянию отличны от находящихся в объеме. Для внутренних молекул равнодействующая всех межмолекулярных взаимодействий равна нулю, а для поверхностных молекул она направлена перпендикулярно поверхности внутрь фазы с большим межмолекулярным взаимодействием. Поверхностные молекулы втягиваются в глубь жидкости и возникает внутреннее давление. Следствием этого является поверхностное натяжение – важная характеристика поверхности. Существует две трактовки σ – силовая и энергетическая:
Единство энергетического и силового подходов демонстрирует опыт Дюпре: На проволочной рамке (рис. а) образуем мыльную пленку. Нижняя сторона рамки – подвижная и, если ничем не нагружена, поднимается вверх из-за стремления пленки сократиться, т. е. На рамку действует сила поверхностного натяжения Fп. Эту силу можно уравновесить грузиком весом Р = Fп. При увеличении веса груза на бесконечно малую величину происходит перемещение подвижной стороны рамки на dh (рис. б). Груз при этом совершает работу против силы Fп:
Одновременно из-за увеличения поверхности пленки возрастает поверхностная энергия:
(коэффициент 2 учитывает двусторонность пленки). Так как Таким образом, величина σ может рассматриваться не только как удельная поверхностная энергия, но и как сила, отнесенная к единице длины контура, ограничивающего поверхность. G Заметим также, что сила поверхностного натяжения Fп имеет ту же природу, что и показанная ранее равнодействующая сил, приложенных к поверхностным молекулам, но направлена не перпендикулярно поверхности, а вдоль нее (тангенциально к поверхности). Это хорошо видно из модели Дюпре. Именно такое направление силы Fп и означает стремление к уменьшению площади поверхности. 3. Что Вы знаете о структурообразовании в дисперсных системах и типах дисперсных структур? Структурообразование в дисперсных системах является результатом самопроизвольно протекающих процессов сцепления частиц, приводящих к уменьшению свободной энергии системы, например процессов коагуляции дисперсной фазы или конденсации вещества в местах контакта частиц. Развитие пространственных сеток (дисперсных структур) различных типов лежит в основе способности дисперсной системы становиться материалом с определенными механическими свойствами. Важнейшей механической характеристикой материала является его прочность Рс (Н/м2), которая определяет способность материала сопротивляться разрушению под действием внешних напряжений. Структуры глобулярного типа. Величина Рс (Рс=χр1, где χ – число контактов; р1 – прочность контактов) обуславливается совокупностью сил сцепления частиц в местах их контакта. В зависимости от характера сил, обуславливающих сцепление частиц, контакты можно условно разделить на коагуляционные и фазовые. В коагуляционных контактах взаимодействие частиц ограничивается их соприкосновением. Для структур с коагуляционными контактами характерны невысокая прочность и механическая обратимость – способность к самопроизвольному восстановлению после механического разрушения (тиксотропия). В фазовых контактах сцепление частиц обусловлено близкодействующими силами когезии. В отличие от коагуляционных фазовые контакты разрушаются необратимо. В зависимости от преобладающего типа контактов между частицами дисперсные структуры условно можно разделить на две основные группы: коагуляционные структуры и структуры с фазовыми контактами. 1. Коагуляционные структуры образуются при потере дисперсной системой агрегативной устойчивости. Коагуляционные дисперсные структуры образуются пигментами и наполнителями лаков, красок, полимеров. Характерным примером тиксотропных структур являются пространственные сетки, возникающие в дисперсиях глин при их коагуляции под действием электролитов. 2. Дисперсные структуры с фазовыми контактами образуются в самых разнообразных физико-химических условиях. Дисперсные структуры, возникающие в процессе выделения (конденсации) новой фазы из метастабильных растворов или расплавов, принято называть конденсационными. Если при этом частицы, образующие структуру, имеют ярко выраженный кристаллический характер, то такие структуры называют кристаллизационными. Примером кристаллизационной дисперсной структуры является твердение полуводного гипса при его взаимодействии с водой: CaSO4·1/2H2O + 1,5H2O = CaSO4·2H2O. Примером некристаллических конденсационных дисперсных структур являются силикаты и алюмосиликаты (силикагели и алюмосиликагели, водные и обезвоженные).
|
||||||||
|
Последнее изменение этой страницы: 2016-08-14; просмотров: 209; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.12.76.168 (0.009 с.) |

 – сила, приложенная к единице длины контура поверхности раздела фаз, действующая перпендикулярно контуру и тангенциально (вдоль) поверхности.
– сила, приложенная к единице длины контура поверхности раздела фаз, действующая перпендикулярно контуру и тангенциально (вдоль) поверхности.
 .
В обратимом процессе полезная работа максимальна и равна изменению энергий Гиббса или Гельмгольца, взятых с обратным знаком. Тогда σ можно представить в виде:
.
В обратимом процессе полезная работа максимальна и равна изменению энергий Гиббса или Гельмгольца, взятых с обратным знаком. Тогда σ можно представить в виде:
 и
и  В общем случае σ – частная производная любого термодинамического потенциала по площади межфазной поверхности.
В общем случае σ – частная производная любого термодинамического потенциала по площади межфазной поверхности.

 .
.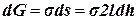
 , получаем:
, получаем: 
 .
.


