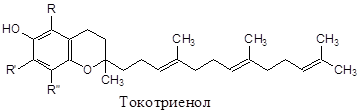Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Витаминоподобные водорастворимые веществаСодержание книги Похожие статьи вашей тематики
Поиск на нашем сайте Витаминоподобные водорастворимые вещества Витамин Р (Биофлавоноиды) Общая характеристика Суточная потребность – около 25–50 мг (точно потребность не установлена) Распространение в природе. Свежие фрукты, ягоды, особенно богата черноплодная рябина, черная смородина, яблоки, виноград, лимон, а также листья чая и плоды шиповника.
Эта группа очень разнообразна. В растениях обнаружено до 2000 флавоноидных веществ и родственных им соединений. Р-витаминными свойствами обладают антоксантины, антоцианы и катехины. В организме человека флавоноиды превращаются в фенольные кислоты. Выводятся из организма преимущественно с мочой в виде коньюгатов с глюкуроновой или серной кислотами. Биохимические функции Флавоноиды снижают проницаемость и ломкость капилляров. Р-витаминные вещества взаимодействуют с аскорбиновой кислотой, участвуя в регуляции образования коллагена соединительной ткани, препятствуют деполимеризации гиалуроновой кислоты гиалуронидазой. Тем самым они снижают проницаемость капилляров. Р-витаминные вещества активируют тканевое дыхание. Авитаминоз Авитаминоз биофлавоноидов проявляется симптомами повышенной ломкости и проницаемости капилляров, точечными кровоизлияниями и кровоточивостью десен. Применение В медицинской практике применяют Р-витаминные препараты – сумма катехинов чайного листа, флавоноидов из рябины черноплодной, а также рутин, кверцетин и гесперидин. Используют и комбинированные препараты с витамином С – аскорутин и галаскорбин. Назначают при лучевом поражении, ожоговой болезни, отравлении ядами, при пониженной свертываемости крови, при кровоточивости десен, кровоизлиянии в сетчатку глаз, ревматизме, инфекционных заболеваниях. Витамин Н (Биотин) Общая характеристика Суточная потребность – 150–200 мкг. Распространение в природе. Богаты биотином – горох, соя, цветная капуста, грибы, яичный желток, печень и др. Однако, основная потребность организма человека в биотине покрывается за счет биосинтеза его кишечными бактериями. Структура витамина и кофермента:
Метаболизм и биохимические функции Поступающий с пищей биотин освобождается с помощью протеаз кишечника от связи с белками и в свободном виде всасывается в тонком кишечнике. В крови он связывается с альбумином и поступает в ткани. Задерживается биотин главным образом в печени и почках. Выводится из организма в неизмененном виде с мочой или калом. В тканях свободный биотин связывается с ε-NH2-группой лизина, находящегося в активном центре “биотиновых” ферментов. Его коферментной формой считается N5-карбоксибиотин. Кофермент биотина способствует усвоению тканями углекислоты (точнее ионов гидрокарбоната). Карбоксибиотин участвует в синтезе пуринов (аденина и гуанина) реакция карбоксилирования, при переносе СО2, в составе пируваткарбоксилазы (см. процесс глюконеогенеза), ацетил~КоА-карбоксилазы (синтез малонил~SKoA), пропионил~КоА-карбоксилазы, а также в других многочисленных реакциях. Тем самым, биотин обеспечивает протекание глюконеогенеза, синтез жирных кислот, окисление остатков пропионовой кислоты в цикле Кребса (т.е. окисление жирных кислот с нечетным числом атомов углерода). Биотин образует специфический комплекс с токсичным белком гликопротеином – авидином (его много в белке куриного яйца) и тем самым обезвреживает его. Однако, при употреблении сырых яиц в больших количествах происходит связывание пищевого биотина и всасывание витамина прекращается. Таким способом можно вызывать биотиновую недостаточность. Авитаминоз Недостаточность биотина у человека не выявлена, но ее можно вызвать искусственно (см. выше). В медицинской практике биотиновые препараты пока широко не используют, хотя осуществляются попытки к его применению при дерматитах. 2.3. Липоевая кислота (витамин N или тиоктовая кислота) Общая характеристика Распространение в природе. Липоевая кислота поступает с пищей. Более богаты ею дрожжи, мясные продукты, молоко. Потребность в ней человека не установлена. Структура витамина. Представляет собой циклический дисульфид:
Биохимические функции Липоевая кислота, поступая в ткани, связывается ковалентно с аминогруппой лизина полипептидной цепи липоевых ферментов (например, дегидролипоилтрансацетилаза). К ним относятся полиферментные комплексы, участвующие в окислительном декарбоксилировании пирувата и α-кетоглутарата (2-оксоглутарата). В составе пируват- и α-кетоглутаратдегидрогеназных комплексов липоевая кислота участвует в окислительно-восстановительных реакциях:
Участие липоевой кислоты в процессе окислительного декарбоксилирования пировиноградной кислоты рассмотрено в теме «Обмен углеводов». Авитаминоз Недостаточность липоевой кислоты у человека не описана. Но этот витамин назначают при поражении печени, сахарном диабете, интоксикации тяжелыми металлами (за счет SH-групп связывает металлы). Считается, что липоевая кислота улучшает углеводный и энергетический обмены. Общая характеристика
Структура ПАБК. Не является витамином для человека, но служит витамином для микроорганизмов. У человека ПАБК, возможно, используется кишечными бактериями для образования фолиевой кислоты (фолацин), которая и поступает в организм. Ее применяют для восстановления нормальной микрофлоры кишечника. 2.5. Витамин В8 (Инозит) Общая характеристика Суточная потребность – 1,0–1,5 г Распространение в природе. Присутствует в пище животного и растительного происхождения. Наиболее богаты им печень, мясные продукты, мозг, яичный желток, а также хлеб, картофель, зеленый горох, грибы. Структура инозита (миоинозита). Шестиатомный циклический спирт:
Биохимические функции Биологической активностью обладает только одна из оптических форм – миоинозит. Инозит входит в состав инозитфосфатидов, содержащихся во всех тканях, но особенно много их в нервной ткани. Инозит обладает липотропным действием, т.к. препятствует накоплению триацилглицеролов в печени (предупреждает жировую инфильтрацию печени). Добавление к пище инозита препятствует жировому перерождению печени. Однако, липотропное действие инозита слабее, чем фосфатидилхолина (лецитина). Авитаминоз У человека инозитовый авитаминоз не описан. Нехватка инозита приводит к задержке роста молодняка, облысению и анемии у мышей и крыс, нарушениям нервной системы у голубей. В практике инозит используют как липотропный препарат. 2.6. Витамин В13 (Оротовая кислота) Общая характеристика Распространение. Широко распространена в животных продуктах. Структура. Оротовая кислота является предшественником при биосинтезе пиримидиновых оснований (урацила, тимина и цитозина):
Биохимические функции Биологически активная форма оротидин-5’-фосфат, который включается в синтез нуклеотидов и нуклеиновых кислот. Благодаря этому оротовая кислота стимулирует синтез белка, деление клеток, рост и развитие животных и растений. Авитаминоз Недостаточности у человека не выявлено, но повышена потребность в ней растущего организма, или отдельных тканей в период регенерации. Практическое применение В медицинской практике оротовую кислоту применяют как стимулятор роста недоношенных детей для усиления процессов кроветворения при анемиях, для повышения регенеративных процессов в пораженных органах (например, в лечении инфаркта миокарда, дистрофии мышц) и др. Витамин U (S-Метилметионин) Общая характеристика От латинского Ulcus – язва, поэтому витамин назвали антиязвенным фактором. Распространение. Содержится в сырых овощах, особенно много его в капусте. Капустный сок обладает способностью задерживать развитие экспериментальной язвы желудка. Структура. По химическому строению является метилированным производным метионина (метилметионинсульфоний хлорид):
Витамин U, как и метионин, является активным донором метильных групп, тем самым, способствуя синтезу в тканях организма холина и холинфосфатидов (лецитина), креатина и других групп веществ содержащих метильные группы. Применение Витамин U применяют для лечения язвенной болезни желудка и двенадцатиперстной кишки, гастритов. Возможно липотропное действие этого витамина. 2.8. Карнитин (Витамин Вт) Общая характеристика Суточная потребность – 500 мг. Распространение в природе. Широко распространенное вещество, особенно много содержится в мясных продуктах. Биосинтез и структура карнитина .. Биосинтез карнитина происходит в основном в печени. Сначала метилируется лизин белка, с образованием ε-N-триметиллизина. Затем укорачивается углеродная цепь лизина, за счет потери первого и второго атомов углерода и образуется γ-бутиробетаин, который в печени при участии γ-бутиробетаингидроксилазы гидроксилируется с образованием карнитина.
γ-Бутиробетаин α-Кетоглутарат Карнитин Сукцинат (ациклическая форма) (янтарная кислота)
Биохимические функции Карнитин участвует в переносе длинноцепочечных ацилов жирных кислот и ацетильных групп через липидную фазу мембран митохондрий, а возможно и других органоидов. Поэтому он оказывает выраженное влияние на процессы окисления жирных кислот и образование из них энергии, а также на использование ацетильных остатков, образующихся в митохондриях, в биохимических реакциях в цитоплазме. Карнитин может находиться в организме, как в развернутой, так и в циклической формах. Поскольку циклическая форма более жирорастворима (вследствие экранирования зарядов метильными группами), то именно в такой циклической форме карнитин способен диффундировать через липидный слой мембраны и переносить ацилы. Ацилы присоединяются к ОН-группе карнитина с образованием ацилкарнитина: Процесс обратимого переноса ацила между КоАSH и карнитином на внешней и внутренней сторонах мембраны осуществляется ферментом ацил-КоА-карнитин-трансферазой (см. схему):
Рис. 1. Схема транспорта жирных кислот через Мембрану митохондрий Имеются данные, что карнитин стимулирует внешнесекреторную функцию поджелудочной железы, оказывает положительный эффект на сперматогенез и подвижность сперматозоидов. Введение карнитина животным повышает образование энергии в дыхательной цепи митохондрий различных органов, стимулирует регенеративные процессы в пораженном миокарде и сперматогенном эпителии семенников. Авитаминоз Карнитиновая недостаточность проявляется в виде поражения мышц, что сопровождается мышечной слабостью, дистрофией и истончением мышечных волокон. Дефицит лизина в пище ухудшает обеспеченность организма карнитином. Практическое применение В медицинской практике карнитин используется для стимуляции мышечной деятельности, внешней секреции поджелудочной железы, при дистрофических процессах в миокарде. 2.9. Витамин В15 (Пангамовая кислота) Общая характеристика Суточная потребность – потребность для человека не известна. Распространение в природе. Содержится во многих продуктах питания. Химическая структура. В15 является N-диметилглициновым эфиром глюконовой кислоты. Соединение нестойкое и легко гидролизуется.
Биохимические функции. Пангамовая кислота подобно метионину служит источником подвижных метильных групп. Она участвует в биосинтезе метилированных соединений: холина, холинфосфатидов, ацетилхолина, креатина и других. Применение В медицинской практике препараты пангамовой кислоты применяют как липотропное средство при жировой инфильтрации печени, атеросклерозе и некоторых других заболеваниях. 2.10. Витамин В4 (холин) Общая характеристика Суточная потребность – 250–600 мг. Распространение в природе. Холином богаты мясо и продукты, получаемые из злаков. Частично холин образуется микрофлорой кишечника.
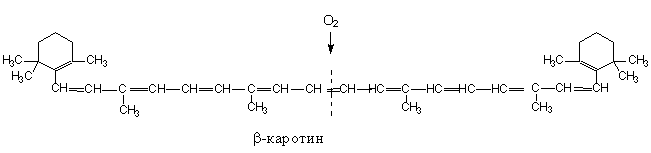
Авитаминоз У человека холиновая недостаточность не описана. У экспериментальных животных холиновая недостаточность проявляется в виде жировой инфильтрации печени и других нарушениях синтеза липидов. Применение В медицинской практике используются препараты холина для лечения поражений печени, вызванных различными заболеваниями и интоксикациями. Жирорастворимые витамины Витамин А (ретинол) Общая характеристика Суточная потребность – 1,5 мг (5000 мЕ) Распространение в природе. Продукты животного происхождения: печень рыб (трески и морского окуня), много в свиной и говяжьей печени, желтке яиц, сметане, цельном молоке. В растительных продуктах: моркови, томатах, свекле, салате содержатся каротиноиды, являющиеся провитаминами А. Поэтому частичное обеспечение витамином А происходит за счет растительных продуктов. Структура и биологическая активность формы витамина А. Витамин А – это непредельный одноатомный спирт, состоящий из β-иононого кольца и боковой цепи из двух остатков изопрена, имеющей первичную спиртовую группу. Витамин А имеет витамеры А1 и А2. Витамин А2 содержит в кольце дополнительную двойную связь (обнаружен у пресноводных рыб):
В организме ретинол (спиртовая ОН-группа в боковой цепи) превращается в ретиналь (альдегид) и ретиноевую кислоту. Происходит последовательное окисление спиртовой группы ретинола. В тканях образуются производные витамина А – ретинилпальмитат, ретинилацетат и ретинилфосфат. Витамин А и его производные в тканях находятся в транс-конфигурации, за исключением сетчатки глаза, где образуются 11-цис-ретинол и 11-цис-ретиналь. Известны три провитамина А: α-, β-, γ-каротины, отличающиеся по химическому строению и биологической активности. Наиболее активен β-каротин, который в клетках слизистой кишечника подвергается окислению по центральной двойной связи с участием фермента каротиндиоксигеназы, при этом образуется две молекулы активного ретиналя (в отличие от α- и γ-каротинов):
Метаболизм Витамин А всасывается вместе с липидами, поэтому для осуществления механизма всасывания необходимо участие желчных кислот. В слизистой оболочке кишечника ретинол образует эфиры с жирными кислотами и транспортируется в составе хиломикронов. В плазме ретинол связывается с ретинолсвязывающим белком (фракция α-глобулина) и доставляется к тканям. В сетчатке ретинол превращается в ретиналь, который входит в состав родопсина и играет важную роль в восприятии света. В печени эфиры ретинола депонируются, где часть его может превращаться в ретиналь и ретиноевую кислоту. Конъюгированная форма ретиноевой кислоты с глюкуроновой кислотой может выводиться с желчью. Биохимические функции Все формы витамина А и их эфиры регулируют следующие биохимические процессы: 1) нормальный рост и дифференцировку клеток развивающегося организма (эмбриона, растущего организма); 2) регуляцию деления и дифференцировки быстро пролиферирующих тканей: хрящевой, костной, сперматогенного эпителия и плаценты, эпителия кожи и слизистых; 3) участие в фотохимическом акте зрения. Ретиноевая кислота не принимает участия в зрительном акте и осуществлении функции размножения, т.е. нормальном развитии плаценты при беременности и созревании сперматозоидов. Однако ретиноевая кислота стимулирует рост костей и мягких тканей. Остальные формы витамина А обеспечивают все основные его биологические функции. Окончательно, механизм регуляции витамином А, процессов деления и дифференцировки клеток не выяснен. Возможно, данный процесс связан с запуском механизма репликации, а выраженное влияние на рост тканей – с регуляцией синтеза хондроитинсульфата в клетках хряща. Многие метаболические функции витаминов А в настоящее время неясны. Наиболее детально изучено участие ретиналя в акте зрения. Как известно, сетчатка человека имеет два типа клеток – палочки и колбочки. Палочки реагируют на слабое сумеречное освещение, а колбочки на дневное и обеспечивают различение цветов. Палочки содержат зрительный пигмент родопсин, а колбочки иодопсин. По своей природе эти пигменты являются сложными белками, состоящими из 11-цис-ретиналя и белка опсина. Однако, по строению родопсин и иодопсин различаются. Родопсин находится в мембранных структурах – дисках, заполняющих наружный сегмент палочки (рис. 2).
Рис. 2. Строение зрительной палочки: 1 – наружный сегмент; 2 – прилегающий сегмент с митохондриям; 3 – тело клетки и ядро; 4 – аксон
Каждый диск представляет собой замкнутый уплощенный мембранный пузырек; палочка содержит около тысячи дисков, уложенных в стопку. Диски синтезируются в прилегающем сегменте палочки и отсюда поступают в наружный сегмент. С противоположного конца наружного сегмента время от времени отделяются частицы и фагоцитируются клетками пигментного эпителия. Процесс образования новых дисков и удаления старых происходит на протяжении всей жизни. В мембранных дисках на долю родопсина приходится около 80% от всех белков мембраны. Молекулы родопсина пронизывают мембрану насквозь. В зрительном акте можно выделить три процесса: 1) фотохимическая абсорбция света; 2) фотохимическая абсорбция света пигментом, в ходе которой он изменяется; 3) регенерация исходного пигмента. Кванты света, поглощаемые родопсином (или иодопсином), вызывают фотоизомеризацию 11-цис-ретиналя в транс-ретиналь:
После этого происходит диссоциация транс-ретиналя и опсина и пигмент обесцвечивается. Поскольку пигменты встроены в мембраны светочувствительных клеток, то фотоизомеризация ретиналя приводит к местной деполяризации мембраны и возникновению электрического импульса, распространяющегося по нервному волокну. Регенерация исходного пигмента возможна прямым путем с участием ретинальизомеразы в сетчатке, но главным образом в печени. На свету в сетчатке этот процесс протекает медленно. В темноте регенерация родопсина максимальна, и протекает через образование транс-ретинола, цис-ретинола и 11-цис-ретинола. Отсутствие регенерации родопсина приводит к слепоте в ночное время. Авитаминоз Раннее проявление – это нарушение темновой адаптации, задержка роста в молодом возрасте, фолликулярный гиперкератоз, избыточное ороговение кожи, вызванное задержкой смены эпителия, сухость слизистых (как следствие замедленного обновления эпителия), ксерофтальмия (сухость конъюнктивы глаз), помутнение роговицы и ее размягчение (кератомаляция), также нарушение функции размножения (оплодотворяющей активности сперматозоидов). Витамин Е (токоферол) Общая характеристика Суточная потребность –20–50 мг. Распространение в природе. Источником витамина Е для человека служат растительные масла: подсолнечное, кукурузное, хлопковое, оливковое. Особенно высоко его содержание в масле, полученном из зародышей пшеницы. Продукты животного происхождения, в том числе молочные, бедны токоферолами. Химическая природа. К витамину Е относятся метильные производные токола и токотриенолы. Витамин Е: α-, β-, γ- и δ-токоферолы и токотриенолы. Самый активный α-токоферол.
Для всасывания пищевого витамина Е необходимо присутствие липидов и желчных кислот. Всасывание происходит в тонком кишечнике путем простой диффузии, затем в составе хиломикронов они транспортируются через лимфатическую систему в кровь и из состава липопротеинов крови (хиломикронов) поступают в органы и ткани. В их клетках токоферолы включаются в состав липидов мембран, где они концентрируются. Наибольшее количество витамина Е в организме содержится в жировой ткани, печени и скелетных мышцах. Не всосавшийся токоферол выводится с калом в виде токофероловой кислоты и ее водорастворимых глюкуронидов – с мочой. Биохимические функции Токоферол регулирует интенсивность свободнорадикальных реакций окисления в живых клетках, поскольку препятствует развитию цепных неуправляемых реакций перекисного окисления полиненасыщенных жирных кислот (липидов и фосфолипидов) в биологических мембранах. По своему механизму действия токоферол является биологическим антиоксидантом, благодаря чему обеспечивает стабильность биологических мембран клеток организма. Существует тесная связь между токоферолом и селеном в регуляции перекисного окисления липидов (ПОЛ), поскольку селен является кофактором глутатионпероксидазы, инактивирующей гидропероксиды липидов. Антиоксидантное действие витамина Е обусловлено тем, что токоферол способен переносить свой фенольный атом водорода на пероксидный радикал:
ROO* + Ток-ОН → ROOH + Ток-О*.
ROO* + Ток-О* → ROOH + Нерадикальный продукт окисления витамина Е.
Таким образом, токоферол останавливает реакцию свободно-радикального окисления полиненасыщенных жирных кислот и сам превращается в продукт нерадикального типа (механизм перекисного окисления липидов см. тему «Биологическое окисление»). Кроме того, токоферол повышает биологическую активность витамина А, защищая его ненасыщенную боковую цепь от перекисного окисления. Возможно, имеются и другие стороны действия токоферолов, но они пока не раскрыты. Авитаминоз Гиповитаминоз Е у человека почти не встречается. Лишь у недоношенных детей встречаются признаки гиповитаминоза, приводящие к гемолитической анемии (из-за низкой устойчивости мембран эритроцитов и их распада). Патология мембран тканей при гиповитаминозе Е, очевидно, служит причиной разнообразия симптомов заболевания: склонность эритроцитов к пероксидному гемолизу, атрофия семенников, рассасывание плаценты и плода при беременности, мышечная дистрофия, а также потеря внутриклеточных азотистых компонентов и белков мышц, некроз печени, размягчение участков мозга, особенно мозжечка. Практическое применение Препараты токоферола используют как антиоксиданты при различных патологических состояниях: для профилактики бесплодия, при заболеваниях печени, инфаркте миокарда, при ожогах, лучевом поражении и т.д. 3.3. Витамин D3 (кальциферол) Общая характеристика Суточная потребность – для детей от 12 до 25 мкг (500–1000 МЕ), для взрослых 40 мкг. Распространение в природе. Содержится в продуктах животного происхождения (в печени, сливочном масле, молоке, дрожжах и растительном масле). Наиболее богата витамином D печень рыб. Рыбий жир используется для профилактики и лечения D-витаминной недостаточности. Структура витамина и его биологически активные формы. По химической природе витамины D – стерины. Существует несколько витамеров витамина D: эргокальциферол – витамин D2, холекальциферол – D3 и дигидроэргокальциферол – D4.
 При облучении УФ светом витамин D2 образуется из растительного предшественника (провитамина D) – эргостерина, а витамин D3 – из 7-дегидрохолестерина, синтезирующегося из холестерола в коже человека и животных. Витамин D3 биологически более активен: При облучении УФ светом витамин D2 образуется из растительного предшественника (провитамина D) – эргостерина, а витамин D3 – из 7-дегидрохолестерина, синтезирующегося из холестерола в коже человека и животных. Витамин D3 биологически более активен:

В природе существуют и менее активные формы витамина D – D4, D5, D6, D7. Однако, ни эрго-, ни холекальциферолы биологически не активны. Биологически активные формы образуются в ходе метаболизма. Пищевые кальциферолы всасываются в тонком кишечнике в присутствии липидов и желчных кислот и в составе хиломикронов по лимфатической системе поступают в кровь, а далее в печень. Сюда же с кровью поступает из кожи эндогенный холекальциферол (D3) (см. схему метаболизма витамина D3). 3.3.2. Метаболизм витамина Д3 в печени и почках Метаболизм витамина D связан с образованием биологически активных форм (рис.3). Специфические гидроксилазы печени и почек, которые катализируют эти реакции, активируются паратгормоном (паратиреоидный гормон или паратирин), который вырабатывается паращитовидной железой.
Рис. 3. Схема метаболизма витамина D3 в печени и почках 3.3.3. Биохимические функции 1,25-гидроксикальциферола (кальцитриола) Органы мишени кальцитриола – тонкий кишечник, кости и почки, на уровне которых он регулирует обмен кальция и фосфора в организме. Эта регуляция основана, главным образом, на трех процессах и направлена на поддержание уровня кальция в крови (в норме концентрация кальция в крови 2,29–2,99 ммоль/л или 9–11 мг/100 мл): 1) транспорт ионов кальция и фосфата через эпителий слизистой тонкого кишечника; 2) мобилизация кальция из костной ткани (это наблюдается при снижении содержания кальция в крови); 3) реабсорбция кальция и фосфора в почечных канальцах. Подобно другим стероидным гормонам (витамин D обладает гормональным эффектом) кальцитриол взаимодействует с хроматином ядра, изменяя скорость синтеза определенных белков, участвующих в связывании и всасывании ионов Са2+ в тонком кишечнике. Кальцитриол индуцирует образование в клетках эпителия кишечника кальций связывающего белка и белковых компонентов кальций зависимой АТФ-азы (Са2+-АТФ-азы). По-видимому, подобная стимуляция витамином D Са2+-АТФ-азы мембран почек приводит к реабсорбции в них ионов кальция (т.е. сохранению кальция в крови). Однако еще не выяснены механизмы участия витамина D в трансмембранном переносе фосфата в кишечнике и почках и мобилизации кальция из костной ткани.
Регуляция механизмов поддержания уровня ионов кальция в крови. В данном процессе паратиреоидный гормон и кальцитриол действуют как синергисты. Паратиреоидный гормон реализует свой гормональный эффект на фосфорно-кальциевый обмен опосредовано через активацию синтеза кальцитриола из витамина D3 (он активирует гидроксилазы в печени и почках). В свою очередь стимуляция синтеза паратиреоидного гормона происходит в ответ на снижение концентрации Са2+ в крови (рис. 4): Рис. 4. Схема регуляции механизмов поддержания уровня кальция в крови
Недостаточность витамина D При недостаточности витамина D у детей развивается рахит. Основной признак этой болезни – нарушение минерализации растущих костей. Вследствие этого кости не имеют нормальной жесткости и у детей, страдающих рахитом, наблюдаются различные деформации скелета – выгнутые наружу голени, вывернутые внутрь колени, четки на ребрах, птичья грудь и т.д. Рахит обычно излечивается витамином D, но есть такие формы, которые не поддаются такому лечению. Они, по-видимому, связаны с нарушением превращения витамина D3 в организме в кальцитриол. Причина – генетически обусловленное нарушение синтеза ферментов – гидроксилаз в печени и почках, рецепторов для связывания паратиреоидного гормона на поверхности клеточных мембран тканей мишеней и др. Продолжительное поступление избыточного количества витамина D (гипервитаминоз) приводит к деминерализации костей и переломам, повышению концентрации кальция в крови и его отложению в мягких тканях, образованию камней в мочевых путях. 3.4. Витамин К (Нафтохинон) Общая характеристика Суточная потребность – 2 мг. Распространение в природе. В зеленых хлоропластах растительных продуктов – капусты, шпината, в корнеплодах и фруктах. В животных продуктах – в печени. Кроме того, витамин К синтезируется бактериальными ферментами тонкого кишечника. Химическая природа и биологически активные формы витамина К. Витамин К представляет собой хинон с боковой изопреноидной цепью. Существует две формы нафтохинонов: филлохиноны (витамины К1–ряда) и менахиноны (витамины К2–ряда).
Филлохиноны и их производные содержатся в растениях и поступают с пищей, а менахиноны образуются в кишечнике или в ходе метаболизма нафтохинонов в тканях организма. Синтетические препараты витамина К – менадион, викасол и синкавит. В организме из них образуются активные менахиноны.
Для всасывания пищевого витамина К в тонком кишечнике необходимы липиды и желчные кислоты. Транспортируется в кровь хиломикронами. Накапливается в печени, селезенке и сердце. Биохимические функции Витамин К регулирует в организме процесс свертывания крови путем участия в образовании компонентов ее свертывающей системы: фактора (II) – протромбина, фактора (VII) – проконвертина, фактора (IX) – фактор Кристмаса и фактор (X) – фактор Стюарта. Витамин К участвует в превращении препротромбина в протромбин. Этот процесс происходит в печени. Витамин К в составе кофактора микросомальной карбоксилазы стимулирует γ-карбоксилирование остатков глутаминовой кислоты в пептидных цепях препротромбина и других факторов свертывающей системы крови (рис. 5).
Рис. 5. Пример посттрансляционной модификации белка
Реакции в которых участвуют белковые факторы II, VII, IX, X, активируются ионами Са2+ и фосфолипидами. Радикалы γ-карбоксиглутаминовой кислоты образуют центры связывания Са2+ на этих белках. По-видимому, перечисленные факторы, а также факторы V’ и VIII’ прикрепляются к бислойным фосфолипидам мембраны и друг к другу при участии ионов Са2+, и в таких комплексах происходит активация факторов II, VII, IX и X. Ион Са2+ активирует также и некоторые другие реакции свертывания. Декальцинированная кровь не свертывается. Авитаминоз Гиповитаминоз, вызванный в эксперименте у животных, проявляется повышенной кровоточивостью, подкожными и внутренними кровоизлияниями. Это связано с тем, что в отсутствие витамина К образуются факторы II, VII, IX и X, не содержащие γ-глутамильных остатков. Такие проферменты не могут превращаться в активные ферменты, т.к. не способны связывать Са2+. Препараты группы кумарина ингибируют витамин-К-зависимое карбоксилирование остатков глутаминовой кислоты, приводящее к образованию γ-карбоксиглутаминовой кислоты в N-концевой части молекул факторов II, VII, IX и X. Таким образом, введение кумарина (дикумарола) вызывает такие же последствия, как недостаточность витамина К. Убихинон (коэнзим Q) Общая характеристика Распространение в природе – много убихинона содержится в мембранах митохондрий, эндоплазматического ретикулума и ядер клеток.
Относится к липофильным витаминоподобным веществам. Синтезируется в тканях человека. Источником его образования служит мевалоновая кислота и продукт обмена фенилаланина и тирозина: Мевалоновая кислота
Источником для синтеза мевалоновой кислоты служит ацетил коэнзим А. Признаки недостаточности убихинона для человека не описаны, но при некоторых состояниях отмечается повышенная потребность в нем. Потребность в убихиноне для человека не известна. Убихинон относится к ряду хиноновых коферментов. Его аналог пластохинон, содержится в растительных клетках. Строение. По химическому строению убихинон представляет собой хинон с боковой изопреноидной цепью. Наиболее часто встречаются у
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-06-29; просмотров: 645; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.214 (0.012 с.) |

 Химическая природа. Флавоноиды (Р-витаминные вещества)представляют собой растительные полифенольные соединения. Одним из первых был выделен рутин из кожуры лимона (см. структурную формулу).
Химическая природа. Флавоноиды (Р-витаминные вещества)представляют собой растительные полифенольные соединения. Одним из первых был выделен рутин из кожуры лимона (см. структурную формулу).


 Пара-аминобензойная кислота (ПАБК) содержится практически во всех продуктах питания. Наиболее богаты ею печень, молоко, дрожжи.
Пара-аминобензойная кислота (ПАБК) содержится практически во всех продуктах питания. Наиболее богаты ею печень, молоко, дрожжи.




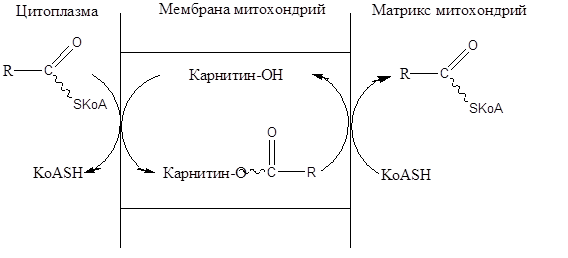

 Химическое строение. По химической природе это производное амина – гидроксид-(2-гидроксиэтил)-триметиламмония.
Химическое строение. По химической природе это производное амина – гидроксид-(2-гидроксиэтил)-триметиламмония.