
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Средней изобарной теплоёмкости воздухаСодержание книги
Поиск на нашем сайте
Методика выполнения опытов следующая: – после ознакомления с установкой измеряем температуру воздуха на входе в калорифер. Для этого включаем установку и, не включая нагреватель калорифера, ожидаем установления постоянства температуры воздуха на выходе из калорифера (измеряется термометром t 2). В начале опыта эта температура будет быстро увеличиваться вследствие нагрева воздуха при его сжатии в вентиляторе. Со временем температура стабилизируется, т.е. установится первый стационарный режим работы установки. Эту температуру принимаем в качестве начальной температуры воздуха, нагнетаемого в калорифер (t 1). Записываем это значение в соответствующую колонку таблицы опытных данных; – подаём на нагреватель калорифера при помощи автотрансформатора напряжение 90-120 В. Ожидаем установления постоянства температуры воздуха t 2 на выходе из калорифера, то есть второго стационарного режима; – при непосредственном проведении опыта одновременно измеряем и записываем значение температуры воздуха на выходе из калориметра t 2 и показания газового расходомера (две цифры до запятой и две после по его шкале) в начале и конце опыта (через 180 сек.); – записываем в таблицу 6.2 показания счетчика и усреднённое значение температуры воздуха после калориметра (t 2) (полусумма соответствующих значений в начале и конце опыта), а также атмосферное давление. Таблица 6.2 Значения величин, измеряемых в опыте
Обработка результатов измерений: – рассчитываем значение средней объемной изобарной теплоемкости воздуха в заданном интервале температур(t 1,…, t 2) в кДж/(нм3 ·к)
где Q = U · I · x ·10-3, кВт (то есть кДж/с) − тепловая нагрузка калорифера в единицу времени (количество теплоты, выделяющейся в проводнике нагревателя при прохождении тока); х = 0,87 − доля теплоты, идущей на нагрев воздуха;
τ − продолжительность опыта (обычно 180 сек.). – рассчитываем значение средней массовой изобарной теплоемкости воздуха в заданном интервале температур (t 2- t 1) в кДж/(нм3·К)
где ρн = р 0/ RT 0, кг/нм3 − плотность воздуха при нормальных условиях (р 0 подставляется в Па и Т 0 − в Кельвинах; R = 287,1 Дж/(кг·К)) – рассчитываем опытное значение средней мольной теплоемкости воздуха в заданном интервале температур (t 1… t 2) ср, кДж/(кмоль·К)
где μ в =28,96 − кажущаяся молекулярная масса воздуха, кг/кМоль. – рассчитываем табличное значение средней мольной изобарной теплоемкости воздуха в интервале температур проведения опыта (t 1… t 2), ккал/(кмоль·К) по уравнению
где t ср = (t 1 + t 2)/2 − среднее значение температуры воздуха в опыте. – определяем относительную погрешность опытного значения средней мольной изобарной теплоемкости воздуха по сравнению с расчётным значением
Перед сопоставлением необходимо согласовать размерности опытного и расчётного значений ср (то есть. учесть, что 1 ккал = 4,1868 кДж).
Контрольные вопросы 1. Дайте математическое и физическое определения понятиям «истинная и средняя удельные теплоёмкости вещества». 2. Значение какой теплоёмкости (истинной или средней) можно рассчитать на основании измеряемых в лабораторной работе величин? 3. Какие величины, какими приборами и с какой целью измеряются в данной лабораторной работе? 4. Определите понятие «нормальные условия». Что означает величина с размерностью нм 3? 5. Дайте определение понятиям «функция состояния и функция процесса». Какой функцией является теплоёмкость? 6. В чем проявляется двойственность физической сущности теплоёмкости с точки зрения основных понятий и определений термодинамики? 7. Как соотносятся значения массовой, объемной и мольной теплоёмкостей? Каковы их размерности в системе СИ? 8. Чем отличаются понятия «теплоёмкость тела» и «удельная теплоёмкость вещества» и как они связаны? 9. Чему равны удельные теплоёмкости веществ в изотермическом и адиабатном (изоэнтропном) процессах? 10. Геометрический смысл истинной и средней теплоёмкостей в координатах T,s? Поясните два свойства диаграммы T,s? 11. Запишите соотношение, связывающее значения изобарной и изохорной теплоёмкостей идеального газа. 12. От скольких параметров зависят теплоёмкости идеального и реального газов? Перечислите эти параметры. 13. Запишите соотношения для расчёта изохорной и изобарной теплоёмкостей идеального газа по упрощенной молекулярно-кинетичекой теории. 14. Запишите соотношение, используемое для пересчёта измеряемого в опыте расхода воздуха в нм 3. 15. Запишите уравнение для расчета теплоты процесса с использованием средних значений изобарной теплоёмкости идеального газа.
Лабораторная работа № 3 посвящена исследованию зависимости давления насыщенного пара от температуры. При выполнении этой работы надо четко уяснить следующее: 1. Температура кипения жидкости (температура парообразования) зависит от давления, под которым находится жидкость. При повышении давления эта температура увеличивается. 2. Исследуемая зависимость графически изображается кривой, начинающейся в тройной точке и оканчивающейся в критической точке. Эта кривая называется кривой парообразования (иногда кривой упругости). В других координатах (p,v; T,s; h,s и др.) кривая парообразования расслаивается, образуя две ветви: насыщенной (кипящей) жидкости и насыщенного (сухого) пара, которые плавно сопрягаются в критической точке. Эти ветви часто называют левой и правой пограничными кривыми соответственно. Критическая точка – особая точка на термодинамической поверхности веществ: при давлении, превышающем критическое р к, обычный фазовый переход жидкость-пар (при р = idem и Т = idem с одновременным сосуществованием двух фаз) не наблюдается, а имеет место перманентный (непрерывный) переход идкого вещества в газообразное состояние. Соответственно при изотермическом сжатии газа при Т > Т крвещество остается в гомогенном состоянии без расслоения на жидкость и пар. Состояние вещества при Т > Т кри v < v кр называется сильно сжатым газом или флюидом. Политропным процессом расширения с показателем п >1 флюид можно непрерывно превратить в жидкость. Пар это такое газообразное состояние вещества, которое можно изотермическим сжатием превратить в жидкость. Газ изотермическим сжатием превращается в флюид Снизу кривая упругости ограничена тройной точкой Т тр (рис. 6.4). Здесь в термодинамическом равновесии находятся три фазы (твердая, жидкая и парообразная). Из этой точки выходят три кривые: парообразования, затвердевания (плавления) и сублимации. В тройной точке значения температуры и давления на кривых парообразования и затвердевания являются минимальными, а на кривой сублимации − максимальными.
Рис. 6.4. Фазовая диаграмма вещества кривые: парообразования 1; затвердевания (плавления) 2; сублимации (возгонки) 3; состояния вещества: твердое Т; жидкое Ж; парообразное П; точки: Ттр– тройная; К – критическая При давлениях, меньших давления в тройной точке р тр, возможен изобарно-изотермический процесс фазового перехода вещества из твердого (кристаллического) в парообразное состояние. Этот процесс называется сублимацией или возгонкой. В интервале давлений от р тр до р кр при изобарном процессе перехода вещества из твёрдого в парообразное состояние имеют место два фазовых перехода. Вначале происходит плавление: переход из твердого состояния в жидкое, а затем − парообразование: превращение из жидкого в парообразное состояние. При р>р кр при этом условии наблюдается один фазовый переход − плавление: при дальнейшем изобарном подводе теплоты происходит перманентное превращение жидкости в газообразное состояние. Диаграмма р,Т называется фазовой диаграммой. Любая точка на этой диаграмме вне линий фазовых переходов соответствует одному из трех фазовых состояний вещества − твердому, жидкому либо парообразному (газообразному). Точки на линиях фазовых переходов (кривые 1, 2, 3) характеризуют состояния сосуществующих фаз (жидкости и пара, твердого тела и жидкости (флюида), твердого тела и пара, соответственно). 3. Важнейшей характеристикой веществ как рабочих тел энергетических и холодильных установок является так называемая температура нормального кипения (t н.к.). Это температура кипения (парообразования) вещества при нормальном атмосферном давлении (760 мм рт. ст.или 1,01325 бар). В зависимости от значений t н.к различают высококипящие (t н.к > 0 ° С) и низкокипящие (t н.к < 0 ° С) вещества. Низкокипящие вещества (аммиак, фреоны) используются в качестве рабочих тел холодильных установок − хладагентов, а высококипящие (вода, ртуть) − в качестве рабочих тел энергетических установок. В зависимости от температуры, которую необходимо поддерживать в охлаждаемом помещении (рефрижераторном трюме) выбирают хладагент из условия, чтобы фактическое давление кипения хладагента при температуре в трюме было несколько выше атмосферного, чтобы исключить подсос воздуха в систему хладагента холодильной машины. На рис. 6.5 в качестве иллюстрации совместно условно показаны кривые парообразования ряда хладагентов.
Рис. 6.5. Условное относительное положение кривых парообразования хладагентов и их нормальные температуры кипения: 1 − R22; 2 − NH3; 3 − R12 Описание лабораторной установки В установку (рис. 6.6) входят: – термостат 1, заполненный термостатирующей жидкостью (водой), служащий для нагрева исследуемого вещества – ацетона, находящегося в баллоне 4; – мешалка 2 для выравнивания температуры воды по объёму термостата; – термометр 3, измеряющий температуру воды и, следовательно, ацетона; – баллон 4 с ацетоном, соединенный капилляром с U-образным мановакуумметром 5.
Рис.6.6. Схема установки для исследования зависимости температуры кипения (насыщения) низкокипящих веществ от давления
Методика выполнения опытов: – после ознакомления с лабораторной установкой определяем положение менисков рабочей жидкости (воды) в правом и левом коленах мановакуумметра 5 и измеряем начальную температуру воды в калориметре термометром 3 (термометр не вынимать из гнезда!); – включаем установку (нагреватель и мешалку) и через каждые (3-4) °С определяем и записываем в табл. 6.3, положение менисков жидкости в правом и левом коленах мановакуумметра; Возможен вариант, когда давление исследуемого пара в баллоне 4 ниже атмосферного (мениск жидкости в колене мановакуумметра, соединенном с баллоном 4, выше, чем в колене, соединенном с атмосферой). Поэтому при заполнении таблицы измерений необходимо в графе примечание записывать, какое давление показывает мановакуумметр. При выполнении лабораторной работы надо также учитывать, что шкала мановакуумметра имеет «0» в средней части, то есть показания левого колена, соединённого с баллоном 4, ниже «0» будут отрицательными, а также то, что атмосферное давление измеряется барометром в мм рт. ст., а мановакуумметр заправлен водой. Поэтому для расчета абсолютного давления насыщения рs, показания мановакуумметра надо делить на 13,6 (1 мм рт. ст. = 13,6 мм вод. ст.) Таблица 6.3 Измеренные и рассчитанные величины
После расчёта значений рs необходимо построить график зависимости рs = ƒ(ts). Поскольку в лабораторной работе исследуется малый участок кривой парообразования, начальная точка координат должна соответствовать минимальной температуре (ось абсцисс) и минимальному давлению (ось ординат). Через полученные опытные точки проводим усредняющую кривую с учетом погрешности измерения температуры и давления в опыте.
Контрольные вопросы
1. Как называется кривая зависимости ps = f(ts)? Изобразите её условно в координатах р, Т полностью с указанием других линий фазовых переходов. Перечислите линии фазовых переходов, охарактеризуйте физические свойства веществ в различных областях фазовой диаграммы. 2. Изобразите пограничную кривую реального газа в координатах p, t, p, v и T, v. Как называется диаграмма p, t? 3. Какие приборы и оборудование используются в лабораторной установке для определения зависимости ps = f(ts)? Объясните их назначение и принцип действия. 4. Сколько независимых параметров необходимо задать для указания состояния насыщенного пара либо кипящей жидкости? Какими параметрами чаще всего задаётся это состояние? 5. Каким фазовым состояниям вещества соответствуют правая и левая ветви пограничной кривой? Как изменяются термодинамические свойства веществ в этих состояниях с ростом температуры и давления? 6. Как называется процесс непосредственного превращения вещества из твердого состояния в парообразное состояние? Где он встречается на практике? 7. Изобразите пограничную кривую жидкость-пар вещества в координатах T, s и h, s. Охарактеризуйте особенности его состояния в характерных точках на этой кривой. 8. Определите понятие «нормальная температура кипения». Как подразделяются вещества в зависимости от их значения такой температуры? 9. Какое практическое значение имеет зависимость давления насыщенного пара от температуры? 10. Какие явления имеют место при изобарном переходе вещества из твердого состояния в парообразное, если ркр> рзад > ртр? 11. Какое явление имеет место при изобарном переходе вещества из твердого состояния в парообразное, если рзад < ртр? 12. Как вещество, находящееся в твердом состоянии при р> ртр, превратить в пар с минимальным числом фазовых переходов? 13. Изобразите в координатах p, v и T, s изотермический процесс превращения жидкости в пар. Какие фазовые превращения при этом наблюдаются? 14. Изобразите в координатах p, v и T, s изобарный процесс превращения жидкости в пар. Какие состояния при этом наблюдаются? 16. Какой процесс происходит в баллоне с ацетоном после окончания опытов. Ваш ответ изобразите на диаграммах p, T и p, v.
Лабораторная работа № 4 посвящена определению теплоты парообразования воды. При её выполнении надо знать следующее: Теплотой парообразования называется количество теплоты, необходимое для превращения одного килограмма кипящей жидкости в насыщенный пар при постоянном давлении. Подвод при этом теплоты не повышает температуру, а вызывает дисгрегацию, то есть увеличение расстояния между молекулами при преобразовании жидкости в пар. Определив массу пара (конденсата) и количество теплоты, затраченное на его образование, рассчитывают теплоту парообразования воды в условиях опыта. Для определения массы пара (конденсата), образующегося за время опыта, достаточно взвесить змеевик со сборником конденсата в начале и конце опыта. Для определения количества подведенной теплоты необходимо измерить температуру воды в калориметре также в начале и конце опыта. Тогда значение теплоты парообразования r рассчитывается из уравнения теплового баланса
где ср, в = 4,1868 кДж/(кг·К) − удельная изобарная теплоёмкость воды; М в − масса воды, находящейся в калориметре (обычно 5 кг); W − водяной эквивалент калориметра, кДж/К. t 1, t 2 − начальная и конечная температура воды в калориметре, °С; М к = (М 2 –М 1 ) − масса образовавшегося пара (конденсата) во время опыта, кг; М 1, М 2 − масса змеевика в начале и конце опыта, кг; ts − температура насыщения (кипения) воды при давлении опыта, °С. Водяной эквивалент калориметра − количество теплоты, необходимое для нагрева на 1 К его смачиваемых частей: корпуса, мешалки, змеевика со сборником конденсата и термометра. Он определен ранее и равен 5,4 кДж/К. Температура насыщения и табличная теплота парообразования при давлении опыта определяются интерполяцией соответствующих величин из таблиц свойств насыщенных воды и водяного пара [3] в зависимости от атмосферного давления в момент проведения опыта. Началом опыта является момент подключения змеевика-конденсатора к колбе-кипятильнику, в котором кипит вода, а концом − момент выравнивания температуры конденсата (змеевика) и температуры воды в калориметре. В этот момент температура воды в калориметре достигает максимальное значение. В уравнении (6.7) левая часть − теплота, полученная водой и калориметром за время опыта. Первое слагаемое правой части − теплота, выделившаяся при конденсации М кг пара: (М к· r), а второе − теплота, отданная конденсатом при его охлаждении от температуры конденсации (ts), до температуры, установившейся в калориметре в конце опыта (t 2). Процессы образования (1-2-3) и конденсации (3-2) пара, а также охлаждения конденсата до конечной температуры в опыте (2-К) представлены на диаграмме T,s (рис. 6.7). Площадь (c-2-3-d-с) соответствует теплоте парообразования r в условиях опыта; площадь (a-1-2-c-а) – теплоте, затрачиваемой на нагрев воды от начальной (комнатной) температуры до температуры кипения (насыщения) ts; площадь (c-2-K-b-с) – теплоте, отдаваемой конденсатом при его охлаждении от температуры конденсации ts до конечной температуры воды в калориметре t 2.
Рис. 6.7. Изображение процессов образования и конденсации пара
Описание экспериментальной установки Экспериментальная установка для определения теплоты парообразования воды (рис. 6.8) состоит из: электронагревателя 1 (электроплитки), кипятильника 2 (стеклянной колбы), паропровода 3 (соединительной трубки), конденсатора 4 (змеевика со сборником конденсата), калориметра 5 (ёмкости с двойными стенками, между которых находится изоляционный материал), мешалки с электрическим приводом 6, термометра 7, экрана 8, препятствующего передаче теплоты лучеиспускания от горячей плитки и колбы к наружной поверхности калориметра. В лабораторную установку также входят электронные весы, точностьвзвешивания которых 0,01 грамма. Методика выполнения опыта
Убедившись, что змеевик со сборником конденсата пустой, взвешиваем его на электронных весах. Перед каждым взвешиванием надо протирать змеевик насухо ветошью.
Рис.6.8. Схема установки для определения теплоты парообразования воды
Помещаем змеевик в калориметр; плотно закрываем крышки калориметра и замеряем начальную температуру воды в калориметре с помощью термометра. Как отмечено ранее, термометр не следует полностью вынимать из калориметра, так как он установлен стационарно. Включаем электронагреватель кипятильника (электроплитку). После достижения устойчивого кипения воды в кипятильнике соединяем его паропроводом со змеевиком-конденсатором и включаем электропривод мешалки; После повышения температуры воды в калориметре на (3-5) °С отсоединяем змеевик-конденсатор от кипятильника, выключаем электрическую плитку и продолжаем непрерывно наблюдать за изменением этой температуры при работающей мешалке; После окончания процесса повышения температуры воды в калориметре (определяется по показаниям термометра и изменению температуры змеевика-испарителя на ощупь), замеряем максимальную температуру воды и останавливаем мешалку. Взвешиваем змеевик-конденсатор и определяем атмосферное давление по имеющемуся в лаборатории барометру. Измеряемые величины записываем в таблицу наблюдений (табл. 6.4). Таблица 6.4 Измеренные в опыте величины
Рассчитываемые по измеренным в опыте параметрам величины записываем в таблицу 6.5 Таблица 6.5 Рассчитываемые в опыте величины
Контрольные вопросы 1. Как устроена лабораторная установка? Какие величины измеряются в этой работе и с какой целью? 2. На что расходуется теплота, подводимая к воде калориметра? 3. Что такое водяной эквивалент калориметра? Зависит ли он от количества воды, залитой в калориметр? 4. Какие величины входят в формулу для расчета теплоты парообразования воды в данной лабораторной работе? 5. Дайте определение понятию «теплота парообразования». Какова размерность теплоты парообразования? 6. Как зависит теплота парообразования от температуры и давления? Изобразите эти зависимости в координатах r, T и r, p. 7. Когда и каким прибором измеряется максимальная температура воды в калориметре? 8. От чего зависит температура конденсата, образующегося в змеевике-конденсаторе? Как она определяется в опыте? 9. От чего зависит и как определяется табличное значение теплоты парообразования (r табл)? Запишите соотношения для расчета теплоты парообразования через энтальпию и энтропию. 10. Покажите на диаграмме T, s теплоту, подводимую к воде калориметра за счет охлаждения конденсата после отключения паропровода и конденсации остатков пара. Из какого уравнения можно рассчитать эту теплоту? 11. Покажите на диаграмме T, s теплоту парообразования. Запишите соотношения для её расчета через значения энтальпии и энтропии. 12. Почему температура воды в калориметре продолжает повышаться после прекращения подачи пара в змеевик-конденсатор? 13. Можно ли на данной лабораторной установке определить теплоту парообразования фреона R-22 и аммиака NH3 при атмосферном давлении? 14. Как изменятся опытное и табличное значения теплоты парообразования воды, если атмосферное давление повысится? 15. Равны ли значения теплоты парообразования у разных веществ при нормальном атмосферном давлении, чем это объясняется? 16. Изобразите на диаграмме T, s процессы, происходящие в испарителе (колбе) с момента включения электроплитки до выхода установки на режим проведения опыта. 17. Изобразите на диаграмме T, s процессы, происходящие в конденсаторе-змеевике после отключения от него испарителя и до его взвешивания.
Лабораторная работа № 5 посвящена исследованию теплоотдачи трубы при свободной конвекции. Работа относится к дисциплине «Основы тепломассообмена», но рассматривается в данном пособии, поскольку при её выполнении студенты осваивают методику измерения температуры с помощью термопар. Свободной (естественной) конвективной теплоотдачей называется процесс отдачи теплоты от стенки (к стенке) при движении теплоносителя относительно неё, обусловливаемом разностью плотностей нагретых и холодных объемов теплоносителя. Количество отдаваемой стенкой теплоты зависит от разности температур стенки и теплоносителя и скорости движения теплоносителя относительно стенки. Эта скорость при естественной конвекции прямо пропорциональна разности температур стенки и теплоносителя. Интенсивность теплоотдачи зависит также от теплофизических свойств теплоносителя, формы теплоотдающей (тепловоспринимающей) поверхности, ее пространственного положения и от ряда других факторов. Количество теплоты, отдаваемое (воспринимаемое) поверхностью стенки, рассчитывается по уравнению Ньютона-Рихмана
Q к = α· F Δ t,
где α − коэффициент теплоотдачи, Вт/(м2К); F − поверхность стенки, м2; Δ t = t ст - – t т − разность температур стенки и теплоносителя. В работе исследуется теплоотдача от поверхности трубы к воздуху помещения лаборатории при свободной конвекции. В частности, исследуется зависимость коэффициента теплоотдачи трубы α при различных её пространственных положениях (горизонтальном, вертикальном и под 45 ° к горизонтали).
Описание экспериментальной установки В установку, схема которой приведена на рис. 6.9, входят: труба 1, подогреваемая вмонтированным во внутрь электрическим нагревателем (электроспиралью) 2. Потребляемая нагревателем мощность регулируется при помощи лабораторного автотрансформатора (ЛАТР-1) 3 и рассчитывается по показаниям вольтметра 4 и амперметра 5. Для измерения температуры наружной поверхности трубы на ней закреплены пять термопар 6, подсоединяемых поочередно при помощи переключателя 7 к зеркальному гальванометру 8. Гальванометр отградуирован в милливольтах (мВ), поэтому для определения температуры в градусах Цельсия (°С) на лабораторном стенде имеется график перевода мВ в °С. Температура воздуха в лаборатории измеряется при помощи обычного ртутного термометра. Температура стен лаборатории измеряется дистанционным лазерным термометром. Размеры трубы лабораторной установки: диаметр 35 мм, длина 1 м.
Рис. 6.9. Схема установки для исследования теплоотдачи трубы При свободной конвекции Методика проведения опыта – последовательно устанавливаем трубу в одно из трёх положений (горизонтальное, вертикальное либо под углом 45 °); – включаем электронагреватель, устанавливаем автотрансформатором напряжение U – замеряем и записываем в соответствующую колонку таблицы измерений, значения напряжения и силы тока в цепи нагревателя; – для достижения стационарного температурного поля трубу выдерживают в соответствующем положении примерно 5минут перед началом измерений; стационарность определяется малым изменением температуры стенки трубы (не более 0,5 °С в минуту по показаниям термопары № 3); – измеряем ЭДС всех пяти термопар; усредненное значение ЭДС переводим в °С при помощи графика, имеющегося на лабораторном столе. При определении истинной средней температуры поверхности трубы учитываем, что термопары показывают температуру относительно холодного спая, находящегося при температуре помещения. Поэтому окончательно истинная температура трубы (t тр) рассчитывается из соотношения t тр = t изм–(t т– t и), где t изм − температура поверхности трубы по показаниям гальванометра, °С; t т, t и − температура воздуха в лаборатории в момент тарировки термопар и при выполнении лабораторной работы, соответственно. Таблица 6.6 Измеряемые в опыте величины
На основании измеренных величин рассчитываем: – количество теплоты Q, Вт, выделяемое электронагревателем
Q = U·I,
где U − напряжение, В; I − сила тока, А; – количество теплоты Q изл, Вт, отдаваемое трубой излучением
где ε лат= 0,87 — степень черноты окисленной латуни; с 0 = 5,67 Вт/(м2·К4) − коэффициент излучения абсолютно черного тела; F тр = π dL, м2 − наружная поверхность трубы (d = 35 мм, L = 1 м) Т тр, К − температура наружной поверхности трубы; Т ст, К − температура стен лаборатории во время опыта;
– количество теплоты, отводимое от трубы свободной конвекцией
Q к = Q – Q изл .
Значение коэффициента теплоотдачи рассчитывается из соотношения
где t в — температура воздуха в лаборатории.
По полученным трем значениям α при горизонтальном и вертикальном расположении трубы, а также при её наклоне под 45° к горизонту (αгор, αвер, α45) надо сделать заключение о том, как и почему изменяется значение коэффициента теплоотдачи при естественной конвекции от одиночной трубы при изменении её пространственного положения. Контрольные вопросы 1. Как устроена экспериментальная установка? Какие величины, с какой целью и как измеряются в опыте? 2. Какие факторы влияют на интенсивность теплоотдачи при свободном движении теплоносителя относительно трубы? 3. Как в лабораторной работе определяется количество теплоты, отводимое от трубы конвекцией? 4. Как определяется количество теплоты, отдаваемое трубой излучением? Какое допущение при этом принято? 5. От чего зависит и как рассчитывается значение приведенного коэффициента излучения? Почему в лабораторной работе eпр = eлат? 6. Как изменится коэффициент теплоотдачи от трубы, если её поместить в поток воздуха, движущегося поперёк трубы? 7. Как зависит коэффициент теплоотдачи от трубы от угла атаки потока теплоносителя? 8. Как изменятся значения конвективного и эффективного коэффициентов теплоотдачи, если трубу окрасить в белый цвет? 9. Как изменятся значения конвективного и эффективного коэффициентов теплоотдачи после окраски трубы в чёрный цвет? 10. Как изменится коэффициент теплоотдачи от трубы, если её поместить в воду той же температуры, что и температура воздуха в помещении? 11. В каком случае и с какой целью делается внешнее либо внутреннееоребрение труб? 13. Какие методы интенсификации процесса теплоотдачи используются на практике? 14. При каком условии изоляция трубы уменьшает теплоотдачу от неё, а при каком условии – увеличивает? 15. Запишите общий вид критериальных уравнений для определения коэффициента теплоотдачи при вынужденной и свободной конвекции? 16. Определите понятия «теплоотдача» и «теплопередача». Какие коэффициенты характеризуют эти процессы? Какой из этих коэффициентов является составляющим другого? Образец оформления титульного листа лабораторной работы по дисциплине «Термодинамика»
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ, МОЛОДЁЖИ И СПОРТА УКРАИНЫ Одесский национальный морской университет
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-26; просмотров: 1078; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 52.14.176.111 (0.011 с.) |


 − объёмный расход воздуха через калорифер, приведенный к нормальным условиям (р 0 = 760 мм рт. ст. или 1,01325·105 Па; t 0 = 0 °С или Т 0 = 273,15 К);
− объёмный расход воздуха через калорифер, приведенный к нормальным условиям (р 0 = 760 мм рт. ст. или 1,01325·105 Па; t 0 = 0 °С или Т 0 = 273,15 К); − объёмный расход воздуха, проходящего через расходомер при температуре t 2;
− объёмный расход воздуха, проходящего через расходомер при температуре t 2; ,
,
 ,
,
 .
.





 100 В;
100 В;
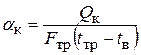 ,
,


