
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Методические указания К лабораторным работамСодержание книги
Поиск на нашем сайте
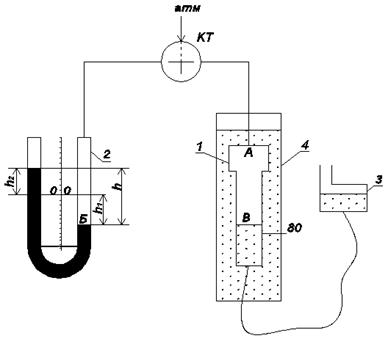
Лабораторный практикум по дисциплинам «Термодинамика» и «Техническая термодинамика», изучаемым в ОНМУ, включает пять работ. Целью практикума является углубление и систематизация теоретических знаний по вышеуказанным дисциплинам. Практикум направлен на ознакомление учащихся с методами экспериментальных исследований термодинамических свойств веществ и приобретение практических навыков использования измерительных приборов при теплотехнических измерениях. Назначение настоящих методических указаний − оказание помощи учащимся в выполнении лабораторных работ по указанным дисциплинам. К выполнению лабораторной работы учащийся готовится заранее, то есть к назначенной дате знакомится с целью лабораторной работы, методикой её выполнения, прорабатывает соответствующий теоретический материал, составляет заготовку протокола лабораторной работы (на отдельном листе изображает схему установки и готовит таблицу для записи результатов измерений). Титульный лист лабораторной работы оформляется в соответствии с приведенным в конце этого раздела образцом. В процессе выполнения работы учащийся записывает измеряемые величины в соответствующие колонки таблицы. После выполнения всех предусматриваемых лабораторной работой расчётов и графических построений студент в индивидуальном порядке защищает полученные результаты. Время выполнения работы, правила защиты и учета её результатов при соответствующем модульном контроле знаний учащихся устанавливается преподавателем в начале лабораторного практикума. Контрольные вопросы, по которым учащийся готовится к защите лабораторной работы, приводятся в конце описания лабораторной работы. Лабораторная работа № 1 посвящена исследованию изотермического процесса. Одной из характеристик этого процесса является постоянство произведения давления и удельного объема во всех точках процесса (pv = idem). Экспериментальному доказательству этого факта посвящена данная работа. Стенд для измерения необходимых величин (рис.6.1) состоит из бюретки 1, U-образного водяного мановакуумметра 2, напорного сосуда 3 и термостатирующего цилиндра 4. Бюретка служит для измерения объема воздуха при данном давлении с помощью шкалы, нанесенной на её образующей. Полный объем, занимаемый воздухом, состоит из его объема в бюретке (от плоскости А до уровня жидкости В, сжимающей либо расширяющей исследуемую порцию воздуха) и объема капилляра, соединяющего бюретку с мановакуумметром (от точки А до уровня жидкости Б в правом колене).
Дополнительными измерениями установлено, что объем капилляра от точки А до уровня жидкости Б в правом колене, когда он совпадает с уровнем жидкости в левом колене (то есть в случае соединения обоих колен с атмосферой) равен 13 см3. Из принципа действия установки (рис. 6.1) следует, что при сжатии воздуха в бюретке объём капилляра увеличивается и рассчитывается по формуле
где d вн = 0,4 см, − внутренний диаметр стеклянной трубки мановакуумметра, h лев, h пр − уровни жидкости в левом и правом коленах мановакуумметра, см.
Рис. 6.1. Схема экспериментального стенда Для исследования изотермического процесса
При расширении воздуха в бюретке объем капилляра уменьшается и равен
Алгоритм исследования изотермического процесса расширения: – соединяем правое и левое колена мановакуумметра и бюретку с атмосферой при помощи трехходового крана КТ (рис. 6.1). При этом уровни воды в коленах мановакуумметра выравниваются; – при помощи напорного сосуда 3 устанавливаем минимальный объем воздуха в бюретке (например, V б,0,расш.= 56 см3); – отсекаем выбранный объём воздуха от окружающей среды, поворачивая трехходовой кран на 180 °; – опускаем постепенно (ступенчато) напорный сосуд, делая 4-5 остановок и записывая при этом показания правого и левого колен мановакуумметра и соответствующие значения объема бюретки в таблицу 6.1. Таблица 6.1 Результаты измерений
Массу воздуха, находящегося в бюретке, рассчитываем из уравнения состояния Клапейрона для М кг идеального газа p 0 V 0,расш = M расш RT 0, где V 0,расш. = (V б, 0,расш.+13)·10–6 − объем воздуха в начале процесса, м3; р 0 = р атм − начальное (атмосферное) давление воздуха, Па;
Т 0 − температура воздуха в помещении во время опыта, К. R = 287,1 кДж/(кг·К) − удельная газовая постоянная воздуха.
Удельный объем воздуха (в м3/кг) в начале изотермического расширения можно рассчитать из уравнения состояния для 1 кгидеального газа p 0 v 0 = RT 0. либо Давление воздуха во всех последующих точках процесса расширения рассчитываем по формуле
где р 0 = р атм – атмосферное давление во время опыта, мм. рт. ст. Для перевода рі в Па необходимо значения, рассчитанные по формуле (6.3), делить на 750 мм. рт. ст.и умножать на 105. Объем воздуха (в см3) во всех исследуемых точках процесса расширения рассчитываем с учётом фактических объёмов бюретки и капилляра
Vi = V б , i + V кап, i,
где Здесь d и h подставляются в см. Проверяем точность выполненных измерений и расчетов, сопоставляя значения pivi и p 0 v 0
Если отклонение какого-либо произведения pivi от p 0 v 0 превышает 3%, то надо повторить измерения и расчеты для данной точки. Алгоритм исследования изотермического процесса сжатия аналогичен рассмотренному выше процессу расширения. Отличие состоит в том, что первоначально при помощи напорного сосуда 2 устанавливаем максимальный объем воздуха в бюретке (например, 94 см3). Масса воздуха при исследовании процесса сжатия Мсж будет другой, но определяется по той же формуле (6.2). Значения давления (в мм. рт. ст) в промежуточных точках процесса сжатия рассчитываем из соотношения
Значения объема воздуха в соответствующих точках процесса сжатия рассчитываем по формуле Vi = V б , i + V кап, i , где Проверку точности выполненных измерений и расчетов во всех промежуточных точках процесса сжатия выполняем по формуле (6.4). После выполнения расчетов для всех точек изотермы сжатия и расширения необходимо построить их совместно в координатах p,v. При этом надо выбрать максимально возможные масштабы по p и v в пределах листа формата А4 миллиметровой бумаги (в крайнем случае в пределах тетрадного листа в клетку). В каждой экспериментальной точке откладываем абсолютные отклонения по p и v. Для этого первоначально рассчитываем соответствующие относительные отклонения δ pi иδ vi из соотношения
то есть относительные погрешности измерений по p и v принимаются равными, а их знак определяется знаком погрешности δ(pv). Отложив в каждой точке абсолютные отклонения Δ pi и Δ vi с учётом их знака, проводим плавную усредняющую кривую в пределах образовавшегося коридора. При изучении конструкции и принципа действия установки следует уяснить роль и назначение термостатирующего сосуда. Желательно установить, какой термодинамический процесс будет протекать в бюретке, если выпустить воду из термостатирующего цилиндра и создать в нём вакуум. Естественно, при выполнении лабораторной работы надо знать, в каких единицах измеряются давление, объем и температура, в каких единицах они подставляются в термодинамические соотношения и как соотносятся между собой различные единицы измерения одного и того же параметра состояния рабочего тела.
Контрольные вопросы
1. Объясните принцип действия лабораторной установки и функциональное назначение основных элементов установки. 2. Каково назначение термостатирующего цилиндра и какую функцию он выполняет при сжатии и расширении воздуха в бюретке?
3. Какой термодинамический процесс можно исследовать на используемой установке, если выпустить воду из термостатирующего цилиндра и поддерживать в нём вакуум? Какой измерительный прибор необходимо дополнительно установить для этого? 4. Дайте определения понятиям разрежение, вакуум, избыточное, манометрическое, атмосферное, барометрическое и абсолютное давление. Запишите соотношения, связывающие эти давления. 5. Поясните назначение измерительных приборов: барометра, вакуумметра, манометра и мановакуумметра? Какое давление подставляется в термодинамические соотношения? 6. Какие элементы экспериментальной установки образуют дополнительный объём? Является ли он постоянным в опытах, как определяется и от чего зависит? 7. Перечислите основные единицы измерения давления и запишите соотношения между ними. 8. Запишите уравнение состояния для 1 кг идеального газа. Объясните физический смысл и размерности параметров, входящих в это уравнение. 9. Запишите уравнение состояния для 1 киломоля идеального газа. Объясните физический смысл и размерности параметров, входящих в это уравнение. 10. Какие параметры характеризуют состояние рабочего тела? 11. Поясните понятия «термические и калорические параметры состояния рабочего тела»? 12. Изобразите на диаграммах p, u и Т, s изотермический и адиабатный процессы сжатия идеального газа, исходящие из общей точки. В каком из этих процессов затрачивается больше технической работы при сжатии до одного и того же давления? 13. Изобразите надиаграммах p, u и Т, s изотермический и адиабатный процессы расширения идеального газа, исходящие из общей точки. В каком из этих процессов получается больше деформационной работы при расширении до одного и того же объёма? 14. Какими единицами измерения может быть задано количество вещества, участвующего в процессе? Каковы соотношения между величинами, задаваемыми этими единицами? 15. Как соотносятся между собой теплота и работа в изотермическом процессе? Как можно организовать изотермическое сжатие воздуха в компрессоре? 16. Какая разница между параметрами состояния и функциями процесса? Какие из этих величин характеризуют состояние рабочего тела?
Лабораторная работа № 2 посвящена экспериментальному определению средней изобарной теплоемкости воздуха. Как известно, теплоемкость − это количество теплоты, необходимое для нагрева единицы количества вещества на один градус в данном термодинамическом процессе. В зависимости от метода определения различают истинную и среднюю теплоемкости.
Истинная теплоемкость − производная от количества теплоты δ q по температуре dT (dt) в данном термодинамическом процессе
Истинная теплоемкость изображается на диаграмме T,s подкасательной (с) к кривой процесса в данной точке А (рис. 6.2). Средняя теплоемкость − количество теплоты q, которое необходимо подвести к единице количества вещества в данном термодинамическом процессе (либо отвести от вещества), чтобы повысить (понизить) его температуру от t 1 до t 2. Этой формулировке соответствует математическая запись
Рис 6.2. Определение истинной теплоемкости рабочего тела с помощью диаграммы T,s Средняя теплоемкость в данном процессе может быть определена экспериментально, а истинная рассчитана по (6.5). Как известно, количество вещества, участвующего в процессе, может быть задано в килограммах, киломолях и нормальных кубических метрах. Поэтому различают массовую, мольную и объемную теплоемкости, имеющие соответственно размерности Дж/(кг·К), Дж/(кмоль·К) и Дж/(нм3·К). Теплоемкость реального газа в заданном термодинамическом процессе зависти от двух параметров состояния. Чаще всего её представляют в табличном виде в зависимости от температуры и давления либо от температуры и удельного объема (реже). Теплоемкость идеального газа зависит только от температуры c = ƒ(T). В рамках упрощенной молекулярно-кинетической теории (МКТ) зависимость теплоемкости от температуры не учитывают, а учитывают только её зависимость от строения молекулы вещества, а именно, от количества атомов в молекуле рассматриваемого газа. По этой концепции изохорная и изобарная теплоемкости вещества рассчитываются из соотношений
где j − количество вращательных внутримолекулярных степеней свободы, R − удельная газовая постоянная рассматриваемого газа, Дж/(кг·К). Для одноатомных молекул j = 0, двухатомных 2, трех- и многоатомных 3. Количество теплоты, подводимое к рабочему телу массой М в заданном термодинамическом процессе (х = const) при изменении температуры от t 1 до t 2 может быть рассчитано из соотношения
В данной лабораторной работе определяется средняя изобарная теплоемкость воздуха, так как его давление при нагреве в лабораторной установке не изменяется. Принципиальная схема установки приведена на рис. 6.3. Установка состоит из: проточного калорифера 1, электронагревателя 2, автотрансформатора 3, электровентилятора 4, газового расходомера 5, вольтметра 6 и амперметра 7. Кроме того, в лаборатории имеются барометр и секундомер для измерения атмосферного давления и продолжительности опытов.
Рис. 6.3. Схема установки для определения
|
|||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-26; просмотров: 442; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.226.187.60 (0.008 с.) |


 ,
,
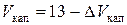 .
. .
.



 .
.
 .
.




 ,
, 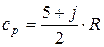 ,
, .
.



