
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Методи визначення поверхневого натягуСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Метод підрахунку крапель Цей метод ще називається сталагмометричним, оскільки в ньому застосовують прилад, який має назву сталагмометр (рис. 7). Для визначення поверхневого натягу досліджувану рідину засмоктують у прилад вище верхньої мітки 1 і спостерігають за її витіканням. Коли меніск рідини опуститься до мітки 1, починають рахувати краплі. Підрахунок ведуть до тих пір, поки меніск не дійде до нижньої мітки 2. Таким чином визначають число крапель, утворених при витіканні певного об’єму рідини, обмеженого двома мітками. Об’єм краплі тим більший, а число крапель n тим менше, чим більший поверхневий натяг рідини s та менше її густина r.
За допомогою сталагмометра найчастіше проводять порівняльне визначення поверхневого натягу, тобто визначають s досліджуваної рідини за відомим поверхневим натягом стандартної рідини s 0. У якості стандартної рідини застосовують, як правило, воду. Значення s 0 води за різних температур наведено в табл. 2.1. Таблиця 2.1. Поверхневий натяг води s0 в Дж/м2
За визначеним числом крапель для води n0 та для досліджуваної рідини n, густиною обох рідин та поверхневим натягом води s 0 розраховують поверхневий натяг досліджуваної рідини за формулою:
2. Метод максимального тиску газового пухирця (метод Ребіндера) В основі методу лежить визначення тиску P, який необхідний для витискування пухирців газу з капіляра в рідину. Цей тиск залежить від поверхневого натягу рідини s та радіусу капіляра r:
Вимірявши тиск P 0 для стандартної рідини з відомим поверхневим натягом s 0 (наприклад, для води) та тиск P для досліджуваної рідини, можна розрахувати її поверхневий натяг s за співвідношенням
Принципову схему приладу Ребіндера зображено на рис. 8. Для визначення тисків Р 0 та Р через капіляр 2, що торкається поверхні досліджуваної рідини, за допомогою вакуумного насосу засмоктуються пухирці повітря, які при цьому долають опір рідини в капілярі. В момент відриву пухирця від кінця капіляру перепад тиску компенсує капілярний тиск рідини. Величину такого перепаду визначають за максимальним показанням манометра. Вимірявши максимальний тиск газового пухирця для стандартної рідини та досліджуваного розчину, розраховують поверхневий натяг останнього за формулою (2.9).
Робота 2.1. Адсорбція на поверхні рідини Дослідження адсорбції на поверхні рідини проводять на прикладі адсорбції поверхнево-активних речовин – одноатомних спиртів – на поверхні поділу фаз розчин спирту – повітря. Оскільки поверхнева активність спиртів не однакова, діапазони досліджуваних концентрацій для різних спиртів мають відрізнятися. Молярна маса, густина та рекомендовані для дослідження концентрації розчинів для різних спиртів наведено в табл. 2.2. Метою роботи є дослідження закономірностей адсорбції ПАР на рідкій поверхні, встановлення параметрів адсорбційного процесу та визначення розмірів молекул ПАР. Таблиця 2.2. Молярна маса, густина та рекомендовані концентрації розчинів досліджуваних спиртів
Хід виконання роботи 1. Записати в табл. 2.3 температуру досліду, назву досліджуваного спирту та його вихідну концентрацію с 0. Переписати із табл. 2.2 в табл. 2.3 рекомендовані концентрації розчинів для досліджуваного спирту та розрахувати об’єми розчину спирту з вихідною концентрацією Vвих. та води Vводи, які потрібно змішати для отримання розчинів об’ємом Vр-ну заданої концентрації. Зазвичай для досліджень готують 10 см3 розчинів.
Таблиця 2.3. Дані для приготування розчинів спирту
2. Приготувати в окремих пронумерованих сухих пробірках розчини досліджуваного спирту із зазначеними у табл. 2.3 концентраціями, відміряючи бюретками розраховані об’єми вихідного розчину спирту Vвих. та води Vводи. 3. За допомогою ретельно промитого сталагмометра визначити кількість крапель дистильованої води n 0, що відповідають об’єму рідини між верхньою та нижньою рисками сталагмометра. Вимірювання проводити тричі до збігу результатів з точністю до однієї краплі. Результати вимірювань записати в табл. 2.4. 4. Аналогічно провести підрахунок кількості крапель для всіх приготованих розчинів у порядку зростання їх концентрацій, починаючи з найнижчої. Перед вимірюванням посудину, з якої заповнюється сталагмометр, необхідно сполоснути невеликою кількістю (~ 1 см3) досліджуваного розчину. Сталагмометр промивати не потрібно. Кількість крапель для кожного розчину визначити тричі і записати отримані дані у відповідний рядок табл. 2.4. Обчислити для кожної концентрації спирту середні значення кількості крапель n. 5. Оскільки розчини розведені, то їх густину можна вважати рівною густині води, тому поверхневий натяг для всіх досліджуваних розчинів розраховувати за спрощеною формулою:
де Таблиця 2.4. Результати вимірювань поверхневого натягу розчинів спирту
6. За даними табл. 2.4 побудувати залежність табл. 2.5. 7. Розрахувати послідовно зміну концентрації спирту при переході від одного розчину до іншого як Dс = сі+1- сі та відповідну зміну поверхневого натягу D σ = σі+1- σі, а потім обчислити їх відношення
При обчисленнях слід враховувати те, що розмірність концентрації – кмоль/м3, тому значення універсальної газової сталої за таких умов R =8,31×103 Дж/(кмоль∙К). Таблиця 2.5. Результати розрахунків характеристик адсорбції на поверхні розчинів спирту
8. 9. Обчислити площу, яку займає на поверхні поділу фаз у щільному моношарі одна молекула ПАР: 10.Визначити значення константи В рівняння Шишковського: 11.Розрахувати за рівнянням Ленгмюра значення повної адсорбції а, використовуючи обчислені параметри адсорбційного процесу К та Г¥ @ а¥:
Записати отримані результати в останню колонку табл. 2.5 і побудувати на одному полі та в однаковому масштабі графіки залежностей Г =
Звіт Таблиці 2.3, 2.4, 2.5. Графіки sексп. = Константи рівняння Ленгмюра: a ¥= кмоль/м2, K = м3/кмоль. Константи рівняння Шишковського: A = м3/кмоль, B = Дж/м2. Площа, яку займає одна молекула адсорбату S 0 = м2. Товщина адсорбційного шару l = м. Висновок. Робота 2.2. Визначення питомої поверхні адсорбента
Дослідження адсорбції на твердому адсорбенті дає можливість встановити його питому поверхню, тобто поверхню 1 кг адсорбенту. Для цього проводять експеримент з адсорбатом, характеристики якого відомі, будують ізотерму адсорбції та визначають величину граничної адсорбції на адсорбенті a ¥ (моль/кг), яка відповідає ємності щільного моношару на поверхні адсорбенту. Ця величина дорівнює максимальній кількості молів адсорбату, що здатні розміститись на поверхні адсорбенту. Кількість молекул адсорбату, які розміщуються на поверхні 1 кг адсорбенту при повному насиченні його поверхні, визначається добутком величини граничної адсорбції a ¥ та числа Авогадро NА. Якщо відома площа, яку займає одна молекула адсорбату на поверхні адсорбента S 0, то можна розрахувати питому поверхню адсорбенту як добуток граничної адсорбції, числа Авогадро та площі, що її займає на поверхні адсорбенту одна молекула адсорбату:
Хід виконання роботи При виконанні даної роботи як адсорбат використовується досліджений у попередній роботі спирт, оскільки для нього вже встановлено величини констант А та В рівняння Шишковського (2.2) та площа Метою роботи є визначення величини питомої поверхні адсорбента за адсорбційними характеристиками ПАР. 1. Переписати з протоколу роботи 2.1 в табл. 2.6 розраховані дані для досліджуваного спирту: константи А та В рівняння Шишковського, температуру, за якої їх було визначено, та площу
Таблиця 2.6. Дані для приготування розчинів досліджуваного спирту
2. Приготувати п’ять розчинів по 25 см3 з концентраціями сзадан. шляхом послідовного розведення вихідного розчину з концентрацією с 0 (кмоль/м3), відміряючи бюретками у ретельно вимиті та пронумеровані колби об’єми вихідного розчину спирту та води, які наведено в табл. 2.6. 3. Зважити на технічних терезах з точністю до 0,01 г п’ять наважок активованого вугілля (маса наважок залежить від марки вугілля та визначається викладачем, зазвичай вона становить 0,25 г) і перенести їх у колби з приготованими розчинами. Для встановлення адсорбційної рівноваги розчини спирту з вугіллям необхідно періодично збовтувати протягом 30 хв. 4. Після досягнення рівноважного адсорбційного стану вміст колб відфільтрувати крізь сухі складані паперові фільтри в пронумеровані пробірки, причому перші порції фільтрату (приблизно 5–7 см3) необхідно вилити, тому що в них концентрація ПАР занижена внаслідок адсорбції спирту фільтрувальним папером. 5. Скориставшись добре промитим сталагмометром, визначити кількість крапель дистильованої води n 0, що поміщаються в об’ємі сталагмометра, обмеженому верхньою та нижньою рисками. Вимірювання проводити тричі до збігу результатів з точністю до однієї краплі. Результати вимірювань записати в табл. 2.7. 6. Аналогічно провести вимірювання для всіх приготованих розчинів в порядку зростання концентрацій, починаючи з найменшої. Посудину, з якої заповнюється сталагмометр, необхідно сполоснути невеликою кількістю досліджуваного розчину (2–3 см3). Сталагмометр промивати не потрібно. Порахувати тричі кількість крапель для кожного розчину і отримані дані записати у відповідний рядок табл. 2.7. Визначити для кожної концентрації середні значення кількості крапель n. 7. Оскільки концентрації розчинів є невисокими, то їхню густину можна вважати рівною густині води, тому поверхневий натяг для всіх досліджуваних розчинів розрахувати за формулою:
де Таблиця 2.7. Результати вимірювань поверхневого натягу розчинів спирту
8. Переписати із табл. 2.6 в таблицю 2.8 значення констант А та В рівняння Шишковського та температуру, за якої їх було визначено. Із табл. 2.7 в табл. 2.8 перенести значення вихідних концентрацій розчинів спирту. Перерахувати та внести в табл. 2.8 значення констант А та В рівняння Шишковського для температури досліду. 9. Розрахувати значення рівноважної концентрації ПАР у фільтратах за допомогою рівняння Шишковського (2.2), перетворивши його на відповідний вираз для обчислення концентрації:
де 10. Розрахувати значення питомої адсорбції ПАР за відомими концентраціями розчинів до та після адсорбції, користуючись рівнянням:
Визначити також відношення 11. Побудувати графік залежності
Таблиця 2.8. Розрахунок характеристик адсорбції спирту на межі поділу активоване вугілля – водний розчин
12. За даними табл. 2.8 на основі лінійної форми рівняння Ленгмюра (1.2) у вигляді
Рис. 10. Графік для визначення граничної адсорбції
13. За побудованим графіком визначити граничне значення питомої адсорбції a¥ як величину, що є оберненою до тангенса кута нахилу прямої. 14. На основі величини граничної адсорбції a¥ і значення
Площа S 0, яку займає на поверхні адсорбенту молекула спирту, визначається розміром її гідрофільної групи і тому для молекул одного гомологічного ряду вона є однаковою. Ця величина розраховується для досліджуваного спирту в роботі 2.1. Звіт Таблиці 2.6, 2.7, 2.8. Графіки Константи рівняння Шишковського: А = м3/кмоль та В = Дж/м2. Гранична питома адсорбція.......................... спирту на активованому вугіллі а ¥ = кмоль/кг. Питома поверхня адсорбенту Sпит. = м2 /кг. Висновок.
Питання до лабораторної роботи
1. Що таке поверхневий натяг? Від чого він залежить? 2. Яке рівняння описує залежність поверхневого натягу розчину ПАР від його концентрації? 3. Чому для однакового об’єму різних рідин характерна різна кількість крапель, що витікають з капіляра? 4. Що таке поверхнева активність ПАР та як вона визначається в лабораторній роботі? 5. Як змінюється поверхнева активність ПАР у гомологічному ряді зі збільшенням вуглецевого ланцюга? 6. Для чого в лабораторній роботі визначають питому надлишкову адсорбцію Г? 7. Що таке гранична адсорбція та від чого вона залежить? 8. Як обчислюють геометричні параметри молекул ПАР у даній лабораторній роботі?
Література: [1] 114 – 136; [2] 72 – 89; [3] 39 – 52; [4] 20 – 27, 33 – 37.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-23; просмотров: 414; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.145.45.223 (0.011 с.) |


 .
.
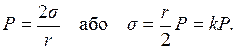
 .
.


 , см3
, см3
 , см3
, см3
 ,
,
 – поверхневий натяг води за температури досліду (див. табл. 2.1). Результати розрахунків занести в табл. 2.4.
– поверхневий натяг води за температури досліду (див. табл. 2.1). Результати розрахунків занести в табл. 2.4. . Оскільки зміна поверхневого натягу від концентрації ПАР описується рівнянням Шишковського
. Оскільки зміна поверхневого натягу від концентрації ПАР описується рівнянням Шишковського  , то експериментальні величини s графічно апроксимують плавною кривою. Координати точок, які не потрапляють на криву, мають бути виправлені за допомогою апроксимації. Значення концентрацій досліджуваних розчинів
, то експериментальні величини s графічно апроксимують плавною кривою. Координати точок, які не потрапляють на криву, мають бути виправлені за допомогою апроксимації. Значення концентрацій досліджуваних розчинів  та апроксимовані величини поверхневого натягу sапр., що їм відповідають, записати в
та апроксимовані величини поверхневого натягу sапр., що їм відповідають, записати в , які є наближеними значеннями похідних. Величини похідних
, які є наближеними значеннями похідних. Величини похідних  можна замінити відношеннями кінцевих різниць
можна замінити відношеннями кінцевих різниць 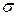 та
та  . Дані розрахунків записати в табл. 2.5. На підставі отриманих величин обчислити значення надлишкової адсорбції Г за рівнянням Гіббса (2.1), яке в цьому випадку виглядатиме таким чином:
. Дані розрахунків записати в табл. 2.5. На підставі отриманих величин обчислити значення надлишкової адсорбції Г за рівнянням Гіббса (2.1), яке в цьому випадку виглядатиме таким чином: .
.




 ,
м-1
,
м-1

 Розрахувати значення ссер./Г та побудувати прямолінійну графічну залежність ссер./Г= f(ссер.) (рис. 9). За тангенсом кута нахилу
Розрахувати значення ссер./Г та побудувати прямолінійну графічну залежність ссер./Г= f(ссер.) (рис. 9). За тангенсом кута нахилу  прямої визначити величину граничної адсорбції Г¥ (a¥), яка є оберненою до нього, а за відрізком
прямої визначити величину граничної адсорбції Г¥ (a¥), яка є оберненою до нього, а за відрізком  , що пряма відтинає на осі ординат, обчислити константу K в рівнянні Ленгмюра (або A в рівнянні Шишковського), тобто константу рівноваги адсорбційного процесу. При визначенні параметрів прямої необхідно враховувати масштаби відповідних осей.
, що пряма відтинає на осі ординат, обчислити константу K в рівнянні Ленгмюра (або A в рівнянні Шишковського), тобто константу рівноваги адсорбційного процесу. При визначенні параметрів прямої необхідно враховувати масштаби відповідних осей. , та товщину адсорбційного шару
, та товщину адсорбційного шару  . Необхідні для розрахунків значення молярної маси та густини спирту запозичити з табл. 2.2. Слід також пам’ятати, що при розрахунках на кмоль число Авогадро NА = 6,02×1026 кмоль–1.
. Необхідні для розрахунків значення молярної маси та густини спирту запозичити з табл. 2.2. Слід також пам’ятати, що при розрахунках на кмоль число Авогадро NА = 6,02×1026 кмоль–1. .
. .
. та а =
та а =  ; ссер./Г=
; ссер./Г=  .
.
 , яку займає одна молекула в щільному мономолекулярному шарі на межі поділу фаз.
, яку займає одна молекула в щільному мономолекулярному шарі на межі поділу фаз. , см3
, см3
 , см3
, см3
 ,
, - поверхневий натяг води, який визначається за даними табл. 2.1, виходячи з температури досліду. Результати занести в табл. 2.7.
- поверхневий натяг води, який визначається за даними табл. 2.1, виходячи з температури досліду. Результати занести в табл. 2.7. ,
,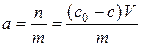 .
. . Дані розрахунків записати в табл. 2.8.
. Дані розрахунків записати в табл. 2.8.


 побудувати прямолінійну залежність
побудувати прямолінійну залежність  (рис. 10).
(рис. 10).
 .
. і
і 


