
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Лабораторна робота № 5 «В’ЯЗКІСТЬ»Содержание книги
Поиск на нашем сайте
Перед тим, як починати виконувати роботу, присвячену вивченню в’язкості розчинів, слід самостійно ознайомитись з кількісною характеристикою динамічної в’язкості (рівняння Ньютона та Пуазейля), віскозиметричним методом визначення в’язкості та молярної маси високомолекулярних сполук (ВМС), рівнянням Ейнштейна для в’язкості колоїдних розчинів та межами його застосування, а також рівняннями Штаудингера та Марка–Куна–Хаувінка.
Стислі теоретичні відомості Між шарами рідини, що рухаються один відносно одного з різними швидкостями, виникає сила внутрішнього тертя F. За Ньютоном така сила пропорційна добутку поверхні дотику шарів рідини S та градієнту швидкості
де du – зміна швидкості при переході від одного елементарного шару рідини до іншого; dx – відстань між шарами. Коефіцієнт пропорційності У випадку ламінарної течії об’ємна швидкість витікання
де V – об’єм рідини з в’язкістю h, що витікає крізь капіляр довжиною l та радіусом r за час З рівняння (5.2) видно, що в’язкість рідини можна визначити, вимірюючи час витікання певного об’єму рідини за гідродинамічного тиску Р крізь капіляр з відомими параметрами:
При визначенні в’язкості рідини зазвичай використовують порівняльний метод. Якщо час витікання однакових об’ємів двох різних рідин крізь такий самий капіляр дорівнює
Оскільки висота рівня обох рідин при вимірюванні є однаковою, то відношення гідродинамічних тисків на кінці капілярної трубки дорівнює відношенню густин, тобто
Віскозиметр – прилад для вимірювання в’язкості (рис. 18) – має вигляд U-подібної трубки з капіляром в одному із колін. Капіляр зверху сполучається з кулькою, об’єм якої визначається мітками «a» і «б». В широке коліно віскозиметра піпеткою наливають певний об’єм стандартної рідини, засмоктують її за допомогою гумової трубки і груші через капіляр у кульку вище мітки «а» і дають вільно витікати. Час витікання об’єму рідини, що знаходиться між мітками «а» і «б», вимірюють за допомогою секундоміра.
При визначенні в’язкості водних розчинів як стандартну рідину використовують воду. Температурну залежність в’язкості води наведено в табл. 5.1. Дослід з водою повторюють три рази (час витікання повинен збігатися з точністю до 0,5 с). Потім проводять аналогічні вимірювання з досліджуваною рідиною. Густини рідин знаходять за таблицями або визначають за допомогою пікнометра. Оскільки зі збільшенням температури в’язкість рідини зменшується, вимірювання Таблиця 5.1. Температурна залежність в’язкості води h 0, Па∙с
Робота 5.1.Дослідження в’язкості структурованих розчинів Залежність в’язкості розчинів від об’ємної концентрації описується рівнянням Ейнштейна
де h 0 – в’язкість дисперсійного середовища; a – коефіцієнт, що залежить від форми часток та взаємодії між ними; j – об’ємна концентрація дисперсної фази. Для колоїдних систем зі сферичними частками дисперсної фази, які не взаємодіють ні між собою, ні з дисперсійним середовищем, a = 2,5. Якщо частки дисперсної фази анізодіаметричні (мають суттєво відмінні розміри в різних проекціях), сольватуються та здатні утворювати структуровані розчини, то коефіцієнт a більшій за 2,5. При цьому його величина зростає залежно від того, наскільки значними є прояви зазначених вище явищ. З метою дослідження інтенсивності сольватації, форми частинок та їх здатності до структуроутворення в розчинах вимірюють в’язкість розчинів з різним об’ємним вмістом дисперсної фази і проводять обробку данних за рівнянням Ейнштейна (5.6). Визначають величину та характер зміни коефіцієнта a і на підставі цих даних роблять висновок стосовно форми частинок дисперсної фази, інтенсивності їхньої сольватації, а також здатності структуруватися.
Хід виконання роботи Об’єктами дослідження у даній роботі є розведені розчини полімерів, які здатні до утворення структурованих рідких середовищ (желатина, карбоксиметилцелюлоза(КМЦ), полівініловий спирт та інші). Метою роботи є підтверження структуроутворення у розчинах полімерів. 1. Записати у табл. 5.2 характеристики системи, що досліджується. Таблиця 5.2. Характеристики досліджуваної системи і умови експерименту
2. Приготувати шість розчинів із різним вмістом дисперсної фази послідовним розведенням вихідного розчину. Для цього в пронумеровані чисті та сухі пробірки відміряти бюретками вказані в табл. 5.3 об’єми вихідного розчину та води. Утворені розчини обережно збовтати. 3. Ретельно вимити візкозиметр. Піпеткою налити у візкозиметр 4. Виміряти час витікання кожного приготованого розчину, починаючи з найменш концентрованого. Для кожного розчину вимірювання проводити тричі аналогічно досліду з дистильованою водою. Дані занести в табл. 5.3, розрахувати та записати для кожного розчину значення середнього часу витікання. 5. Обчислити в’язкість розчинів. Враховуючи те, що розчини, які досліджуються, мають низькі концентрації дисперсної фази, можна вважати, що густина таких розчинів дорівнює густині води. Це дозволяє спростити розрахункову формулу (5.5) до вигляду:
де h 0 – в’язкість дисперсійного середовища; t 0 – середній час витікання води; t – середній час витікання розчину. Обчислені значення в’язкості розчинів записати у табл. 5.3. 6. Розрахувати та записати у табл. 5.3 для розчину кожної концентрації величини специфічної в’язкості hsp = Таблиця 5.3. Результати вимірювання в’язкості досліджуваних розчинів
7. На підставі отриманих даних побудувати графік залежності
Рис. 19. Залежність для визначення коефіцієнта a рівняння Ейнштейна Звіт Таблиці 5.2, 5.3. Графіки h = f(j), Значення коефіцієнта a рівняння Ейнштейна: Висновок.
Питання до лабораторної роботи 1. Як пов’язані між собою об’ємна швидкість витікання рідини з капіляра та її в’язкість? 2. В’язкість яких дисперсних систем описується рівнянням Ейнштейна? 3. На що вказує величина коефіцієнта a рівняння Ейнштейна при малих значеннях об’ємної концентрації (j → 0)? 4. Про що свідчить злам на залежності специфічної в’язкості від об’ємної концентрації?
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-23; просмотров: 206; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.135.186.233 (0.008 с.) |

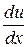 :
: ,
,
 в рівнянні (5.1) є коефіцієнтом внутрішнього тертя або динамічною в’язкістю (скорочено – в’язкість). У відповідності до (5.1) в’язкість має розмірність Па·с. Рідини, для яких є справедливою формула (5.1), називаються ньютонівськими.
в рівнянні (5.1) є коефіцієнтом внутрішнього тертя або динамічною в’язкістю (скорочено – в’язкість). У відповідності до (5.1) в’язкість має розмірність Па·с. Рідини, для яких є справедливою формула (5.1), називаються ньютонівськими. ньютонівської в’язкої нестисливої рідини крізь тонку циліндричну трубку визначається законом Пуазейля:
ньютонівської в’язкої нестисливої рідини крізь тонку циліндричну трубку визначається законом Пуазейля: ,
,
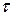 ; D Р – різниця тисків на кінцях капіляра.
; D Р – різниця тисків на кінцях капіляра.
 (для стандартної рідини) та t (для досліджуваної рідини), то згідно з (5.3) відношення в’язкостей досліджуваної та стандартної рідин складає
(для стандартної рідини) та t (для досліджуваної рідини), то згідно з (5.3) відношення в’язкостей досліджуваної та стандартної рідин складає
 . Отже, формула для визначення в’язкості досліджуваної рідини набуває вигляду:
. Отже, формула для визначення в’язкості досліджуваної рідини набуває вигляду:

 ,
,

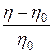 .
. . Згідно з рівнянням 5.6 це повинна бути пряма лінія, яка виходить з початку координат (див. рис. 19). Обчислити за тангенсом кута нахилу цієї прямої коефіцієнт a в рівнянні Ейнштейна (5.6) та за його величиною зробити висновок про форму частинок дисперсної фази, інтенсивність їхньої сольватації та характер взаємодії між ними.
. Згідно з рівнянням 5.6 це повинна бути пряма лінія, яка виходить з початку координат (див. рис. 19). Обчислити за тангенсом кута нахилу цієї прямої коефіцієнт a в рівнянні Ейнштейна (5.6) та за його величиною зробити висновок про форму частинок дисперсної фази, інтенсивність їхньої сольватації та характер взаємодії між ними.
 .
.



