
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Робота 5.2. Визначення молярної маси ВМС віскозиметричним методомСодержание книги
Поиск на нашем сайте
Спираючись на теорію в’язкості Ейнштейна для розведених розчинів низькомолекулярних сполук, Штаудингер встановив залежність специфічної в’язкості розведених розчинів полімерів від їх концентрації. Для розчинів, що містять анізодіаметричні (наприклад, паличкоподібні) макромолекули, він отримав співвідношення:
де hsp = З рівняння (5.8) випливає, що специфічна в’язкість, віднесена до концентрації, тобто приведена в’язкість
Рівняння Штаудингера (5.8) є справедливим лише для розчинів полімерів, що містять короткі та жорсткі ланцюги, які здатні зберігати паличкоподібну форму. Гнучкі ж ланцюги полімерів, що складаються зі значної кількості молекул, зазвичай згортаються в клубок, що зменшує опір їхньому руху. В таких випадках більш коректно пов’язувати молярну масу полімеру з характеристичною в’язкістю Для визначення молярної маси полімерів за характеристичною в’язкістю найчастіше застосовують рівняння Марка – Куна – Хаувінка:
де K – константа, що залежить від природи розчинника та полімеру; a –стала, яка характеризує форму макромолекули та може набувати значень від 0,5 (для клубків – глобул) до 1,7 (у випадку абсолютно жорстких макромолекул). Величини цих констант для деяких систем наведено в табл. 5.4.
Таблиця 5.4. Значення констант K та a рівняння Марка–Куна–Хаувінка для деяких систем полімер – розчинник
Отже, для визначення молярної маси полімеру за експериментальною концентраційною залежністю в’язкості його розчинів розраховують значення специфічної Хід виконання роботи Метою роботи є визначення молекулярної маси ВМС на підставі вимірювань в’язкості розчинів. 1. Підготовка до експерименту: 1.1. В табл. 5.5 зазначити систему, що досліджується: вказати назву ВМС та розчинника, навести концентрацію вихідного розчину с 0 і концентрації розчинів (за вказівкою викладача), які потрібно приготувати шляхом розведення вихідного розчину для проведення дослідження. 1.2. Розрахувати та записати в табл. 5.5 об’єми вихідного розчину та розчинника, які необхідні для приготування 10 см3 кожного з розчинів. 1.3. За допомогою бюреток приготувати розчини, наливаючи в сухі пронумеровані пробірки зазначені в табл. 5.5 об’єми рідин. Таблиця 5.5. Дані для приготування досліджуваних розчинів
2. Проведення експерименту: 2.1. Тричі промити дистильованою водою віскозиметр і три рази визначити час витікання води через капіляр віскозиметра, записуючи отримані результати в табл. 5.6. За табл. 5.1 визначити для температури досліду і записати в табл. 5.6 значення в’язкості води. 2.2. Визначити за допомогою віскозиметра тричі час витікання кожного з досліджуваних розчинів (різниця у часі не повинна бути більше 2.3. Розрахувати та записати в табл. 5.6 середній час витікання для кожного з досліджуваних розчинів. Таблиця 5.6. Експериментальні дані та результати розрахунків
3. Обробка експериментальних даних: 3.1. За отриманими експериментальними даними розрахувати та зафіксувати у табл. 5.6 для кожного з розчинів: 3.1.1. в’язкість розчину за формулою (5.7); 3.1.2. специфічну в’язкість, обчислену за рівнянням:
3.1.3. приведену в’язкість, визначену за співвідношенням (5.9). 3.2. За даними табл. 5.6 побудувати графік залежності
Рис. 20. Графік залежності приведеної в’язкості від концентрації 3.3. Визначити величину відрізка, що відтинається прямою на осі ординат і дорівнює характеристичній в’язкості [ h ] (див. рис. 20). Знаючи її, на підставі рівняння (5.10) визначити молярну масу ВМС за формулою:
(значення коефіцієнтів K та a для конкретної системи взяти із табл. 5.4). Звіт Таблиці 5.5 і 5.6. Графік Значення молекулярної маси ВМС: Висновок. Питання до лабораторної роботи 1. Як визначається молярна маса полімеру за вимірюваннями в’язкості його розчинів? Література: [1] 261– 269, 323 – 331; [2] 237 – 249, 265 – 273; [3] 321– 326, 423 – 437; [4] 214 – 220.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-23; просмотров: 264; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.217.89 (0.008 с.) |



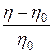 – специфічна в’язкість розчину; К – константа, яка є характерною для розчинів полімерів одного гомологічного ряду у певному розчиннику і яка визначається, наприклад, за молярною масою низькомолекулярних членів гомологічного ряду кріоскопічним методом; М – молярна маса полімеру; с – масовачастка полімеру у розчині.
– специфічна в’язкість розчину; К – константа, яка є характерною для розчинів полімерів одного гомологічного ряду у певному розчиннику і яка визначається, наприклад, за молярною масою низькомолекулярних членів гомологічного ряду кріоскопічним методом; М – молярна маса полімеру; с – масовачастка полімеру у розчині. , не залежить від концентрації с розчину полімеру і пропорційна його молярній масі М:
, не залежить від концентрації с розчину полімеру і пропорційна його молярній масі М:
 , оскільки саме ця величина визначає приріст в’язкості розчину, обумовлений присутністю в ньому мікрочастинок та їхньою анізодіаметричністю.
, оскільки саме ця величина визначає приріст в’язкості розчину, обумовлений присутністю в ньому мікрочастинок та їхньою анізодіаметричністю.
 та приведеної
та приведеної  визначають характеристичну в’язкість
визначають характеристичну в’язкість  (див. рис. 20). Використовуючи її значення, за рівнянням (5.10) обчислюють молярну масу полімеру.
(див. рис. 20). Використовуючи її значення, за рівнянням (5.10) обчислюють молярну масу полімеру.
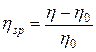 ;
;
 , який має бути прямою (рис. 20).
, який має бути прямою (рис. 20).
 (5.13)
(5.13)


