Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Опыт № 2. Зависимость скорости реакции от температурыСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Зависимость скорости реакции от температуры в гомогенной среде изучить на примере реакции Nа2S2O3+Н2SO4=Nа2SO4+SO2↑+S↓+Н2O При взаимодействии раствора тиосульфата натрия с серной кислотой выпадает в осадок сера, вызывающая при достижении определённой концентрации помутнение раствора. По промежутку времени от начала реакции до заметного помутнения раствора можно судить об относительной скорости этой реакции. Налить в одну пробирку 5см3 раствора тиосульфата натрия, в другую - 5 см3 раствора серной кислоты. Обе пробирки поместить в стакан с водой, чтобы растворы приняли температуру воды, и записать ее в журнал. Слить вместе содержимое обеих пробирок, точно отметив время от начала реакции до появления помутнения. В две другие пробирки налить по 5 см3 тех же растворов. Поместив пробирки в водяную баню или стакан с водой, нагреть воду на 10°С выше температуры предыдущего опыта. Выдержав пробирки при этой температуре 5-7 мин; слить содержимое пробирок. Измерить время до появления мути. Повторить опыт, повысив температуру ещё на 10°С. Результаты опытов свести в таблицу.
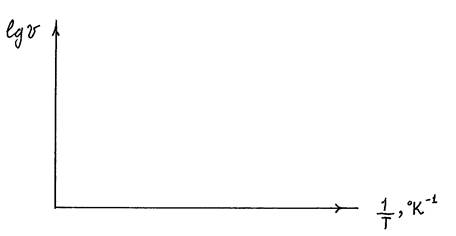
По полученным данным построить график зависимости модуля логарифма скорости реакции от обратной величины абсолютной температуры.
Сделать вывод о зависимости скорости реакции от температуры. Из графика определить тангенс угла наклона и вычислить энергию активации: Е = 2,303.R.tg α = ___________________________________________ Дж/моль
Опыт № 3. Скорость реакции в гетерогенной системе Налить в две пробирки по 5 см3 соляной кислоты. Отвесив на технохимических весах две навески по 0,2 г мрамора в кусочках, одну навеску мрамора растереть в ступке в порошок. Затем одновременно в одну пробирку ссыпать порошок, а в другую - бросить кусочки мрамора. Заметить время, которое потребовалось для полного растворения мрамора. Для обоих случаев рассчитать относительную скорость реакции (υ =1/τ). Определить, в каком случае скорость реакции больше и во сколько раз. Результаты опыта свести в таблицу.
Опыт №4. Влияние концентрации реагирующих веществ на смещение химического равновесия Смещение химического равновесия вследствие изменения концентрации реагирующих веществ исследовать на примере реакции FеС13+ЗКCNS ↔ ЗКС1+ Fe(CNS)3 Отмерив мерной пробиркой по 5 см3 разбавленных растворов хлорида железа (III) и роданида калия, смешать их и разделить на равные части в 4 пробирки. Окраску раствору придаёт образующийся роданид железа. Одну пробирку оставить для сравнения, во вторую - добавить 2-3 капли концентрированного раствора FеС13, в третью - 3—4 капли насыщенного раствора KСNS, а в четвёртую - насыпать немного кристаллического хлорида калия. Сравнив окраску растворов в трёх пробирках с окраской в контрольной пробирке, по изменению интенсивности окраски определить направление смещения равновесия и объяснить происходящие явления, исходя из принципа Ле - Шателье. Общий вывод по работе:
Опыт №2.Усиление гидролиза одной соли раствором другой гидролизующейся соли К 3 см3 концентрированного раствора (соль образована слабым основанием и сильной кислотой, её гидролиз протекает в основном только по 1-й ступени) прилить немного концентрированного раствора Nа2СО3 (соль образована, напротив, сильным основанием и слабой кислотой, её гидролиз протекает также по 1-й ступени) до образования устойчивого осадка. При этом наблюдать выделение пузырьков газа. В результате сливания двух вышеуказанных растворов происходит образование соли, полученной из слабых основания и кислоты. Эта соль подвергается полному гидролизу. Написать молекулярные и ионные уравнения реакций.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-23; просмотров: 565; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.133.141.201 (0.006 с.) |