
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Изучение электропроводности жидкостей и определение электрохимического эквивалента медиСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Цель и задача работы: Изучение механизма прохождения тока в электролитах и законов электролиза, проведение электролиза и определение электрохимическoго эквивалента меди.
Общие сведения
Вещества, водные растворы которых проводят электрический ток, называются электролитами. В отличие от металлов, имеющих электронную проводимость и полупроводников, имеющих электронно-дырочную проводимость, электролиты обладают ионной проводимостью. Иногда электролитами называют и сами проводящие растворы, хотя более правильное выражение – раствор электролита. Молекулы воды в незначительной степени распадаются на ионы:
Концентрация ионов водорода определяет кислотность раствора, а концентрация ионов гидроксила характеризует щелочность раствора. В чистой воде концентрации ионов Н + и ОН - равны. Чистая вода диссоциирует очень слабо. В 1 моль воды при 22º С распадается на ионы всего Однако получить такую воду очень трудно, т.к. в воздухе всегда присутствует углекислый газ, который, растворяясь воде, увеличивает концентрацию водородных ионов. Так как вода имеет большую диэлектрическую проницаемость ( Результатом диссоциации является образование сольватов (гидратов), когда молекулы воды «обволакивают» ионы, образуя вокруг них сольватную оболочку (рисунок 1).
Рисунок 1 Сольватные оболочки: а – катиона; б – аниона
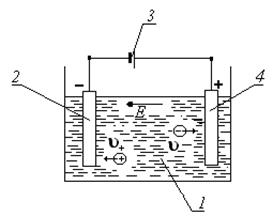
Для возникновения электрического тока в электролите, необходимо в ванну с раствором электролита опустить электроды из проводящего материала (металл, уголь и т.п.), к которым подключить источник тока (рисунок 2). Такое устройство называется гальванической или электролитической ванной.
Рисунок 2 Электролитическая ванна: 1 - ванна с раствором медного купороса; 2 - катод; 3 – источник тока; 4 – анод;
На ион в электролите действуют две силы: сила со стороны электрического поля
где Сила
где При движении иона в электролите между силами быстро устанавливается равновесие и движение иона между электродами можно рассматривать как равномерное и прямолинейное, поэтому:
Из (4) следует:
Если обозначить Так как ток в электролитах представляет собой упорядоченное движение ионов обоих знаков, обусловленное действием внешнего электрического поля, то плотность тока в электролите определяется выражением:
где n + и Происходящие на катоде и на аноде окислительно-восстанови-тельные реакции подчиняются законам Фарадея. Первый закон: масса выделившегося на электроде вещества пропорциональна протекшему через электролит заряду:
где Электрохимические эквиваленты ряда элементов приведены в таблице 1.
Таблица 1 Значения электрохимических эквивалентов для некоторых веществ
Второй закон: электрохимические эквиваленты элементов прямо пропорциональны их химическим эквивалентам:
где F - число Фарадея (F= 96500
Продукты электровосстановления или электроокисления ионов электролита могут вступить в химические реакции с раствором вблизи электрода. Такие процессы называются вторичными реакциями. Все эти процессы находят применение в различных отраслях техники, многие из них используются также в медицине.
|
||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 580; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.216.122.2 (0.011 с.) |

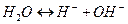 . (1)
. (1)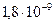 моль.
моль.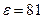 ) и молекулы воды обладают значительным дипольным моментом (
) и молекулы воды обладают значительным дипольным моментом (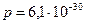 Кл∙м), то вокруг молекул воды на межатомных расстояниях (
Кл∙м), то вокруг молекул воды на межатомных расстояниях ( нм) существует довольно сильное электрическое поле. Последнее является непосредственной причиной, ослабляющей силу электростатического притяжения ионов в молекулах растворенного вещества. Поэтому в процессе растворения соли или щелочи за счет тепловых соударений происходит распад молекул на анионы и катионы. Если молекулы растворенного вещества в воде не диссоциируют на ионы, то раствор не является проводником. Например, водные растворы сахаров, глицерина – изоляторы.
нм) существует довольно сильное электрическое поле. Последнее является непосредственной причиной, ослабляющей силу электростатического притяжения ионов в молекулах растворенного вещества. Поэтому в процессе растворения соли или щелочи за счет тепловых соударений происходит распад молекул на анионы и катионы. Если молекулы растворенного вещества в воде не диссоциируют на ионы, то раствор не является проводником. Например, водные растворы сахаров, глицерина – изоляторы.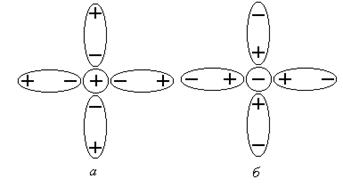
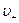 и
и 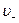 - скорости положительных и отрицательных ионов
- скорости положительных и отрицательных ионов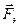 и сила сопротивления движению со стороны среды
и сила сопротивления движению со стороны среды 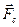 . Сила, действующая со стороны электрического поля, вычисляется по формуле:
. Сила, действующая со стороны электрического поля, вычисляется по формуле: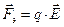 , (2)
, (2)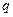 - заряд иона, Кл;
- заряд иона, Кл; 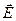 - напряженность электрического поля,
- напряженность электрического поля, 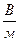 .
.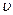 :
: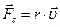 , (3)
, (3) - коэффициент сопротивления движению ионов в среде.
- коэффициент сопротивления движению ионов в среде.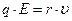 . (4)
. (4)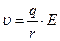 . (5)
. (5)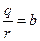 , то
, то 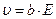 . Коэффициент b называется подвижностью ионов. Физический смысл подвижности в том, что она характеризует скорость ионов в электролите при напряженности электрического поля Е = 1
. Коэффициент b называется подвижностью ионов. Физический смысл подвижности в том, что она характеризует скорость ионов в электролите при напряженности электрического поля Е = 1 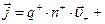
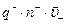 , (6)
, (6) - - концентрации катионов и анионов;
- - концентрации катионов и анионов; 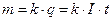 , (7)
, (7) - электрохимический эквивалент; I – сила тока, А; t - время, с.
- электрохимический эквивалент; I – сила тока, А; t - время, с.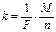 , (8)
, (8)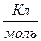 ); M – молярная масса выделившегося на электроде вещества; n – его валентность,
); M – молярная масса выделившегося на электроде вещества; n – его валентность, 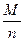 - химический эквивалент.
- химический эквивалент.


