
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Методика выполнения работы и ее обоснование
Результаты многочисленных исследований реакции разложения мочевины в водных растворах указывают на то, что первым этапом разложения является изомеризация мочевины, т.е. ее превращение в цианат аммония с последующим переходом из цианата в карбонат и далее – в аммиак и углекислоту: CO(NH2)2 ↔ NH4CNO NH4CNO → (NH4)2CO3 → 2NH3 + CO2 + H2O. Реакция превращения цианата в карбонат протекает практически необратимо. Такого рода разложение с заметной скоростью происходит лишь в водных растворах и при повышенных температурах (50оС и более), причем протекает по мономолекулярному механизму. В ходе реакции водный раствор органического вещества CO(NH2)2 с ковалентными связями превращается в раствор, диссоциирующей на ионы соли NH4CNO, поэтому электропроводность его со временем растет. Это дает возможность измерять скорость реакции как приращение электропроводности и ее можно считать пропорциональной концентрации конечного продукта. Влиянием присутствия переменного количества мочевины можно пренебречь. Исследуемая реакция является реакцией первого порядка, поэтому расчет константы скорости реакции ведется по уравнению где c 0 – начальная концентрация мочевины; x – концентрация мочевины, прореагировавшей к данному моменту времени; t – время данного замера от начала реакции. Принимаем, что увеличение электропроводности во времени пропорционально количеству образовавшегося карбоната или количеству прореагировавшей мочевины. Обозначим: L 0– электропроводность раствора в момент начала реакции; Lt – электропроводность в данный момент времени t; L ∞ – электропроводность, соответствующая последнему измерению, когда процесс разложения мочевины полностью закончен. Тогда, c 0 = const(L∞ - L 0), (c 0 – x) = const(L∞ - L 0) – const(Lt – L 0). Таким образом, расчеты можно проводить по уравнению:
Величину L 0 непосредственно экспериментально определить не удается, так как от начала реакции до первого измерения проходит некоторое время. Поэтому, величину L 0находят экстраполяцией, для чего строят график в координатах ln(L ∞ - Lt) – t и затем вычисляют L 0. Вычислив константу скорости реакции для каждого момента времени, определяют среднее значение и сравнивают с величиной k, полученной графическим путем по тангенсу угла наклона прямой к оси t на графике.
По двум константам скорости и двум температурам определяют величину энергии активации по уравнению Аррениуса (1.13).
Порядок выполнения работы
1. Стакан в термостате наполняют дистиллированной водой (около 100 см3). Термостат закрывают крышкой, устанавливают электроды для измерения электропроводности и термодатчик. Электроды устанавливают так, чтобы они были ниже уровня воды на 0,5 – 1 см. Подключают электроды и термодатчик. 2. Устанавливают термостат на поддержание требуемой температуры (50, 60 или 70°С). Обеспечивают перемешивание воды в стакане и, когда температура в нем установится на требуемом уровне, переходят к выполнению следующего пункта. 3. Растворяют навеску (1г) мочевины. Через 1 минуту после начала растворения мочевины выключают перемешивание и начинают измерение электропроводности. 4. Проводят измерение электропроводности (L) в течение 30 минут с интервалом в 3 минуты. 5. Чтобы довести реакцию практически до конца и определить значение L ∞, температуру в термостате поднимают до 95°С и выдерживают раствор в течение 1 часа. Затем охлаждают до первоначальной температуры и определяют электропроводность L ∞. 6. Проводят опыт при другой температуре (согласно п. 1 – 5). 7. Результаты заносят в таблицу. Строят графики в координатах ln(L ∞ - Lt) – t,из которых находят L 0. 8. Вычисляют константы скорости реакции и энергию активации.
Рекомендуемый вид таблицы
Температура опыта T = °С L ∞ = мСм L 0 = мСм
Работа № 4
|
|||||||||
|
Последнее изменение этой страницы: 2021-05-11; просмотров: 55; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.23.127.197 (0.007 с.) |
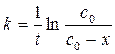 ,
, 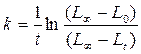 . (3.1)
. (3.1)


