
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Способы выражения состава раствора
Основные понятия и определения. Количество вещества n – это число молей данного вещества. m(г) – масса растворенного вещества, М – молярная масса вещества. Моль – количество вещества (в граммах), численно равное молекулярной массе вещества. (1 моль воды Н2О – 18 граммов). Плотность раствора раствора. ρ [мг/дм3] = ρ[г/м3]
2.2.1 Массовая доля δ растворенного вещества В – отношение массы вещества к массе раствора: Если плотность раствора не указана, можно считать, что ρ = 1(г/мл) Задача.: Вычислить массовую долю азотнокислого аммония NH4NO3, если в 230 г воды растворили 20 г соли. Решение: масса растворенного вещества m(B) = 20 г, масса раствора m(R) = 230 + 20 = 250 г, δ = 20/250 = 0,08. Задача. Вычислить массу сульфата натрия Na2SO4 в растворе объемом 0,2 л с δ = 0,1 и ρ = 1,05(г/мл) = 1050 (г/л). Решение: m = δ×ρ×V = 0,1×1050×0,2 = 21г. 2.2.2. Процентное содержание вещества в растворе ω% = δ×100% Задача: приготовить 60 г 40% раствора сернокислого железа FeSO4. Решение: в 100 г раствора должно содержаться 40 г FeSO4. Составляем пропорцию: раствор вещество 100 г ------ 40 г (Fe SO4) 60 г ------ х г х = 24 г. Для приготовления 60 г раствора надо взять 24 г соли и 60 – 24 = 36 г воды. Задача. Из 60% раствора серной кислоты и 10% раствора серной кислоты приготовить 5 л 40% раствор кислоты. Решение: если I раствора взять х(л), II раствора у(л), тогда кислоты в растворе будет δ1×х + δ2×у, объем раствора (х + у) литров. δ = 0,4, следовательно, 2.2.3. Мольная доля χ(В) растворенного вещества – отношение количества растворенного вещества (в молях) к суммарному числу молей в растворе, с учетом числа молей растворителя. Задача: определить мольную долю ионов Na+ в растворе, если 29 г NaCl растворили в 360 г воды. Решение: NaCl = Na+ + Cl–; при растворении одного моля соли в растворе будет 1моль ионов натрия и 1моль ионов хлора. 29 г соли это 29/58 = 0,5 моля соли, следовательно, в растворе будет 0,5 моля Na+, 0,5 моля Cl– и 360/18 = 20 молей воды. χ(Na+) = 0,5/(0,5 + 0,5 + 20) ≈ 0,024.
2.2.4. Молярная концентрация вещества в растворе – это отношение количества растворенного вещества к объему раствора, Св = nВ/Vr; nВ – число молей растворенного вещества, Vr – объем раствора в литрах. Т.к. масса растворенного вещества Запись 2М H2SO4 означает раствор, в каждом литре которого содержится 2 моля серной кислоты, т.е. 2×98 = 196 г кислоты. Задача. Вычислить молярную концентрацию раствора серной кислоты, H2SO4, если плотность раствора ρ = 1176 (г/л) и массовая доля кислоты в растворе δ = 0,25. Решение: масса кислоты в растворе m = ρ×δ×V; Задача. Какой объем раствора с ω = 9,3% серной кислоты с ρ = 1,05 (г/мл) потребуется, чтобы приготовить 0,35М раствор кислоты объемом 40 мл. Решение: Vωρ×ω = VCC×M; Vω = Задача. Сколько мл 0,1М раствора KMnO4 надо взять, чтобы приготовить 120 мл 0,02М раствор. Решение: чтобы приготовить 120 мл 0,02М раствора, надо взять m = C×V×M граммов соли. В исходном растворе соли mо = Cо×Vо×M. По условию задачи m = mо, следовательно C×V×M = Cо×Vо×M; Для приготовления раствора надо взять 24 мл исходного раствора и добавить 120 – 24 = 96 г воды. 2.2.5. Моляльная концентрация вещества в растворе Cm – это отношение количества растворенного вещества в 1 кг растворителя: если n – число молей растворенного вещества, тогда
2.2.6. Нормальная концентрация или нормальность раствора - это количество эквивалентов n экв растворенного вещества в 1 литре раствора: Сн = nэкв/V; [V] = литр. Нормальная концентрация обозначается Сн или H. Запись 2H(H2SO4) означает раствор серной кислоты, в каждом литре которого содержится 2 молярных массы эквивалентов серной кислоты.
Так как количество эквивалентов растворенного вещества nэкв = m/Мэкв, m – масса растворенного вещества в граммах, Мэкв – молярная масса эквивалента растворенного вещества, [Мэкв] = г/моль, получим: нормальная концентрация вещества в растворе Cn = (m/Мэкв)/V Замечание: параллельно с понятием молярная масса эквивалента вещества, используется понятие грамм – эквивалент вещества. Эквивалентом называется весовое количество вещества, взаимодействующее без остатка с одной (точнее с 1,008) весовой частью водорода или с восемью частями кислорода. Эквивалент водорода равен 1, кислорода 8. Вычисление молярной массы эквивалента вещества (Мэкв) Молярная масса эквивалентов кислорода О2 Мэкв = 8, молярная масса эквивалентов водорода равна Мэкв = 1 Молярная масса эквивалентов иона равна атомной массе элемента деленной на заряд иона. Например, Мэкв(Ca2+) = 40/2 =20 Молярная масса эквивалентов элемента в составе гидрида равна молекулярной массе элемента деленной на число атомов водорода в химической формуле гидрида. Например, М экв (Cl) в HCl равна 34,5/1 = 34,5 г/моль, М экв (N) в NH3 равна 14/3, М экв (С) в СН4 равна 12/4 = 3 Молярная масса эквивалентов элемента в составе окисла равна молярной массе элемента деленной на степень окисления элемента в химической формуле окисла. Например, М экв (Cu) в Cu2O равна 63,5/1 = 64,5 г/моль, М экв (Cu) в CuO равна 63,5/2 = 31,75 г/моль. Молярная масса эквивалентов окисла Мэкв = A / s + 8 A – атомный вес элемента в составе окисла, s – степень окисления элемента в окисле. Например, Мэкв(N2O) = 14/1 + 8 = 22(г/моль), Мэкв(N2O3) = 14/3 + 8 = 38/3 (г/моль), Мэкв(Fe2O3) = Молярная масса эквивалентов кислоты равна молярной массе кислоты, деленной на число атомов водорода, которые замещаются в данной реакции, на основность кислоты. Например, Мэкв серной кислоты в реакции H2SO4 + Zn = ZnSO4 + H2 равна 98/2 = 49(г/моль); Мэкв серной кислоты в реакции H2SO4 + NaCl = NaHSO4 + HCl равна 98/1 = 98(г/моль)[замещается только один атом водорода]. Молярная масса эквивалентов основания равна молярной массе основания, деленной на число гидроксильных групп: Мэкв (NaOH) = 40/1 = 40(г/моль). Молярная масса эквивалентов соли равна молярной массе соли, деленной на произведение валентности металла в составе соли на число атомов металла в составе соли. Например: Мэкв (BaSO4) = В случае кристаллогидратов при расчете эквивалента соли следует учитывать кристаллизационную воду. Например, Мэкв (CaCl2•6H2O) =
а) Закон эквивалентов утверждает, что массы вступивших в реакцию веществ пропорциональны их эквивалентам, эквиваленты взаимодействующих веществ соответственно. б) Решение задач с использованием закона эквивалентов в) Закон эквивалентов можно записать по- другому: V1×H1 = V2×H2, где V и Н – объём и нормальная концентрация реагентов.
Задача. При восстановлении водородом 0,646 г оксида металла образовалось 0,162 г воды. Записать химическую формулу оксида. Решение: в 0,162 г воды кислорода содержится 0,144 г. Такое количество кислорода потребовалось для образования 0,646 г оксида, следовательно, металла в оксиде 0,646 – 0,144 = 0,502 г. Закон эквивалентов:
химической формуле оксида FeO. Пользуясь растворами, концентрация которых выражена нормальностьюН, легко рассчитать в каких объемных отношениях они должны быть смешаны, чтобы растворенные вещества прореагировали без остатка. Пусть V1 литров раствора вещества 1 с концентрацией Н1 реагирует с V2 л раствора вещества 2 с концентрацией Н2. Чтобы вещества прореагировали без остатка, Н1×V1 = Н2×V2. Задача: Определить концентрацию серной кислоты H2SO4, если для нейтрализации 60 мл кислоты потребовалось 20 мл 0,3Н раствора щелочи. Решение: так как вещества реагируют в эквивалентных количествах, получим: Н1×60 = 0,3×20 Н1 = 0,1. Ответ: концентрация серной кислоты равна 0,1Н. Задача. Вычислить молярную концентрацию раствора Cm, если к 1,5Н раствору щелочи NaOH объемом 1,2 литра добавить 0,4 литра 0,6Н раствора щелочи. Решение: 1,5Н концентрация щелочи равна 1,5/1 = 1,5(моль/л), аналогично 0,6Н = 0,6М. Следовательно, Задача. Вычислить нормальную, молярную и процентную концентрации раствора, если в растворе объемом 400 мл растворили 10,4 г фосфата кальция, Ca3(PO4)2, M(Ca3(PO4)2 = 310; плотность раствора ρ = 1,04(г/мл). Решение: молярная масса эквивалентов соли Мэкв = 310/(2×3) ≈ 52
ω% = 2.2.7. Концентрация, выражаемая титром. Титром называется число граммов растворенного вещества в 1 мл раствора; титр обозначается буквой Т; [Т] = г/мл; Т = m/V, m – масса растворенного вещества в граммах, V – объем раствора в мл или см3. Задача: определить моляльность, нормальность и титр 40% раствора серной кислоты H2SO4, имеющей плотность ρ = 1,307 г/мл. Решение: воспользуемся формулой для пересчета концентраций: δ×ρ = С×М;
|
|||||||
|
Последнее изменение этой страницы: 2021-04-04; просмотров: 92; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.12.36.87 (0.027 с.) |

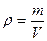 [г/мл], m(г) – масса раствора, V(мл) – объем
[г/мл], m(г) – масса раствора, V(мл) – объем m - масса растворенного вещества; m(R) масса раствора; т.к. масса раствора m(R) = m + m(RS), где m(RS) – масса растворенного вещества, следовательно
m - масса растворенного вещества; m(R) масса раствора; т.к. масса раствора m(R) = m + m(RS), где m(RS) – масса растворенного вещества, следовательно  . Если известна плотность раствора ρ(г/мл), тогда масса раствора m(R) = ρ×V, масса растворенного вещества m(B) = δ×ρ×V
. Если известна плотность раствора ρ(г/мл), тогда масса раствора m(R) = ρ×V, масса растворенного вещества m(B) = δ×ρ×V ; по условию
; по условию , 2х = 3у и х + у = 5; у = 2л, х = 3л.
, 2х = 3у и х + у = 5; у = 2л, х = 3л.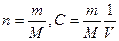 [C] = моль/литр, [m] = г, [V] = литр, М – молярная масса растворенного вещества. Если [V] = мл, тогда
[C] = моль/литр, [m] = г, [V] = литр, М – молярная масса растворенного вещества. Если [V] = мл, тогда 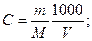
 , если [V] = мл.
, если [V] = мл.
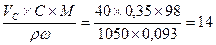 мл.
мл. = 24 мл.
= 24 мл.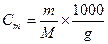 ; m – масса растворённого вещества в граммах, М – молярная масса растворенного вещества, g – масса растворителя в граммах. Если ρ – плотность растворителя, V – объем растворителя, тогда масса растворителя g =ρV и
; m – масса растворённого вещества в граммах, М – молярная масса растворенного вещества, g – масса растворителя в граммах. Если ρ – плотность растворителя, V – объем растворителя, тогда масса растворителя g =ρV и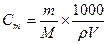 ; [ρ] = г/л, [V] = л., [m] = грамм.
; [ρ] = г/л, [V] = л., [m] = грамм. (г/моль); Мэкв(СО2) = 12/4 + 8 = 11(г/моль).
(г/моль); Мэкв(СО2) = 12/4 + 8 = 11(г/моль). (г/моль), Мэкв (Al2(SO4)3) =
(г/моль), Мэкв (Al2(SO4)3) =  ; в 1Н растворе соли должно содержаться 57 г Al2(SO4)3 в одном литре раствора. В рассмотренных примерах мы считаем, что все атомы металла замещаются атомами водорода. Но это совсем необязательно. Например, молярная масса эквивалентов фосфата натрия Na3PO4 в реакции Na3PO4 + 2HCl = NaH2PO4 + 2NaCl М экв = 164/2, т.к. в реакции замещаются 2 атома натрия.
; в 1Н растворе соли должно содержаться 57 г Al2(SO4)3 в одном литре раствора. В рассмотренных примерах мы считаем, что все атомы металла замещаются атомами водорода. Но это совсем необязательно. Например, молярная масса эквивалентов фосфата натрия Na3PO4 в реакции Na3PO4 + 2HCl = NaH2PO4 + 2NaCl М экв = 164/2, т.к. в реакции замещаются 2 атома натрия. (г/моль) [валентность кальция 2, число атомов кальция 1].
(г/моль) [валентность кальция 2, число атомов кальция 1].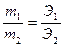 где m1, m2 и Э1 и Э2 – массы и
где m1, m2 и Э1 и Э2 – массы и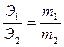 ,
, ; эквивалент металла в оксиде Э1 = 27,89. Это соответствует
; эквивалент металла в оксиде Э1 = 27,89. Это соответствует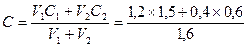 = 1,275 (моль/л).
= 1,275 (моль/л). 0,5(моль/л);
0,5(моль/л); 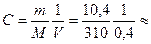 0,08 (моль/л)
0,08 (моль/л)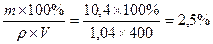 .
.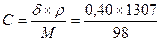 ; С = 5,33(моль/л). Для серной кислоты Н = 2С = 10,66 (моль/л). Титр – это число граммов кислоты в 1 мл; т.к. у нас кислоты 5,33 моля, а это 5,55×98 = 522,34 г в 1 литре; Т = 522,34/1000 = 0,52234 г/мл.
; С = 5,33(моль/л). Для серной кислоты Н = 2С = 10,66 (моль/л). Титр – это число граммов кислоты в 1 мл; т.к. у нас кислоты 5,33 моля, а это 5,55×98 = 522,34 г в 1 литре; Т = 522,34/1000 = 0,52234 г/мл.


