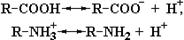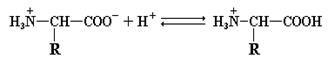Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Методические указания к лабораторному практикуму по курсуСодержание книги
Поиск на нашем сайте «Общая и экологическая биохимия» Раздел «Аминокислоты. Пептиды. Белки» Лабораторная работа № 1
Оборудование и материалы: · Термостат · Камера хроматографическая · Бумага хроматографическая · Пипетки стеклянные на 1мл и 5 мл · Микропипетки автоматические · Цилиндры мерные на 250мл и 100мл · Колба емкостью 250мл · Пробирки · Штативы для пробирок · Бумага фильтровальная · Индикаторная бумага универсальная · Сито нейлоновое · Ванночка со льдом
Реактивы: · Яичный белок · Гидроксид натрия (NaOH), 10% раствор, 14.3 М раствор · Сульфат меди (CuSO4), 2% раствор, 0.04М раствор · Ацетат свинца (Pb(CH3COO)2), раствор · Нитрит калия (натрия) (KNO2, NaNO2), 0.5% раствор · Карбонат натрия (Na2CO3), 10% раствор · Нитропруссид натрия (Na2[Fe(CN)5NO]), 10% раствор · Нингидрин, 1% раствор · Реактив Миллона · a-нафтол, 0.2% спиртовой раствор · Сульфониловая кислота, 1% раствор в 5% соляной кислоте
Теоретическая Часть
Аминокислоты
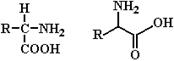
В процессах жизнедеятельности клетки главенствующую роль играют белки – биополимеры, построенные из мономерных единиц – L- a-аминокислот. Биологические свойства белков определяются, в основном, их аминокислотным составом, точнее порядком расположения аминокислот в полипептидной цепи, что в конечном итоге определяет пространственную структуру белка. Основными функциональными группами аминокислот являются их амино- и карбоксильные группы, которые связаны с одним и тем же (a) углеродным атомом (рис. 1.1).
Рис. 1.1 Два варианта изображения структурной формулы аминокислоты.
За исключением глицина, у которого R (см. рис. 1.1) представлен атомом водорода, у всех остальных протеиногенных аминокислот четыре группы, связанные с a-углеродным атомом, различны. Благодаря тетраэдрическому расположению четырех разных заместителей у a-углеродного атома, любая аминокислота (кроме глицина) обладает оптической активностью. При этом одни аминокислоты, входящие в состав белков, являются (при рН 7.0) право-вращающими, а другие – лево-вращающими. Тем не менее, вследствие того, что природные аминокислоты имеют пространственную конфигурацию L-глицеральдегида, все они относятся к L-a-аминокислотам.
Ионные формы аминокислот
Свободные аминокислоты включают, по крайней мере, две слабоионизованные группы: карбоксильную группу (–СОО¯) и аминогруппу (–NН3+). В растворе эти группы находятся в двух формах, заряженной и незаряженной, между которыми поддерживается протонное равновесие:
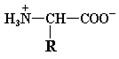
R–COOH и R–NH3+ являются протонированными партнерами, то есть кислотами, а R–COO¯ и R–NH2 – сопряженными основаниями (т.е. акцепторами протонов) соответствующих кислот. Следовательно, структура аминокислоты, изображенная на рис. 1.1, не может существовать в растворе, поскольку одна из указанных групп в той или иной степени ионизирована. Вполне понятно, что суммарный заряд (алгебраическая сумма всех положительных и отрицательных зарядов) аминокислоты зависит от величины рН, то есть от концентрации протонов в растворе. Значение рН, при котором суммарный заряд аминокислоты равен нулю и она не перемещается в постоянном электрическом поле, называется ее изоэлектрической точкой (р I). Такая в целом незаряженная форма аминокислоты носит название цвиттериона. Для алифатических аминокислот цвиттерион имеет следующий вид:
При увеличении или уменьшении рН по отношению к изоэлектрической точке происходит «перезарядка» аминокислоты и она утрачивает форму цвиттериона. В случае подкисления раствора, степень ионизации карбоксильной группы резко падает и аминокислота выступает в роли основания, присоединяя протоны.
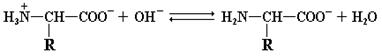
При повышении рН происходит обратный процесс: аминокислота, выступая в качестве кислоты, протоны отдает.
|
||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 158; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.134 (0.009 с.) |