Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Построение калибровочных графиковСодержание книги
Поиск на нашем сайте
Биуретовый метод Таблица 1
Метод Лоури Таблица 2
Метод Брэдфорд Таблица 3
Приложение Строение и номенклатура аминокислот В природных объектах обнаружено около 300 аминокислот, однако только 20 из них – протеиногенных – входит в состав белков (см. таблицу в Приложении). В таблице показаны структуры этих аминокислот, а также их трехбуквенные и однобуквенные обозначения, которые широко используют-ся в биохимической литературе. Однобуквенные обозначения применяются для записи наиболее длинных аминокислотных последовательностей (например, полных аминокислотных последовательностей белков). В настоящее время существует множество различных принципов классификации аминокислот. Рассмотрим некоторые из них.
I. Классификация, учитывающая строение радикала и функциональных групп 1. Ациклические аминокислоты: 1) Моноаминомонокарбоновые аминокислоты (глицин, аланин, серин, цистеин, метионин, треонин, лейцин, изолейцин, валин); 2) Моноаминодикарбоновые аминокислоты (аспарагиновая кислота, глутаминовая кислота); 3) Диаминомонокарбоновые аминокислоты (лизин, аргинин). 2. Циклические аминокислоты: 1) Гомоциклические (фенилаланин, тирозин); 2) Гетероциклические (триптофан, гистидин).
II. Классификация ациклических аминокислот по числу углеродных атомов в молекуле (“семейства” аминокислот) 1. С2 – глицин; 2. С3 – аланин, серин, цистеин; 3. С4 – треонин, метионин, g-аминомасляная кислота, аспарагиновая кислота, аспарагин; 4. С5 – валин, глутаминовая кислота, глутамин, аргинин; 5. С6 – лизин, лейцин, изолейцин.
III. Классификация аминокислот по полярности, входящих в их состав радикалов 1. Полярные 1) Незаряженные: аминокислоты, содержащие в боковых цепях гидроксильные группы (серин, треонин, тирозин), атом серы (цистеин, метионин), а также амиды кислых аминокислот (глутамин, аспарагин). 2) Заряженные: это кислые (аспарагиновая кислота, глутаминовая кислота) и основные (лизин, аргинин, гистидин) аминокислоты.
2. Неполярные (гидрофобные) К этой группе относятся алифатические (глицин, аланин, валин, лейцин, изолейцин) и ароматические (фенилаланин, триптофан, пролин) аминокислоты. Протеиногенные аминокислоты
Название |
Формула |
Сокращенное обозначение |
Название |
Формула |
Сокращенное обозначение | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Русское | Английское | Русское | Английское | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Аминокислоты с алифатическими боковыми цепями | Аминокислоты с боковыми цепями, содержащие атом серы | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
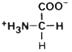
| Глицин |
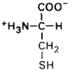
| Гли | Gly (G) | Цистеин 2) |
| Цис | Cys (C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
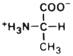
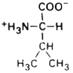
| Аланин |
| Ала | Ala (A) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
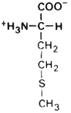
| Метионин |
| Мет | Met (M) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
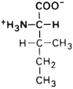
| Валин |
| Вал | Val (V) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Лейцин |
| Лей | Leu (L) | Аминокислоты с боковыми цепями, содержащими кислые группы или их амиды | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
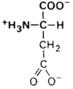
| Аспараги-новая кислота |
| Асп | Asp (D) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
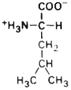
| Изолейцин |
| Илей | Ile (I) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
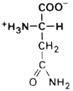
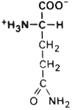
| Аспарагин |
| Асн | Asn (N) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Аминокислоты с боковыми цепями, содержащими гидроксильные (-ОН) группы 1) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
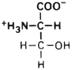
| Серин |
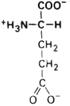
| Сер | Ser (S) | Глутами-новая кислота |
| Глу | Glu (E) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
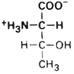
| Треонин |
| Тре | Thr (T) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Глутамин |
| Глн | Gln (Q) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Аминокислоты с боковыми цепями, содержащими основные группы | Аминокислоты, содержащие ароматические кольца | ||||||||
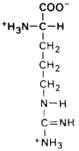
| Аргинин |
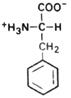
| Арг | Arg (R) | Фенилаланин |
| Фен | Phe (F) | ||
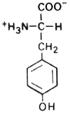
| Тирозин |
| Тир | Tyr (Y) | ||||||
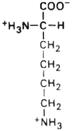
| Лизин |
| Лиз | Lys (K) | ||||||
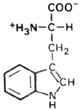
| Триптофан
|
| Три | Trp (W) | ||||||
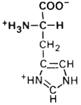
| Гистидин |
| Гис | His (H) | ||||||
| Иминокислоты | |||||||||
| Пролин | 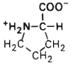
| Про | Pro (P) | ||||||
1) – сюда же можно отнести тирозин, который имеет фенильную груп-пировку;
2) – к этой группе аминокислот относится цистин, который состоит из двух остатков цистеина связанных между собой дисульфидной связью.
Учебное издание
Бокуть Сергей Борисович,
Ячник Наталия Николаевна,
Шейко Людмила Михайловна,
Сяхович Виталий Эдуардович
Практикум по
|
| Поделиться: |