
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Методика расчета кинетических закономерностей и термодинамических параметров реакции ацилирования целлюлозосодержащего сырья смесью «о-аминобензойная кислота - тионилхлорид - трифторуксусная кислота»
С целью установления некоторых кинетических закономерностей протекания реакции ацилирования проводили расчет констант скорости реакции. Реакция ацилирования данной системой начинается в гетерогенной среде, а также проходит на поверхности макромолекулы целлюлозы и, следовательно, является топохимической, поэтому обработку кинетических данных проводили по уравнению Ерофеева-Колмогорова [39]: ln[-ln(1-α)] = lnk + n∙lnτ, (2.5)
где α - степень превращения гидроксильных групп в сложноэфирные;- эмпирический коэффициент, сопоставляемый с константой скорости реакции;- эмпирический коэффициент, учитывающий число элементарных стадий при превращении зародыша в активно растущее ядро и число направлений, в которых растут ядра; τ - время синтеза. Степень превращения рассчитывали по формуле [40]:
где СЗ - степень замещения по АКК в полученных сложных эфирах целлюлозы в момент времени τ; СЗmax - максимальная степень замещения ОН-групп целлюлозы равная 3. В данных условиях реакции наблюдаются линейные зависимости между ln[-ln(1-a)] и lnt на основании которых определяли константу скорости и lnK с применением метода Саковича по уравнению: К=n∙k1/n, (2.7) где n и k - эмпирические коэффициенты уравнения Ерофеева-Колмогорова;- константа скорости реакции, с-1. Термодинамические параметры реакции ацилирования вычисляли на основании уравнения Эйринга при построении графика в координатах
где К - константа скорости, с-1; ћ - постоянная Планка, 6,62∙10-34 Дж∙с; Т - температура, К; Кb - постоянная Больцмана, 1,38∙10-23 Дж/К; ∆S¹ - энтропия активации, Дж/(моль∙К);- универсальная газовая постоянная 8,31 Дж/(моль∙К); ∆Н¹ - энтальпия активации.
Изучение адсорбции ионов металлов
Навески адсорбентов массой 0,01 г помещали в колбы и заливали 50 мл раствором исследуемой соли в различных концентрациях, и выдерживали в течении 24 часов. Равновесную концентрацию ионов металлов определяли колориметрическим методом, в соответствии с ГОСТ 4388-72 для ионов Cu2+, ГОСТ18293-72 для ионов Pb2+ , ГОСТ 23862.31-79 для ионов Th4+ . Обсуждение результатов
Проводимые на кафедре ТППиЭ АлтГТУ в течение нескольких лет исследования, показали возможность получения СЭЦ из целлюлозосодержащего сырья - древесины. В связи с тем, что получение лигнина с ароматическими кислотами не исследовано, представлялось интересным изучить взаимодействие лигнина с ароматическими кислотами, в частности с о-аминобензойной кислотой.
Целью нашей работы было получение сложных эфиров лигнина с оАБК в среде «трифторуксусная кислота - тионилхлорид». Взаимодействие лигнина с ароматическими аминокислотами позволяет получить практически значимые продукты лигнина, которые могут быть использованы в различных областях народного хозяйства. Сульфатный лигнин в ходе проделанной работы обрабатывался ацилирующей смесью: о-аминобензойная кислота - трифторуксусная кислота - тионилхлорид. Трифторуксусная кислота в процессе ацилирования лигнина выполняет роль растворителя и катализатора реакции. Процесс ацилирования можно представить следующими стадиями: взаимодействие о-аминобензойной кислоты с ТФУК при интенсивном перемешивании;
добавление тионилхлорида к смеси и выдерживание при постоянной температуре до полного взаимодействия:
По окончании реакции ацилированный лигнин высаждали в воду, промывали до нейтральной среды, высушивали и доводили до постоянной массы. В полученных соединениях определяли выход (в %), количество связанной о-аминобензойной кислоты. Количество полученного продукта определяли в процентах относительно исходной навески лигнина по формуле:
где m1 - масса полученного продукта; m0 - исходная навеска лигнина В таблице 1 приведены результаты определения выхода продукта ацилирования лигнина смесью «о-АБК - ТФУК - ТХ». Таблица 1 - Количество полученного продукта в процентах относительно исходной навески лигнина
В процессе ацилирования выход продукта составляет выше 100 % относительно исходной навески лигнина. Возрастание массы ацилированного лигнина происходит за счет присоединения ароматической кислоты, при этом возрастание выхода продукта с повышением времени и температуры синтеза коррелируется с данными по содержанию связанной кислоты.
Для определения связанной кислоты использован метод потенциометрического титрования. По данным химического анализа на содержание связанной о-аминобензойной кислоты рассчитано количество связанных гидроксильных групп в лигнине, представленное в таблице 2.
Таблица 2 - Количество связанных гидроксильных групп в лигнине
Приведенные данные показывают, что с увеличением температуры и продолжительности синтеза возрастает количество связанных гидроксильных групп в лигнине. Как видно из полученных данных, количество прореагировавших гидроксильных групп лигнина больше исходного количества свободных алифатических и ароматических групп в чистом лигнине. Это связано с тем, что реакция протекает не только по свободным гидроксильным группам, но и по метоксильным и простым эфирным связям, которые становятся не устойчивыми в процессе ацидолиза. Реакция ацилирования данной системой начинается в гетерогенной среде и проходит на поверхности макромолекулы лигнина и является топохимической, поэтому обработку кинетических данных проводили по уравнению Ерофеева-Колмогорова:
ln[-ln(1 - α)] = lnk + n · lnτ, (3.2)
где α - степень превращения гидроксильных групп в сложноэфирные;- константа скорости реакции;- эмпирический коэффициент, учитывающий число элементарных стадий при превращении зародыша в активно растущее ядро и число направлений, в которых растут ядра; τ - время синтеза. Степень превращения рассчитывается по формуле:
где Сон - количество замещенных гидроксильных групп в полученных сложных эфирах лигнина в момент времени τ; Сон max - максимальное количество гидроксильных групп в лигнине, равное 34. Кинетика процесса ацилирования рассмотрена по уравнению 3.2 для топохимических реакций. По кинетической зависимости, представленной на рисунке 2, определены константы скорости реакции (коэффициент корреляции 0,94-0,97).
- 250С; 2 - 350С; 3 = 450С; 4 = 550С Рисунок 2 - Кинетические анаморфозы реакции ацилирования лигнина о-аминобензойной кислотой
В данных условиях реакции наблюдаются линейные зависимости (рисунок 1) между ln[-ln(1-a)] и ln t, на основании которых определяется lnK с применением метода Саковича по уравнению 3.4.
К = n∙k1/n, (3.4)
где n и k - эмпирические коэффициенты уравнения Ерофеева-Колмогорова;- константа скорости реакции в с-1. Термодинамические параметры реакции ацилирования вычисляли на основании уравнения Эйринга (3.5) при построении графика в координатах
Где К - константа скорости, ћ - постоянная Планка (6,62·10-34 Дж·с), Т - температура (К), Кb - постоянная Больцмана (1,38·10-23 ·Дж / К), ∆S¹ - энтропия активации (Дж / (моль·К)),- универсальная газовая постоянная (8,31 Дж / (моль·К), ∆Н¹ - энтальпия активации.
Рисунок 3 - Зависимость константы скорости реакции ацилирования лигнина о-аминобензойной кислотой от температуры
Значение термодинамических параметров для реакции ацилирования лигнина о-аминобензойной кислотой составило для теплового эффекта реакции DH = 313 кДж/моль, энтропия активации DS = 612 Дж/моль·К. По найденным параметрам рассчитана свободная энергия Гиббса активации переходного комплекса реакции ацилирования лигнина м-аминобензойной кислотой, ее значение составляет 121,44 кДж/моль. Полученное значение энтальпии активации указывает на энергетические затраты, необходимые для диффузии ацилирующего агента к гидроксилам лигнина и образования переходного комплекса. Исходя из полученного значения энтропии активации, можно предположить, что происходит быстрое разрушение активированного комплекса с переходом в продукты реакции. Вычисленное значение энергии Гиббса активации переходного комплекса коррелируется с ранее полученными данными по сложным эфирам целлюлозы, синтезированными из древесины осины. Исходя из этого можно сделать предположение, что на реакцию ацилирования ароматическими кислотами не оказывает влияние вид растительного сырья (древесина, целлюлоза, лигнин), поскольку общая энергетика процесса имеет одинаковое значение. Анализ ацилированного лигнина методом ИК - спектроскопии (рисунок 4) показал наличие полос поглощения в области 3600-3400 см-1 характерных для полос поглощения валентных колебаний NH2 и OH-групп, при этом интенсивность полосы поглощения значительно ниже, чем у чистого лигнина и смещена к области 3200 см-1, что говорит о преобладании аминогрупп введенной кислоты. Полоса поглощения в области 1730 - 1750 см-1, имеющая большую интенсивность, характерна для валентных колебаний СО - групп в сложных эфирах, и подтверждает образование о-аминобензоата лигнина с высоким содержанием в связанном виде о-аминобензойной кислоты. Присутствие полос поглощения в областях 1610 - 1450 см-1, ответственных за колебания ароматического кольца, обосновывается присутствием структурных единиц остаточного лигнина, увеличивают свою интенсивность в связи с введением ароматической кислоты. Полоса поглощения в области 1730 см-1 увеличивает свою интенсивность с ростом температуры и продолжительности синтеза, что подтверждает увеличение количества прореагировавших гидроксильных групп лигнина. В ходе проведенных экспериментов были получены о-аминобензоаты лигнина с содержанием о-аминобензойной кислоты до 32 % от массы ацилированного лигнина. Методом ИК-спектроскопии доказано образование о-аминобензоата лигнина.
Для полученных о-аминобензоатов лигнина, а также чистого лигнина были изучены сорбционные свойства на ионы поливалентных металлов: Cu2+, Pb2+, Th4+ (приложение Б). Предельная адсорбция насыщения и энергия адсорбции для различных ионов была рассчитана по уравнению Дубинина-Радушкевича (3.6) (таблица 3).
где А - величина равновесной адсорбции, мг/г; А0 - величина предельной адсорбции, мг/г;- универсальная газовая постоянная 8,31 Дж/(моль∙К); Т - температура, К; Е - энергия адсорбции катионов металлов, Дж/моль; С0 - исходная концентрация, мг/л; С - концентрация после адсорбции, мг/л;
Таблица 3- Предельная адсорбция насыщения и энергия адсорбции
Для определения предельной сорбционной емкости сорбента и исследования влияния температуры на распределение ионов меди в гетерогенной системе водный раствор - сорбент были получены изотермы сорбции тяжелых металлов при комнатных температурах. В исследованных процессах ионного обмена на сорбенте концентрация подвижных ионов в фазе сорбента при равновесии соизмерима с избыточной адсорбцией. Экспериментальные изотермы были обработаны в рамках модели сoрбции ТОЗМ. Обработка линейных зависимостей (lnA -ln(Cs/Cp) методом наименьших квадратов свидетельствует, что модель ТОЗМ удовлетворительно (с коэффициентом корреляции 0,97 - 0,99) описывает процесс, однако, дает несколько завышенные величины предельной сорбции. Известно, что предельная сорбция на немодифицированных лигноцеллюлозных сорбентах не превышает 1 моль/кг. Эта величина согласуется с содержанием карбоксильных групп в сорбенте. Вероятно, причина завышенной величины предельной сорбции по модели ТОЗМ связана с ионообменным механизмом сорбции ионов металлов целлюлозосодержащим сорбентом. Рассчитанные энергии адсорбции в ряду увеличения радиуса ионов согласуются с рядами Гофмейстера. Данное обстоятельство также свидетельствует о применимости ТОЗМ не только для целлюлозных сорбентов, но и для лигнина и его производных. Анализ ЯМР-спектров позволяет выделить следующие сигналы интенсивности в области: 170 м.д - появляется связь СОО, которая не наблюдается в чистом лигнине, таким образом подтверждается образование аминобензоатов лигнина; 158 м.д. - Сар-О - простая эфирная ароматическая связь; 140-120 м.д. - сигналы атомов углерода в ароматическом кольце структурных единиц лигнина и введённой аминокислоты., в отличие от чистого лигнина увеличивается интенсивность сигналов модифицированного лигнина в этих областях; 105 - 75 м.д. - СН2О алифатическая; 64-50 м.д. - метоксильная связь, эти сигналы исчезли в ацилированном лигнине, потому что реакция ацилирования проходит также и по простым эфирным связям.
ЯМР спектр сульфатного лигнина представлен в приложении В.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2020-03-14; просмотров: 124; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.222.109.213 (0.031 с.) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 , (2.6)
, (2.6)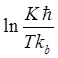 от 1/Т.
от 1/Т. (2.8)
(2.8)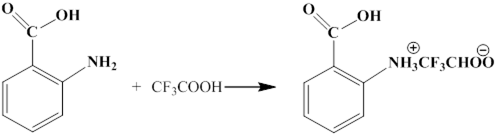
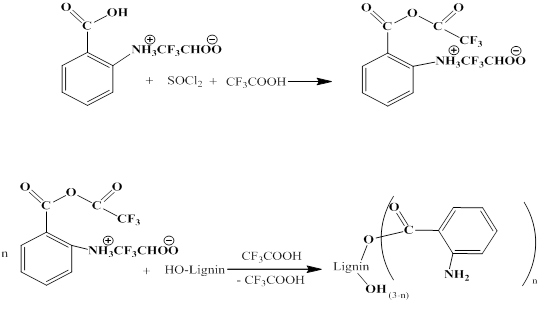
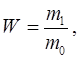 (3.1)
(3.1)
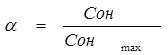 , (3.3)
, (3.3)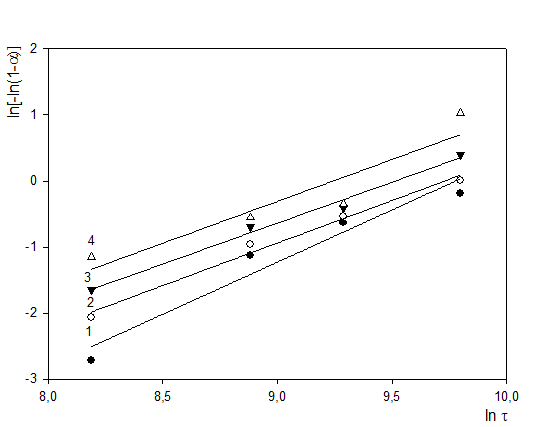
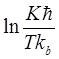 от 1/Т и на основании данного уравнения определяли энергию и энтропию активации.
от 1/Т и на основании данного уравнения определяли энергию и энтропию активации.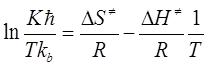 , (3.5)
, (3.5)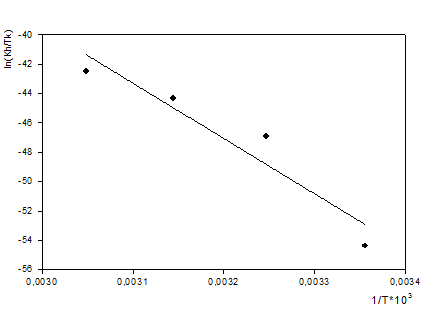
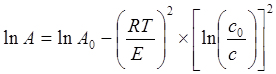 , (3.6)
, (3.6)


