Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Определить, образуется ли осадок хлорида свинца (II), если к 0,05 М раствору нитрата свинца (II) добавить равный объем 0,02 М раствора хлороводородной кислоты.Содержание книги
Поиск на нашем сайте
с
С учетом увеличения объема раствора при сливании в 2 раза:
с
с
с
Так как 2,5·10 Ответ: осадок PbCl2 не образуется. 3. Составить схему коррозионного ГЭ, возникающего при контакте оловянной пластинки площадью 35 см2 с медной в растворе соляной кислоты. Написать уравнения электродных процессов и суммарной реакции процесса коррозии. а) Вычислить объемный и весовой показатели коррозии, если за 70 мин в процессе коррозии выделилось 1,5 см3 газа (н.у.). б) Вычислить весовой и глубинный показатели коррозии, если за 80 мин потеря массы корродируемого металла составила 5,6 ∙10-3 г. Плотность металла 7,3 г/см3.
Решение По таблице находим значения стандартных электродных потенциалов олова (II) и меди (II):
Так как Составим схему коррозионного ГЭ:
А(-)Sn │ HCl │ Cu(+)K или А(-)Sn │ H+ │ Cu(+)K
Cоставляем уравнения электродных процессов и суммарной реакции процесса коррозии:
На A(-)Sn – 2ē = Sn2+ На К(+)2Н+ + 2ē = Н2
Sn + 2H+ = Sn2+ + H2
Sn + 2HCl = SnCl2 + H2 – суммарная реакция процесса коррозии. а) Рассчитываем объемный показатель коррозии (KV) по формуле
Из уравнения суммарной реакции процесса коррозии следует, что при коррозии выделяется водород. Следовательно, V газа = Тогда
K V =
Рассчитываем весовой показатель коррозии K m по формуле
K m = В процессе коррозии разрушению подвергается олово и выделяется водород. Следовательно:
М эк(Ме) = М эк(Sn) =
K m =
Ответ: K V = 367,3 см3/м2∙ч. K m = 1,95 г/м2∙ч.
б) Рассчитываем весовой показатель коррозии K m по формуле
При расчете K m принимаем
Тогда
K m =
Рассчитываем глубинный показатель коррозии по формуле
П =
Ответ: K m = 1,2 г/м2∙ч, П = 1,44 мм/год. МЕТАЛЛЫ V–VI ГРУППЫ УРОВЕНЬ А 1. Определить степень окисления всех элементов в соединениях WO2, WBr5, (NH4)2WO4.
Ответ: + 4 -2 +5-1 -3+1 +6-2 WO2, WBr5, (NH4)2WO4
Как изменяются кислотно-основные свойства гидроксидов хрома с увеличением его степени окисления в ряду Сr+2, Сr+3, Сr+6?
основание HCrO2 кислота амфотер. гидроксид
|
||||||||||||||||
|
Последнее изменение этой страницы: 2017-02-21; просмотров: 433; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.217.116 (0.008 с.) |

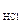 = 0,02 M
с
= 0,02 M
с 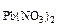 = 0,05 M
= 0,05 M
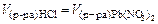
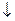 + 2HNO3.
Осадок PbCl2 образуется только в случае, если
+ 2HNO3.
Осадок PbCl2 образуется только в случае, если
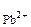 · с
· с 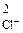 > ПР
> ПР  = 2·10
= 2·10 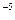 (таблица).
(таблица).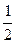 с
с 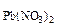 ·
· 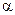 · n
· n 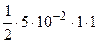 = 2,5·10-2 моль/л;
= 2,5·10-2 моль/л;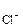 =
= 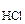 ·
· 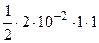 = 1·10-2 моль/л;
= 1·10-2 моль/л;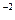 ·(1·10
·(1·10 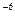 .
.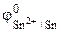 = – 0,14 В,
= – 0,14 В, 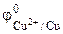 = 0,34 В.
= 0,34 В.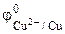 , то анодом в коррозионном ГЭ будет олово, катодом – медь.
, то анодом в коррозионном ГЭ будет олово, катодом – медь.

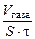 , см3/м2∙час.
При расчете K V принимаем:
S – площадь поверхности анода, м2;
τ – время процесса коррозии, ч;
V газа – объем выделившегося газа, см3.
, см3/м2∙час.
При расчете K V принимаем:
S – площадь поверхности анода, м2;
τ – время процесса коррозии, ч;
V газа – объем выделившегося газа, см3.
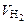 .
.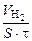 =
= 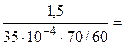 367,3 см3/м2∙ч.
367,3 см3/м2∙ч.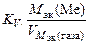 , г/м2∙ч.
, г/м2∙ч.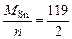 = 59,5 г/моль,
= 59,5 г/моль, = 11200 см3/моль.
= 11200 см3/моль.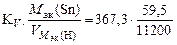 = 1,95 г/м2∙ч.
= 1,95 г/м2∙ч. 5,6∙10-3 г
S = 35 см 2
ρMe = 7,3 г/см3
5,6∙10-3 г
S = 35 см 2
ρMe = 7,3 г/см3
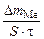 , г/м2∙ч.
Коррозии подвергается олово.
Тогда потеря массы металла
, г/м2∙ч.
Коррозии подвергается олово.
Тогда потеря массы металла
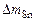 .
.
 – г; S – м2, τ – ч.
– г; S – м2, τ – ч.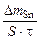 =
= 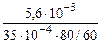 = 1,2 г/м2∙ч.
= 1,2 г/м2∙ч. =
= 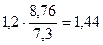 мм/год.
мм/год.