
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Глава V. Химическое равновесие в гетерогенных системахСодержание книги
Поиск на нашем сайте
5.1. Использование процессов образования и растворения осадков в анализе Реакции осаждении лежат в основе ряда аналитических операций и широко используются для различных целей анализа: 1. Обнаружение ионов в растворе (осадок – аналитический сигнал) по образованию осадков определенного цвета или структуры (микрокристаллоскопия). Например: а) гексацианоферрат (II) калия K4[Fe(CN)6] в слабокислой среде образует с ионами железа (III) темно-синий осадок гексацианоферрата (II) железа (III) (берлинская лазурь): 4Fe3+ + 3[Fe(CN)6]4- → Fe4[Fe(CN)6]3↓; б) оксалат аммония дает в растворах с солями кальция белый кристаллический осадок оксалата кальция, нерастворимый в уксусной кислоте: Са2+ + С2О42- → СаС2О4↓; в) гексанитрокобальтат (III) натрия Na3[Co(NO2)6] образует с солями калия в нейтральной среде кристаллический осадок желтого цвета К2Na[Co(NO2)6]: 2К+ + Na3[Co(NO2)6] → К2Na[Co(NO2)6] ↓ + 2Na+; г) сульфат-ионы с ионами кальция образуют белый кристаллический осадок CaSO4·2H2O. Игольчатые кристаллы в виде пучков или звездочек наблюдаются под микроскопом; д) ионы J- образуют с ионами свинца (II) в уксуснокислой среде желтый осадок в виде блестящих золотистых кристаллов: Pb2+ + 2J- → PbJ2↓ 2. Разделение катионов и анионов на аналитические группы. Сложные смеси веществ, используя реакции осаждения, можно разделить на группы в 3-5 ионов. Разделение на группы в значительной степени облегчает анализ, делает его систематическим. Для такого разделения подбираются соответствующие групповые реагенты. В зависимости от избранной классификации, это могут быть сульфид-ионы, карбонат-ионы, фосфат-ионы и т.д. Кислотно-щелочная классификация базируется на получении осадков хлоридов, сульфатов, гидроксидов катионов. Например: а) по кислотно-щелочной классификации для разделения смеси ионов NH4+, K+, Na+, Ag+, [Hg2]2+, Pb2+ к исследуемому раствору добавляют 2 М раствор соляной кислоты. Хлориды серебра, свинца, ртути (I) выделяются в виде осадка белого цвета (AgCl, PbCl2, Hg2Cl2), а хлориды ионов NH4+, K+, Na+ остаются в фильтрате. В дальнейшем каждая группа анализируется отдельно; б) анионы 2-ой (Cl-, Br-, J-, S2-) и 3-ей (NO3-, NO2-, CH3COO-) аналитических групп можно разделить, вводя в исследуемый раствор нитрат серебра в присутствии азотной кислоты. При этом соли серебра анионов 2-ой группы выпадают в осадок, а 3-ей остаются в растворах. 3. Удаление мешающих ходу анализа ионов. Например: а) присутствие в исследуемом растворе катионов бария мешает открытию ионов кальция и стронция, поэтому катионы бария удаляются при его открытии хроматом калия в уксуснокислой среде. Осадок хромата бария отфильтровывается, а в фильтрате затем открывают ионы Sr2+, Ca2+; б) присутствие ионов Sr2+ мешает открытию ионов Ca2+. К исследуемому раствору приливают раствор сульфата аммония. При этом катионы стронция практически полностью переходят в осадок SrSO4, а основная часть катионов кальция остается в растворе в виде непрочного комплексного иона [Сa(SO4)2]2- и иона Ca2+. Ионы кальция открывают в центрифугате после отделения осадка SrSO4; в) для открытия ионов магния в растворе, содержащем ионы железа, марганца, висмута, сурьмы, используют способность соединений Mg(OH)2 и (MgOH)2CO3 растворяются в солях аммония. К исследуемому раствору приливают хлорид или нитрат аммония, затем карбонат аммония. В осадок выпадают карбонаты железа, висмута, сурьмы, марганца, а катионы магния остаются в растворе, и после отделения осадка их можно открыть в фильтрате действием раствора гидрофосфата натрия Na2HPO4 механизм растворения гидроксидов, подобных Mg(OH)2 рассмотрен в §5 этой главы; 4. Исследование свойств осадков: растворимость, способность образовывать пересыщенные растворы, зависимость растворимости от температуры, растворимость в кислотах, щелочах и других растворителях. 5. Выделение из смеси соединений определяемых элементов с последующим их концентрированием из сильно разбавленных растворов. 6. Количественное определение ионов путем выделения в виде малорастворимых соединений, соответствующей их обработки (промывание, фильтрование, прокаливание) и взвешивания на аналитических весах (гравиметрия). 7. Количественное определение ионов в виде малорастворимых соединений путем титрования исследуемого раствора стандартным раствором реагента (Объемный анализ. Метод осаждения).
5.2. Равновесие в системах осадок Û раствор. Произведение растворимости. Константа растворимости При аналитических исследованиях очень важно знать последовательность осаждения ионов из раствора, полноту осаждения, растворимость осадков, условия образования осадков, условия переведения того или иного вещества в другие малорастворимые электролиты или в раствор. Абсолютно нерастворимых веществ в природе не существует. В насыщенном растворе между осадком и раствором над ним устанавливается динамическое равновесие: KtAn↓ ↔ Kt+ + An-* (насыщенный раствор) Для бинарного электролита согласно закону действующих масс, учитывая, что поверхность осадка постоянна, можно записать:
ПРа (К sо) – произведение растворимости – важнейшая аналитическая константа, характеризующая основную закономерность равновесного процесса в системе осадок Û раствор, называемую правилом произведения растворимости: произведение активностей ионов малорастворимого электролита в его насыщенном водном растворе при постоянной температуре является постоянной величиной. В общем случае для электролита типа KtmAnn с учетом стехиометрических коэффициентов для реакции: KtmAnn↓ ↔ mKt+ + nAn- произведение растворимости запишется:
Учитывая, что получаем: Для малорастворимых соединений (Р<10-4 моль/л) и для бинарных электролитов (ПР≤10-8) в отсутствии других сильных электролитов ионная сила раствора (µ) мала, коэффициенты активности (fi) приближаются к 1, и для необходимых расчетов можно пользоваться упрощенным выражением:
По величине произведения растворимости можно судить о растворимости электролитов. Чем больше величина произведения растворимости, тем больше и растворимость данного соединения. Но делать выводы о большей или меньшей растворимости (в моль/л) веществ по величинам произведений растворимости можно только для однотипных электролитов. Например, сравнивая значения произведений растворимости следующих веществ:
Самая меньшая растворимость из приведенных соединений у сульфида железа. Выбор наиболее чувствительных осадителей также можно осуществить по величинам произведений растворимости. Например, для решения вопроса, каким из анионов полнее можно осадить ион Ba2+, сравнивают произведения растворимости ряда соединений:
В данном случае наиболее полное осаждение достигается при использовании ионов SO42-. Причем чувствительность ионов осадителей повышается в следующей последовательности: C2O42- < CO32- < CrO42- < SO42- Для катионов кальция чувствительность тех же анионов увеличивается в другой последовательности: CrO42- < SO42- < CO32- < C2O42-; т.к. Сравнивая произведения растворимости хроматов бария и кальция, можно увидеть, что после осаждения ионов Ва2+ в растворе останутся ионы кальция.
|
||||
|
Последнее изменение этой страницы: 2017-02-08; просмотров: 371; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.20 (0.01 с.) |

 (V.I)
(V.I)
 ;
; 
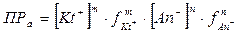 (V.2)
(V.2)
 = 1,78·10-10;
= 1,78·10-10;  = 1,1·10-10;
= 1,1·10-10;  = 8,3·10-17;
= 8,3·10-17; 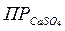 = 9,1·10-6;
= 9,1·10-6;  = 5,0·10-18, можно расположить их по степени уменьшения растворимости (в моль/л) в следующий ряд:
= 5,0·10-18, можно расположить их по степени уменьшения растворимости (в моль/л) в следующий ряд: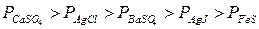
 = 1,2·10-10;
= 1,2·10-10; = 5,1·10-9;
= 5,1·10-9;  = 1,1·10-7.
= 1,1·10-7. = 7,1·10-4;
= 7,1·10-4;  = 4,8·10-9;
= 4,8·10-9;  = 2,3·10-9.
= 2,3·10-9.


