

Мы поможем в написании ваших работ!
ЗНАЕТЕ ЛИ ВЫ?
|
Геометрические конфигурации молекул
| Тип гибриди-зации
| Число гибридных орбиталей
| Число неподелен-ных электронных пар
| Геометри-ческая форма
| Угол между связями
| Примеры
| | SP
|
|
| линейная
| 1800

| СаСl2, C2H2, BeCl2, CO2, C (карбин)
| | SP2
|
|
| плоская треугольная
| 1200

| C2H4, BCl3, AlF3, C6H6, O3, C (графит)
| | SP3
|
|
| тетраэдричес-кая
| 109028΄

| CH4, CCl4, SiH4, NH4+, С (алмаз)
| |
| тригональная пирамида
| 107°3΄
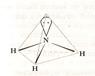
| NH3, SO32-, NF3
| |
| угловая
| 104°5΄
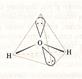
| H2O, XeO2
| | SP3d
|
|
| тригонально-бипирами-дальная
| 900,1200
| РСl5
| | SP3d2
|
|
| октаэдричес-кая
| 900
| SF6
|
Приложение 8
Некоторые частные реакции катионов первой аналитической группы по кислотно-основной классификации
| Реагент
| Катионы
| | Li+
| Na+
| K+
| NH4+
| | NaOH, KOH
|
|
|
| Выделяется NH3 (лучше при нагревании)
| | Na2CO3, K2CO3
| Li2CO3 ↓ - белый
|
|
| Выделяется NH3 при кипячении
| | Na2НРO4
| Li3РO4 - белый
|
|
| Выделяется NH3 при кипячении
| | K[Sb(OH)6]
| Li[Sb(OH)6] ↓ - белый (из конц. растворов)
| Na[Sb(OH)6]↓ - белый
|
| H[Sb(OH)6] - белый аморфный осадок
| | H2[PtCl6], Na2[PtCl6]
|
|
| К2[PtCl6]↓ - желтый
| (NH4)2[PtCl6]↓ - желтый
| | Na3[Co(NO2)6]
| Li3[Co(NO2)6]↓ - желтый
|
| NaK2[Co(NO2)6]↓ - желтый
| Na(NH4)2[Co(NO2)6]↓ - желтый
| | Na2Pb[Cu(NO2)6]
|
|
| K2Pb[Cu(NO2)6]↓ - черный
| Черный осадок
| | Zn(UO2)Ac8*
| LiZn(UO2)3Ac9 ↓ - желто-зеленый
| NaZn(UO2)3Ac9·9H2O↓ - желтый или зеленовато-желтый
|
|
| | NH4F, NaF
| LiF ↓ - белый аморфный осадок
|
|
|
| | K2[HgI4]+KOH (Ре-актив Несслера)
|
|
|
| [OHg2NH2]I↓ - красно-бурый
| | Цвет пламени горелки
| Карминово-красный
| Желтый
| Фиолетовый
|
| *Ас – ацетат-ион СН3СОО-.
Приложение 9 Некоторые частные реакции катионов второй аналитической группы по кислотно-основной классификации
| Реагент
| Катионы
| | Ag+
| Pb2+
| Нg22+
| | HCl, хлориды
| AgCl↓ - белый, растворимый в NH4ОH
| PbC12↓- белый, растворимый в горячей воде
| Hg2C12↓ - белый, чернеющий в NH4ОH
| | KOH, NaOH
| Аg2O↓ - бурый, растворимый в NH4ОH
| Pb(OH)2↓- белый, растворимый в кислотах и избытке щелочей.
| Hg2О↓- черный
| | NH40H (избыток)
| [Аg(NН3)2]+ раствор
|
| Рb(ОН)2↓-белый
| (NН2Нg)Сl↓ + ↓Hg - черный
| | K2Cr04
| Аg2СrО4↓ кирпично- красный
| PbCr04↓ - желтый
| Hg2CrО4↓ - красный
| | H2S04, сульфаты
| Ag2SO4↓ - белый (из конц. растворов)
| PbS04↓ - белый
| Нg2SO4 - белый (из конц. растворов)
| | Na2HP04
| Аg3РО4↓ - желтый, растворимый в растворе аммиака
| Pb3(PO4)2 ↓- белый, растворимый в HNO3, в растворах щелочей
| Hg2HPO4↓ - белый, растворимый в HNO3
| | НI, (KI)
| AgI↓- желтый
| РbI2↓- золотисто-желтый, растворимый в горячей воде, NaOH, избытке КI
| Hg2I2↓- грязно-зеленый, растворимый в избытке КI
| | Сильные восстановители
| Ag↓ - черный
| Pb↓ - черный
| Hg↓ - черный
| | | | | | |
Приложение 10 Некоторые частные реакции катионов третьей аналитической группы по кислотно-основной классификации
| Реагент
| Катионы
| | Са2+
| Ba2+
| Sr2+
| | (NH4)2СО3, Nа2СО3, К2СО3
| СаСО3↓ - белый
| ВаСО3↓ - белый
| SrСО3↓ -белый
| | Осадки растворяются в минеральных кислотах и уксусной кислоте
| | Na2HP04
| СаНРО4↓ белый
| ВаНРО4↓ белый
| SrHP04↓ белый
| | Осадки растворяются в минеральных кислотах и уксусной кислоте
| | (NH4)2C204
| СаС2О4↓ - белый, нерастворимый в уксусной кислоте
| ВаС2О4↓ - белый, растворимый в уксусной при нагревании
| SrC204↓ - белый, частично растворимый в уксусной кислоте
| | Осадки растворяются в минеральных кислотах
| | H2S04 и растворимые сульфаты
| CaS04↓ - белый, нерастворимый в разб. кислотах, заметно растворяется в растворе (NH4)2SO4
| BaS04↓ - белый, нерастворимый в разб. кислотах, заметно растворяется в конц. Н2SO4
| SrS04↓ - белый, нерастворимый в разб. кислотах, заметно растворяется в конц. Н2SO4
| | К4[Fe(CN)6]
| К2Ca [Fe(CN)6] ↓ - белый, растворимый в минеральных кислотах
| K2Ba[Fe(CN)6]↓ - белый (из конц. растворов), растворимый в минеральных кислотах
|
| | CaS04·2Н2О (гипсовая вода)
|
| BaS04↓ - белый
| SrS04↓ - белый
| | К2Сr04
|
| ВаСrО4↓ - желтый (из конц. растворов), растворимый в минеральных кислотах, не растворимый в уксусной кислоте.
| SrCrO4↓ - желтый (из конц. растворов), растворимый в минеральных кислотах и уксусной кислоте.
| | Цвет пламени горелки
| Кирпично - красный
| Желто-зеленый
| Карминово-красный
|
Приложение 11 Некоторые частные реакции катионов четвертой аналитической группы по кислотно-основной классификации
| Реагент
| Катионы
| | A13+
| Cr3+
| Sn2+
| As (III)
| As (V)
| Zn2+
| | (NH4)2S
| Аl(ОН)3↓ - белый
| Сr(ОН)3↓-серо-зеленый
| SnS↓ - буро-черный
| As2S3 – желтый
| As2S5 – желтый
| ZnS↓ - белый
| | NaOH, КОН
| Аl(ОН)3↓ - белый
| Сr(ОН)3↓-серо-зеленый
| Sn(OH)2 - белый
| AsO33- в растворе
| AsO43- в растворе
| Zn(ОН)2↓ - белый
| | Растворяются в избытке растворов щелочей
| | NaOH + Н2О2
| [Al(OH)4]-2- в растворе
| Желтый раствор Cr042-
| [Sn(OH)6]2- в растворе
| AsO33- в растворе
| AsO43- в растворе
| [Zn(OH)4]2- в растворе
| | Na2HP04
| AlP04↓ - белый, растворимый в щелочах, нерастворимый в уксусной кислоте
| CrPО4↓ - зеленый, растворимый в щелочах, нерастворимый в уксусной кислоте
| SnHPO4↓, Sn3(PO4)2↓ - белый | AsO33- в растворе
| AsO43- в растворе
| Zn3(РО4)↓ - белый, растворимый в щелочах, аммиаке, в уксусной кисолоте
| | Раствор NH3
| Аl(ОН)3↓ - белый
| Сr(ОН)3↓-серо-зеленый
| Sn(OH)2 - белый
| AsO33- в растворе
| AsO43- в растворе
| Zn(ОН)2↓ - белый
| | Цвет пламени горелки
| Не окрашивает
| Не окрашивает
| Синий
| Бледно-голубой
| Бледно-голубой
| Не окрашивает
|
Приложение 12 Некоторые частные реакции катионов пятой аналитической группы по кислотно-основной классификации
| Реагент
| Катионы
| | Mg2+
| Sb (III)
| Sb (V)
| Bi (III)
| Mn2+
| Fe2+
| Fe3+
| | NaOH, КОН, NН4ОH
| Mg(OH)2↓ - белый
| Sb(ОН)3↓- белый
| SbO(OH)3↓- белый
| Bi(ОН)3 - белый
| Мn(OН)2↓-белый
| Fe(OH)2↓ - белый
| Fe(OH)3 ↓ - красно-бурый
| | NaOH (избыток) + Н2О2
| Mg(OH)2↓ - белый
| [Sb(OH)4]- в растворе
| [Sb(OH)6]- в растворе
| Bi(ОН)3↓ - белый
| МnО(ОН)2↓ - темно-коричневый
| Fе(ОН)3↓ - красно-бурый
| Fе(ОН)3↓ - красно-бурый
| | Na2CO3
| (MgOH)2CO3↓ - белый
| Sb(ОН)3↓- белый
| SbO(ОН)3↓- белый
| BiOHCO3↓ - белый
| (MnOH)2CO3↓ - белый
| FeCO3↓ - белый
| FeOHCO3↓ - красно-бурый
| | Na2HP04
| MgHPO4, Mg3(PO4)2↓ - белый, в присутствии NH3 – белый осадок NH4MgPO4
| (SbO)3PО4↓- белый
| SbO(OH)3↓ - белый
| BiРО4↓ - белый
| МnHРО4↓, Мn3(РО4)2↓ - белый
| FeHPO4↓, Fe3(PO4)2↓ - зеленый
| FeРO4↓ - желтый
| | K4[Fe(CN)6]
|
|
|
|
|
|
| Fe4[Fe(CN)6]3↓ - cиний
| | К3[Fе(СN)6]
|
|
|
|
|
| Fe3[Fe(CN)6]2↓ - cиний
|
| | KCNS
|
|
|
|
|
|
| Fе(СNS)3 – красный раствор
| | (NH4)2S
| Мп(ОН)2↓ - белый (из конц. растворов)
| Sb2S3↓ - оранжевый
| Sb2S5↓ - оранжевый
| Bi2S3↓ - черно-коричневый
| MnS↓ - розово-телесный
| FeS↓ - черный
| Fe2S3↓ - черный
| | Цвет пламени
| Не окрашивает
| Голубой
| Голубой
| Зеленый
| Не окрашивает
| Не окрашивает
| Не окрашивает
|
Приложение 13 Некоторые частные реакции катионов шестой аналитической группы по кислотно-основной классификации
| Реагент
| Катионы
| | Сu2+
| Cd2+
| Hg2+
| Co2+
| Ni2+
| | NaOH, КОН
| CuOHCl↓ - голубовато-зеленый (из растворов хлоридов)
| Cd(OH)2↓ - белый
| HgO↓ - желтый
| Co(OH)Cl↓- голубой (из растворов хлоридов)
| Ni(OH)Cl↓- зеленый (из растворов хлоридов)
| | Раствор NH3 в избытке
| [Cu(NH3)4]2+ синий раствор
| [Cd(NH3)4]2+ бесцветный раствор
| [Hg(NH3)4]2+ бесцветный раствор
| [Co(NH3)6]2+ желтый раствор
| [Ni(NH3)6]2+ сине-фиолетовый раствор
| | Na2CO3
| (CuOH)2CO3↓ - голубой
| (CdOH)2CO3↓ - белый
| HgCO3↓ (HgOH)2CO3↓ -красно-бурый
| (CоOH)2CO3↓ - розово-фиолетовый
| (NiOH)2CO3↓ - зеленый
| | Na2HPO4
| CuHPO4↓, Cu3(PO4)2↓ - голубой
| CdHPO4↓, Cd3(PO4)2↓ - белый
| HgHPO4↓, Hg3(PO4)2↓ - белый
| CoHPO4↓, Co3(PO4)2↓ -фиолетовый
| NiHPO4↓, Ni3(PO4)2↓ -зеленый
| | (NH4)2S, H2S
| CuS↓- черный
| CdS↓- желтый
| HgS↓- черный
| CoS↓ - черный
| NiS↓ - черный
|
Приложение 14
|











