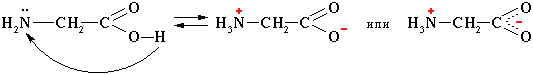Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Углеводы. Классификация. ФункцииСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Углеводы. Классификация. Функции Углеводами - называют органические соединения, состоящие из углерода (C), водорода (H) и кислорода(O2). Общая формула таких углеводов Cn(H2O)m. Примером может служить глюкоза (С6Н12О6)
С точки зрения химии углеводы являются органическими веществами, содержащими неразветвленную цепь из нескольких атомов углерода, карбонильную группу (C=O), а также несколько гидроксильных групп(OH).
В организме человека углеводы производятся в незначительном количестве, поэтому основное их количество поступает в организм с продуктами питания.
Виды углеводов. Углеводы бывают: 1) Моносахариды (самые простые формы углеводов) - глюкоза С6Н12О6 (основное топливо в нашем организме) - фруктоза С6Н12О6 (самый сладкий углевод) - рибоза С5Н10О5 (входит в состав нуклеиновых кислот) - эритроза С4H8O4 (промежуточная форма при расщеплении углеводов)
2) Олигосахариды (содержат от 2 до 10 остатков моносахаридов) - сахароза С12Н22О11 (глюкоза + фруктоза, или в просто – тростниковый сахар) - лактоза C12H22O11 (молочный сахар) - мальтоза C12H24O12 (солодовый сахар, состоит из двух связанных остатков глюкозы) 110516_1305537009_Sugar-Cubes.jpg
3) Сложные углеводы (состоящие из множества остатков глюкозы) - крахмал (С6H10O5)n (наиболее важный углеводный компонент пищевого рациона, человек потребляет из углеводов около 80% крахмала.) - гликоген (энергетические резервы организма, излишки глюкозы, при поступлении в кровь, откладываются про запас организмом в виде гликогена) крахмал12.jpg 4 ) Волокнистые, или неусваеваемые, углеводы, определяющиеся как пищевая клетчатка. - Целлюлоза (самое распостраненное органическое вещество на земле и вид клетчатки)
По простой классификации углеводы можно разделить на простые и сложные. В простые входят моносахариды и олигосахариды, в сложные полисахариды и клетчатка.
Основные функции. Энергетическая. Углеводы являются основным энергетическим материалом. При распаде углеводов высвобождаемая энергия рассеивается в виде тепла или накапливается в молекулах АТФ. Углеводы обеспечивают около 50 – 60 % суточного энергопотребления организма, а при мышечной деятельности на выносливость — до 70 %. При окислении 1 г углеводов выделяется 17 кДж энергии (4,1 ккал). В качестве основного энергетического источника в организме используется свободная глюкоза или запасенные углеводы в виде гликогена. Является основным энергетическим субстратом мозга.
Пластическая. Углеводы (рибоза, дезоксирибоза) используются для построения АТФ, АДФ и других нуклеотидов, а также нуклеиновых кислот. Они входят в состав некоторых ферментов. Отдельные углеводы являются структурными компонентами клеточных мембран. Продукты превращения глюкозы (глюкуроновая кислота, глюкозамин и др.) входят в состав полисахаридов и сложных белков хрящевой и других тканей. Запас питательных веществ. Углеводы накапливаются (запасаются) в скелетных мышцах, печени и других тканях в виде гликогена. Систематическая мышечная деятельность приводит к увеличению запасов гликогена, что повышает энергетические возможности организма. Специфическая. Отдельные углеводы участвуют в обеспечении специфичности групп крови, исполняют роль антикоагулянтов (вызывающие свертывание), являясь рецепторами цепочки гормонов или фармакологических веществ, оказывая противоопухолевое действие. Защитная. Сложные углеводы входят в состав компонентов иммунной системы; мукополисахариды находятся в слизистых веществах, которые покрывают поверхность сосудов носа, бронхов, пищеварительного тракта, мочеполовых путей и защищают от проникновения бактерий и вирусов, а также от механических повреждений. Регуляторная. Клетчатка пищи не поддается процессу расщепления в кишечнике, однако активирует перистальтику кишечного тракта, ферменты, использующиеся в пищеварительном тракте, улучшая пищеварение и усвоение питательных веществ.
Химические свойства Моносахариды проявляют свойства спиртов и карбонильных соединений. Окисление. a) Как и у всех альдегидов, окисление моносахаридов приводит к соответствующим кислотам. Так, при окислении глюкозы аммиачным раствором гидрата окиси серебра образуется глюконовая кислота (реакция "серебряного зеркала"). b) Реакция моносахаридов с гидроксидом меди при нагревании так же приводит к альдоновым кислотам. c) Более сильные окислительные средства окисляют в карбоксильную группу не только альдегидную, но и первичную спиртовую группы, приводя к двухосновным сахарным (альдаровым) кислотам. Обычно для такого окисления используют концентрированную азотную кислоту.
Восстановление. Восстановление сахаров приводит к многоатомным спиртам. В качестве восстановителя используют водород в присутствии никеля, алюмогидрид лития и др.
III. Специфические реакции Кроме приведенных выше, глюкоза характеризуется и некоторыми специфическими свойствами - процессами брожения. Брожением называется расщепление молекул сахаров под воздействием ферментов (энзимов). Брожению подвергаются сахара с числом углеродных атомов, кратным трем. Существует много видов брожения, среди которых наиболее известны следующие: a) спиртовое брожение b) молочнокислое брожение c) маслянокислое брожение
Упомянутые виды брожения, вызываемые микроорганизмами, имеют широкое практическое значение. Например, спиртовое – для получения этилового спирта, в виноделии, пивоварении и т.д., а молочнокислое – для получения молочной кислоты и кисломолочных продуктов.
3. Стереоизомерия моносахаридов D- и L-ряды. Открытые и циклические формулы. Пиранозы и фуранозы. α- и β-аномеры. Циклоцепная таутомерия. Явление муторотации.
Способность ряда органических соединений вращать плоскость поляризации поляризованного света вправо или влево называют оптической активностью. Исходя из сказанного выше, следует, что органические вещества могут существовать в виде правовращающих и левовращающих изомеров. Такие изомеры получили название стереоизомеров, а само явление стереоизомерии. В основе более строгой системы классификации и обозначения стереоизомеров лежит не вращение плоскости поляризации света, а абсолютная конфигурация молекулы стереоизомера, т.е. взаимное расположение четырех обязательно разных замещающих групп, находящихся в вершинах тетраэдра, вокруг локализованного в центре атома углерода, который получил название асимметрического атома углерода или хирального центра. Хиральные или, как их еще называют, оптически активные атомы углерода обозначают в структурных формулах звездочками
Таким образом, под термином стереоизомерия следует понимать различную пространственную конфигурацию заместителей у соединений, имеющих одну и ту же структурную формулу и обладающих одинаковыми химическими свойствами. Такой вид изомерии называют также зеркальной изомерией. Наглядным примером зеркальной изомерии могут служить правая и левая ладони руки. Ниже приведены структурные формулы стереоизомеров глицеринового альдегида и глюкозы.
Если у асимметрического атома углерода в проекционной формуле глицеринового альдегида ОН-группа располагается справа, такой изомер называют D-стереоизомером, а если ОН-группа расположена слева –L-стереоизомером. В случае тетроз, пентоз, гексоз и других моноз, которые обладают двумя и более асимметрическими атомами углерода, принадлежность стереоизомера к D- или L-ряду определяют по расположению ОН-группы у предпоследнего атома углерода в цепи – он же является последним асимметрическим атомом. Например, для глюкозы оценивают ориентацию ОН-группы у 5-ого атома углерода. Абсолютно зеркальные стереоизомеры называют энантиомерами или антиподами.
Стереоизомеры не отличаются по своим химическим свойствам, но отличаются по биологическому действию (биологической активности). Большая часть моносахаридов в организме млекопитающих относится к D-ряду – именно к этой конфигурации специфичны ферменты, ответственные за их метаболизм. В частности D-глюкоза воспринимается как сладкое вещество, благодаря способности взаимодействовать с вкусовыми рецепторами языка, в то время как L-глюкоза безвкусна, поскольку ее конфигурация не воспринимается вкусовыми рецепторами. В общем виде строение альдоз и кетоз можно представить следующим образом.
Стереоизомерия. Молекулы моносахаридов содержат несколько центров хиральности, что служит причиной существования многих стереоизомеров, отвечающих одной и той же структурной формуле. Например, в альдогексозе имеются четыре асимметрических атома углерода и ей соответствуют 16 стереоизомеров (24), т. е. 8 пар энантиомеров. По сравнению с соответствующими альдозами кетогексозы содержат на один хиральный атом углерода меньше, поэтому число стереоизомеров (23) уменьшается до 8 (4 пары энантиомеров).
Открытые (нециклические) формы моносахаридов изображают в виде проекционных формул Фишера. Углеродную цепь в них записывают вертикально. У альдоз наверху помещают альдегидную группу, у кетоз - соседнюю с карбонильной первичную спиртовую группу. С этих групп начинают нумерацию цепи.
Для обозначения стереохимии используется D,L-система. Отнесение моносахарида к D- или L-ряду проводят по конфигурации хирального центра, наиболее удаленного от оксогруппы, независимо от конфигурации остальных центров! Для пентоз таким «определяющим» центром является атом С-4, а для гексоз - С-5. Положение группы ОН у последнего центра хиральности справа свидетельствует о принадлежности моносахарида к D-ряду, слева - к L-ряду, т. е. по аналогии со стереохимическим стандартом - глицериновым альдегидом
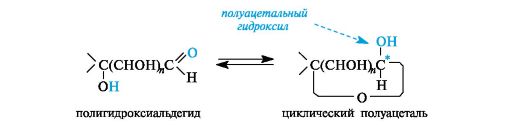
Циклические формы. Открытые формы моносахаридов удобны для рассмотрения пространственных отношений между стереоизомерными моносахаридами. В действительности моносахариды по строению являются циклическими полуацеталями. Образование циклических форм моносахаридов можно представить как результат внутримолекулярного взаимодействия карбонильной и гидроксильной групп, содержащихся в молекуле моносахарида.
Впервые циклическую полуацетальную формулу глюкозы предложил А. А. Колли (1870). Он объяснил отсутствие некоторых альдегидных реакций у глюкозы наличием трехчленного этиленоксидного (α-окисного) цикла:
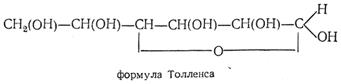
Позже Толленс (1883) предложил аналогичную полуацетальную формулу глюкозы, но с пятичленным (γ-окисным) бутиленоксидным кольцом:
Формулы Колли — Толленса громоздки и неудобны, не отражают строения циклической глюкозы, поэтому были предложены формулы Хеуорса.
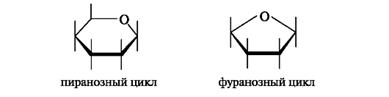
В результате циклизации образуются термодинамически более устойчивые фуранозные (пятичленные) и пиранозные (шестичленные) циклы. Названия циклов происходят от названий родственных гетероциклических соединений - фурана и пирана.
Образование этих циклов связано со способностью углеродных цепей моносахаридов принимать достаточно выгодную клешневидную конформацию. Вследствие этого в пространстве оказываются сближенными альдегидная (или кетонная) и гидроксильная при С-4 (или при С-5) группы, т. е. те функциональные группы, в результате взаимодействия которых осуществляется внутримолекулярная циклизация.
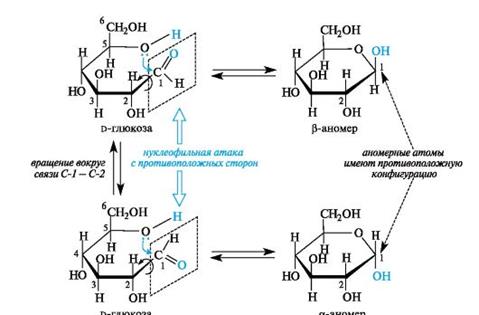
В циклической форме создается дополнительный центр хиральности - атом углерода, ранее входивший в состав карбонильной группы (у альдоз это С-1). Этот атом называют аномерным, а два соответствующих стереоизомера - α- и β-аномерами (рис. 11.1). Аномеры представляют собой частный случай эпимеров.
У α-аномера конфигурация аномерного центра одинакова с конфигурацией «концевого» хирального центра, определяющего принадлежность к d- или l-ряду, а у β-аномера - противоположна. В проекционных формулах Фишера у моносахаридов d-ряда в α-аномере гликозидная группа ОН находится справа, а в β-аномере - слева от углеродной цепи.
Рис. 11.1. Образование α- и β-аномеров на примере d-глюкозы
Формулы Хеуорса. Циклические формы моносахаридов изображают в виде перспективных формул Хеуорса, в которых циклы показывают в виде плоских многоугольников, лежащих перпендикулярно плоскости рисунка. Атом кислорода располагают в пиранозном цикле в дальнем правом углу, в фуранозном - за плоскостью цикла. Символы атомов углерода в циклах не указывают.
Для перехода к формулам Хеуорса циклическую формулу Фишера преобразуют так, чтобы атом кислорода цикла располагался на одной прямой с атомами углерода, входящими в цикл. Это показано ниже на примере a-d-глюкопиранозы путем двух перестановок у атома С-5, что не изменяет конфигурацию этого асимметрического центра (см. 7.1.2). Если преобразованную формулу Фишера расположить горизонтально, как требуют правила написания формул Хеуорса, то заместители, находившиеся справа от вертикальной линии углеродной цепи, окажутся под плоскостью цикла, а те, что были слева, - над этой плоскостью.
У d-альдогексоз в пиранозной форме (и у d-альдопентоз в фуранозной форме) группа СН2ОН всегда располагается над плоскостью цикла, что служит формальным признаком d-ряда. Гликозидная гидроксильная группа у a-аномеров d-альдоз оказывается под плоскостью цикла, у β-аномеров - над плоскостью.
D-ГЛЮКОПИРАНОЗА По аналогичным правилам осуществляется переход и у кетоз, что показано ниже на примере одного из аномеров фуранозной формы d-фруктозы.
Циклоцепная таутомерия обусловлена переходом открытых форм моносахаридов в циклические и наоборот. Изменение во времени угла вращения плоскости поляризации света растворами углеводов называют мутаротацией. Химическая сущность мутаротации состоит в способности моносахаридов к существованию в виде равновесной смеси таутомеров - открытой и циклических форм. Такой вид таутомерии называется цикло-оксо-таутомерией. В растворах равновесие между четырьмя циклическими таутомерами моносахаридов устанавливается через открытую форму - оксоформу. Взаимопревращение a- и β-аномеров друг в друга через про- межуточную оксоформу называется аномеризацией. Таким образом, в растворе d-глюкоза существует в виде таутомеров: оксоформы и a- и β-аномеров пиранозных и фуранозных циклических форм.
ЛАКТИМ-ЛАКТАМНАЯ ТАУТОМЕРИЯ Этот вид таутомерии характерен для азотсодержащих гетероциклов с фрагментом N=C—ОН. Взаимопревращение таутомерных форм связано с переносом протона от гидроксильной группы, напоминающей фенольную ОН-группу, к основному центру — пиридиновому атому азота и наоборот. Обычно лактамная форма в равновесии преобладает.
Моноаминомонокарбоновые. По полярности радикала: С неполярным радикалом:(Аланин,валин, лейцин, фенилаланин)Моноамино,монокарбоновые С полярным незаряженным радикалом(Глицин, серин, аспарагин, глутамин) С отрицательно заряженным радикалом(Аспарагиновая,глутаминовая кислота)моноамино,дикарбоновые С положительно заряженным радикалом(лизин,гистидин) диамино,монокарбоновые
Стереоизомерия
Все природные α-аминокислоты, кроме глицина (NH2 -CH2 - COOH), имеют асимметрический атом углерода (α-углеродный атом), а некоторые из них даже два хиральных центра, например, треонин. Таким образом, все аминокислоты могут существовать в виде пары несовместимых зеркальных антиподов (энантиомеров). За исходное соединение, с которым принято сравнивать строение α-аминокислот, условно принимают D- и L-молочные кислоты, конфигурации которых, в свою очередь, установлены по D- и L-глицериновым альдегидам. Все превращения, которые осуществляются в этих рядах при переходе от глицеринового альдегида к α-аминокислоте, выполняются в соответствии с главным требованием − они не создают новых и не разрывают старых связей у асимметрического центра. Для определения конфигурации α-аминокислоты в качестве эталона часто используют серин (иногда аланин). Природные аминокислоты, входящие в состав белков, относятся к L-ряду. D-формы аминокислот встречаются сравнительно редко, они синтезируются только микроорганизмами и называются «неприродными» аминокислотами. Животными организмами D-аминокислоты не усваиваются. Интересно отметить действие D- и L-аминокислот на вкусовые рецепторы: большинство аминокислот L-ряда имеют сладкий вкус, а аминокислоты D-ряда − горькие или безвкусные. Без участия ферментов самопроизвольный переход L-изомеров в D-изомеры с образованием эквимолярной смеси (рацемическая смесь) осуществляется в течение достаточно длительного промежутка времени. Рацемизация каждой L-кислоты при данной температуре идет с определенной скоростью. Это обстоятельство можно использовать для установления возраста людей и животных. Так, например, в твердой эмали зубов имеется белок дентин, в котором L-аспартат переходит в D-изомер при температуре тела человека со скоростью 0,01% в год. В период формирования зубов в дентине содержится только L-изомер, поэтому по содержанию D-аспартата можно рассчитать возраст человека или животного.
I. Общие свойства 1. Внутримолекулярная нейтрализация → образуется биполярный цвиттер-ион: Водные растворы электропроводны. Эти свойства объясняются тем, что молекулы аминокислот существуют в виде внутренних солей, которые образуются за счет переноса протона от карбоксила к аминогруппе:
цвиттер-ион Водные растворы аминокислот имеют нейтральную, кислую или щелочную среду в зависимости от количества функциональных групп. 2. Поликонденсация → образуются полипептиды (белки):
При взаимодействии двух α-аминокислот образуется дипептид. 3. Разложение → Амин + Углекислый газ: NH2-CH2-COOH → NH2-CH3 + CO2↑ IV. Качественная реакция 1. Все аминокислоты окисляются нингидрином с образованием продуктов сине-фиолетового цвета! 2. С ионами тяжелых металлов α-аминокислоты образуют внутрикомплексные соли. Комплексы меди (II), имеющие глубокую синюю окраску, используются для обнаружения α-аминокислот.
Физиологические активные пептиды. Примеры. Пептиды, обладая высокой физиологической активностью, регулируют различные биологические процессы. По биорегуляторному действию пептиды принято делить на несколько групп: · соединения, обладающие гормональной активностью (глюкагон, окситоцин, вазопрессин и др.); · вещества, регулирующие пищеварительные процессы (гастрин, желудочный ингибирующий пептид и др.); · пептиды, регулирующие аппетит (эндорфины, нейропептид-Y, лептин и др.); · соединения, обладающие обезболивающим эффектом (опиоидные пептиды); · органические вещества, регулирующие высшую нервную деятельность, биохимические процессы, связанные с механизмами памяти, обучения, возникновением чувства страха, ярости и др.; · пептиды, которые регулируют артериальное давление и тонус сосудов (ангиотензин II, брадикинин и др.). · пептиды, которые обладают противоопухолевым и противовоспалительным свойствами (Луназин) · Нейропептиды — соединения, синтезируемые в нейронах, обладающие сигнальными свойствами
Классификация белков - по форме молекул (глобулярные или фибриллярные); - по молекулярной массе (низкомолекулярные, высокомолекулярные и др.); - по химическому строению ( наличие или отсутствие небелковой части); - по локализации в клетке (ядерные, цито-плазматические, лизосомальные и др.); - по локализации в организме (белки крови, печени, сердца и др.); - по возможности адаптивно регулировать количество данных белков: белки, синтезирующиеся с постоянной скоростью (конститутивные), и белки, синтез которых может усиливаться при воздействии факторов среды (индуцибельные); - по продолжительности жизни в клетке (от очень быстро обновляющихся белков, с Т1/2 менее 1 ч, до очень медленно обновляющихся белков, Т1/2 которых исчисляют неделями и месяцами); - по схожим участкам первичной структуры и родственным функциям (семейства белков). Классификация белков по химическому строению Простые белки. Некоторые белки содержат в своём составе только полипептидные цепи, состоящие из аминокислотных остатков. Их называют "простые белки". Примером простых белков - гистоны; в их составе содержится много аминокислотных остатков лизина и аргинина, радикалы которых имеют положительный заряд. 2. Сложные белки. Очень многие белки, кроме полипептидных цепей, содержат в своём составе небелковую часть, присоединённую к белку слабыми или ковалентными связями. Небелковая часть может быть представлена ионами металлов, какими-либо органическими молекулами с низкой или высокой молекулярной массой. Такие белки называют "сложные белки". Прочно связанная с белком небелковая часть носит название простетической группы. У биополимеров, макромолекулы которых состоят из полярных и неполярных групп, сольватируются полярные группы, если растворитель полярен. В неполярном растворителе, соответственно, сольватируются неполярные участки макромолекул. Обычно он хорошо набухает в жидкости, близкой к нему по химическому строению. Так, углеводородные полимеры типа каучуков набухают в неполярных жидкостях: гексане, бензоле. Биополимеры, в состав молекул которых входит большое количество полярных функциональных групп, например, белки, полисахариды, лучше набухают в полярных растворителях: воде, спиртах и т.д. Образование сольватной оболочки молекулы полимера сопровождается выделением энергии, которая называется теплотой набухания. Теплота набухания зависит от природы веществ. Она максимальна при набухании в полярном растворителе ВМС, содержащего большое количество полярных групп и минимальна при набухании в неполярном растворителе углеводородного полимера. Кислотность среды, при которой устанавливается равенство положительных и отрицательных зарядов и белок становится электронейтральным, называется изоэлектрической точкой (ИЭТ). Белки, у которых ИЭТ находится в кислой среде, называются кислыми. Белки, у которых значение ИЭТ находится в щелочной среде, называются основными. У большинства растительных белков ИЭТ находится в слабокислой среде . Набухание и растворение ВМС зависят от: Роль 2,3-дифосфоглицерата 2,3-Дифосфоглицерат образуется в эритроцитах из 1,3-дифосфоглицерата, промежуточного метаболита гликолиза, в реакциях, получивших название шунт Раппопорта.
Реакции шунта Раппопорта
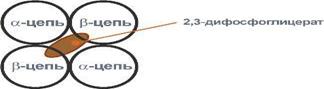
2,3-Дифосфоглицерат располагается в центральной полости тетрамера дезоксигемоглобина и связывается с β-цепями, образуя поперечный солевой мостик между атомами кислорода 2,3-дифосфоглицерата и аминогруппами концевого валина обеих β-цепей, также аминогруппами радикалов лизина и гистидина.
Расположение 2,3-дифосфоглицерата в гемоглобине Функция 2,3-дифосфоглицерата заключается в снижении сродства гемоглобина к кислороду. Это имеет особенное значение при подъеме на высоту, при нехватке кислорода во вдыхаемом воздухе. В этих условиях связывание кислорода с гемоглобином в легких не нарушается, так как концентрация его относительно высока. Однако в тканях за счет 2,3-дифосфоглицерата отдача кислорода возрастает в 2 раза.
Углеводы. Классификация. Функции Углеводами - называют органические соединения, состоящие из углерода (C), водорода (H) и кислорода(O2). Общая формула таких углеводов Cn(H2O)m. Примером может служить глюкоза (С6Н12О6)
С точки зрения химии углеводы являются органическими веществами, содержащими неразветвленную цепь из нескольких атомов углерода, карбонильную группу (C=O), а также несколько гидроксильных групп(OH).
В организме человека углеводы производятся в незначительном количестве, поэтому основное их количество поступает в организм с продуктами питания.
Виды углеводов. Углеводы бывают: 1) Моносахариды (самые простые формы углеводов) - глюкоза С6Н12О6 (основное топливо в нашем организме) - фруктоза С6Н12О6 (самый сладкий углевод) - рибоза С5Н10О5 (входит в состав нуклеиновых кислот) - эритроза С4H8O4 (промежуточная форма при расщеплении углеводов)
2) Олигосахариды (содержат от 2 до 10 остатков моносахаридов) - сахароза С12Н22О11 (глюкоза + фруктоза, или в просто – тростниковый сахар) - лактоза C12H22O11 (молочный сахар) - мальтоза C12H24O12 (солодовый сахар, состоит из двух связанных остатков глюкозы) 110516_1305537009_Sugar-Cubes.jpg
3) Сложные углеводы (состоящие из множества остатков глюкозы) - крахмал (С6H10O5)n (наиболее важный углеводный компонент пищевого рациона, человек потребляет из углеводов около 80% крахмала.) - гликоген (энергетические резервы организма, излишки глюкозы, при поступлении в кровь, откладываются про запас организмом в виде гликогена) крахмал12.jpg 4 ) Волокнистые, или неусваеваемые, углеводы, определяющиеся как пищевая клетчатка. - Целлюлоза (самое распостраненное органическое вещество на земле и вид клетчатки)
По простой классификации углеводы можно разделить на простые и сложные. В простые входят моносахариды и олигосахариды, в сложные полисахариды и клетчатка.
Основные функции. Энергетическая. Углеводы являются основным энергетическим материалом. При распаде углеводов высвобождаемая энергия рассеивается в виде тепла или накапливается в молекулах АТФ. Углеводы обеспечивают около 50 – 60 % суточного энергопотребления организма, а при мышечной деятельности на выносливость — до 70 %. При окислении 1 г углеводов выделяется 17 кДж энергии (4,1 ккал). В качестве основного энергетического источника в организме используется свободная глюкоза или запасенные углеводы в виде гликогена. Является основным энергетическим субстратом мозга. Пластическая. Углеводы (рибоза, дезоксирибоза) используются для построения АТФ, АДФ и других нуклеотидов, а также нуклеиновых кислот. Они входят в состав некоторых ферментов. Отдельные углеводы являются структурными компонентами клеточных мембран. Продукты превращения глюкозы (глюкуроновая кислота, глюкозамин и др.) входят в состав полисахаридов и сложных белков хрящевой и других тканей. Запас питательных веществ. Углеводы накапливаются (запасаются) в скелетных мышцах, печени и других тканях в виде гликогена. Систематическая мышечная деятельность приводит к увеличению запасов гликогена, что повышает энергетические возможности организма. Специфическая. Отдельные углеводы участвуют в обеспечении специфичности групп крови, исполняют роль антикоагулянтов (вызывающие свертывание), являясь рецепторами цепочки гормонов или фармакологических веществ, оказывая противоопухолевое действие. Защитная. Сложные углеводы входят в состав компонентов иммунной системы; мукополисахариды находятся в слизистых веществах, которые покрывают поверхность сосудов носа, бронхов, пищеварительного тракта, мочеполовых путей и защищают от проникновения бактерий и вирусов, а также от механических повреждений. Регуляторная. Клетчатка пищи не поддается процессу расщепления в кишечнике, однако активирует перистальтику кишечного тракта, ферменты, использующиеся в пищеварительном тракте, улучшая пищеварение и усвоение питательных веществ.
|
|||||||||
|
Последнее изменение этой страницы: 2017-02-05; просмотров: 6257; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.119.112.22 (0.019 с.) |