
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Теоретический объем дымовых газовСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
При полном сгорании топлива дымовые газы, уходящие из топки, содержат: двуокись углерода СО2, пары Н2О (образующиеся при сгорании водорода топлива), сернистый ангидрид SO2, азот N2 – нейтральный газ, поступивший в топку с кислородом воздуха, азот из состава топлива, а также избыточный кислород воздуха О2. При неполном сгорании к указанным элементам добавляются еще окись углерода СО, водород Н2 и метан СН4. Для удобства подсчетов продукты сгорания разделяют на сухие газы и водяные пары. Объем сухих газов принимают за 100%. При полном сгорании топлива состав сухих продуктов сгорания (в процентах по объему) следующий:
Газообразные продукты сгорания состоят из трехатомных газов СО2, SO2, сумму которых принято обозначать символом RO2, и двухатомных газов О2 и N2. Тогда равенство будет иметь вид: При полном сгорании При неполном сгорании
Объем сухих трехатомных газов определяется по формуле
Теоретический объем азота, м3/кг, находящегося в воздухе и топливе
Теоретический объем водяных паров твердого или жидкого топлива состоит из: · Объема водяных паров, м3/кг, полученных в результате сжигания водорода и испарения влаги из топлива · Объема водяных паров, поступающих с воздухом · Объема форсуночного пара, м3/кг, при сжигании мазута и его распылении с помощью паровых форсунок
Полный теоретический объем водяных паров, м3/кг
При избытке воздуха
Тогда полный объем дымовых газов, м3/кг,
При сжигании газообразного топлива теоретический объем азота, м3/м3,
Объем сухих трехатомных газов, м3/м3
Теоретический объем водяных паров, м3/м3
Где d = 10 г/м3 – влагосодержание газообразного топлива, отнесенное к 1 м3 сухого газа.
Коэффициент избытка воздуха Действительное количество воздуха, необходимое для полного сгорания 1 кг топлива, должно быть несколько большим теоретического, так как при практическом сжигании топлива не все количество теоретически необходимого воздуха используется для горения топлива; часть его не участвует в реакции горения в результате недостаточного для перемешивания воздуха с топливом, а также из-за того, что воздух не успевает вступить в соприкосновение с углеродом и уходит в газохды котла в свободном состоянии.
Отношение количества воздуха, действительно подаваемого в топку, к теоретически необходимому называют коэфициентом избытка воздуха
где Коэффициент избытка воздуха зависит от вида сжигаемого топлива, способа его сжигания, конструкции топки и принимается на основании опытных данных. Для газообразного топлива Для твердого топлива при факельном сжигании Для твердого топлива при слоевом сжигании Для жидкого топлива То значение Для поддержания нормального горения нужно подводить воздуха в топку столько, сколько требуется для полного сгорания топлива, что достигается постоянным контролем за составом дымовых газов. Наиболее важно определение содержания в дымовых газах СО и СО2. В случае неполного сгорания при недостатке воздуха в составе уходящих из топки газов будут углеводороды, окись углерода СО, а иногда и чистый водород Н, а при чрезмерном избытке воздуха создаются условия для удаления из топки несгоревших летучих горючих веществ и уноса частичек твердого топлива. Поэтому при эксплуатации топки следует сводить неполноту сгорания к возможному минимуму. Как правило котельный агрегат работает с незначительной химической неполнотой сгорания. При присосе холодного воздуха в газоходы котла экономичность его работы снижается, следовательно необходимо добиваться полной герметизации газоходов.
|
|||||
|
Последнее изменение этой страницы: 2017-01-19; просмотров: 458; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.144.93.10 (0.011 с.) |

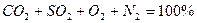 . (13)
. (13)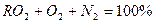 , (14)
, (14) . (15)
. (15)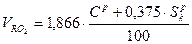 . (16)
. (16) . (17)
. (17) ;
;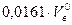 ;
;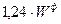 , где
, где  - расход форсуночного пара для распыливания 1 кг мазута (
- расход форсуночного пара для распыливания 1 кг мазута (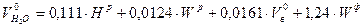 , (18)
, (18)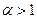 полный объем водяных паров, м3/кг, будет равен
полный объем водяных паров, м3/кг, будет равен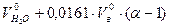 ,
, . (19)
. (19) , (20)
, (20)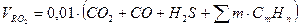 . (21)
. (21) . (22)
. (22)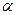
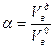 , (23)
, (23) - действительный объем воздуха, подаваемого в топку на 1 кг топлива.
- действительный объем воздуха, подаваемого в топку на 1 кг топлива.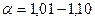 ;
;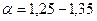 ;
;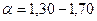 ;
;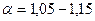 .
.


