
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Общие и специфические пути катаболизмаСодержание книги
Поиск на нашем сайте В настоящее время доказано, что огромное разнообразие пищевых продуктов и в-в, из которых эти продукты состоят, при попадании в организм, подвергаются относительно ограниченным катаболитическим превращениям Схема катаболизма Б, Л, У: Белки Углеводы Жиры $ $ ' (
$ ПВК $ Ацетил КоА $ ЦТК kСо2 i mН2о Н+gАТФ (окислительное фосфорилирование.) 1,2,3,4,5, - специфические пути катаболизма I - общий путь катаболизма.
Существует четыре этапа распада У, Ж, Б:
Образование ацетил КоА и реакции ЦТК (I и II этапы) относятся к общему пути катаболизма. Некоторы АК вступают в общий путь катаболизма на промежуточных стадиях ЦТК.
Не все мономеры сложных веществ пищи подвергаются катаболизмау. Часть мономеров используется для анаболических реакций, при этом синтезируются специфические для данной особи сложные вещества: Ж, Б, У, нуклеотиды и т.д. Этот связывающий цикл, объединяющий анаболизм и катаболизм посредством энергетических системы и общих метаболитов, называется двойственным или амфиболическим путем обмена. Окислительное декарбоксилирования ПВК и ЦТК. Большинство тканей энергию получают за счет аэробных процессов. Полное окисление ПВК происходит через общий конечный путь обмена Ж Б У, т.е. лимонно-кислый цикл Кребса (ЦТК) в аэробных условиях. В ЦТК включается не сам пируват, а продукт его окислительного декарбоксилирования – ацетилКоА. ПВК предварительно путем диффузии переносится из цитозоля в митохондрии, реакция ее превращения катализируются мультиферментным пируват-ДГ-комплексом. Общая схема реакции: ПВК+НSКоА+НАД¦ацетилКоА+СО2+НАД·Н2 Пируват ДГ комплекс – это мультифермент, состоящие из 3-х ферментов: а) пируват ДГ (Е1) б) дигидролипоилтрансацетилаза (Е2) в) дигидролипоил ДГ (Е3), в которой используют 5 коферментов: 1. тиаминпирофосфат (ТПФ), 2. амид липоевой кислоты (липоамид), 3. НSКоА, 4. ФАД, 5. НАД.
1) Реакция декарбоксилирования ПВК (ф-т Е1) СН3 СН3 | | С=О + Е1-ТПФ ¦ СН – ТПФ-Е1 + СО2 | | СООН ОН ПВК гидроксиэтилтиаминпирофосфат
2) Реакция окисления гидроксиэтиламинпирофосфата и перенос его на амид ЛК
СН – ТПФ-Е1 + S || | | окислен. форма ф-та О SН ОН ацетиллипоат
3) Перенос ацетильной гр. на КоА (Е2)
НS ацетил- КоА восст. форма ферментата
4) Окисление ЛК до ее дисульфида (Е3)
НS | ЛК Е2 + Е3ФАД·Н2
5) Регенерация окисленной Е3ФАД· Н2: Е3ФАД·Н2+НАДg Е3ФАД + НАД · Н2 Т.о., все ферменты дегидрогеназного комплекса оказываются в исходном положении, пригодном для следующего цикла. Ацетил-КоА включается в ЦТК и полностью окисляется до СО2. Когда содержание АТФ в клетке начинает превышать определенный уровень, ПДГ - комплекс, поставляющий энергетич. «топливо» для ЦТК, включается. ПВК, является исходным субстратом общего пути катаболизма. Цикл трикарбоновых кислот. -этап катаболизма У, Ж, Б в аэробных условиях. Реакции ЦТК протекают, как и образование ацетил-КоА, в митохондриях, в отличие от гликолиза, которое протекает в цитозоле. Реакции ЦТК 1). Реакция конденсации СН3Со~S-КоА + СООН СООН Ацетил-КоА | | С=О цитрат синтаза СН2 + НS· КоА | ¦ | СН2 ОН - С-СООН | | СН-СООН СН2 ЩУК(оксалоацетат) | СООН цитрат Цитратсинтаза катализирует гидролиз макроэргической связи ацетил КоА, за счет энергии гидролиза обеспечивается протекание ферментативного катализа. 2). Реакция дегидратации СООН СООН – Н2О | +Н2О | ¦ СН2 D СН2 цитрат аконитат гидратаза | - Н2О | ! С-СООН СН - СООН +Н2О || | СН СН-ОН | | СООН СООН цис-аконитат изоцитрат гидроксильная группа присоединяется к другому углеродному атому. 3).Реакция окисления и декарбоксилирования. Е- изоцитратдегидрогеназа Происходит перенос протона и двух электронов на молекулу НАД и освобождение второго протона, т.е. дегидрирование изоцитрата
Изоцитрат + НАД (НАДФ) D СООН | (СН2)2 + НАД·Н2 + СО2 | С=О | СООН a-кетоглутарат 4. Окислительное декарбоксилирование. a-кетоглутарат СООН a-кетоглутарат + НS-КоА + НАД дГ – комплекс | ¦ (СН2)2 + | О= С ~ S-КоА сукцинил КоА 5. Реакция расщепления. сукцинил КоА- СООН сукцинил КоА + ГДФ + Фн синтетаза | ¦ (СН2)2 + ГТФ + НS·КоА | СООН янтарная кислота (сукцинат) 5 а реакция субстратного фосфорилирования (Е нуклеозиддифосфаткиназа) ГТФ + АДФ D АТФ + ГТФ Происходит перенос макроэргической связи с сукцината на молекулу ГДФ с образованием ГТФ и сукцината (субстратное фосфорилирование) 6. Реакция дегидрирования сукцинат дГ СООН сукцинат + ФАД D | СН + ФАД·Н2 || СН | СООН фумаровая кислота (фумарат) после восстановления ФАД происходит пернос протонов и электронов с него в дыхательную цепь при участии коэнзима Q. При этом осуществляется регенерация простетической группы фермента.
7.Реакция гидратации. СООН фумарат гидратаза | фумарат + Н2О D НО - СН + ФАД·Н2 | СН2 | СООН Яблочная к-та (малат) Положительно заряженный атом углерода взаимодействует с -ОН группой, сначала за счет электростатических сил, а затем образуется сигма связь с атомом кислорода. 8. Реакция окисления. Фермент осуществляет перенос Н с -ОН и близлежащего углеродного атома на НАД с дальнейшим поступлением в дыхательную цепь митохондриальная СООН Малат + НАД НАД – завис. малатДГ | D С=О + НАД·Н2 | СН2 | СООН ЩУК(оксалоацетат). Т. о., за один оборот цикла происходит полное окисление одной молекулы ацетил – КоА. Суммарное уравнение превращения ацетил – КоА ферментами ЦТК: СН3СО~SКоА+2Н2О + Фн. + АДФ ¦ 2СО2 + 3НАД·Н2 + ФАД·Н2 + АТФ + КоА·SH ферменты ЦТК
Всего (включая окислительное декарбоксилирование ПВК) образуется 4 мол. НАД·Н2 и 1 мол. ФАД·Н2, которые поступают в матрикс митохондрий и дифундируют к ее внутренней мембране, окисляются соответствующей ДГ-зой. При окислении 1 мол. НАД·H2 образуется 3 мол. АТФ; 1 мол ФАД · Н2 – 1мол. АТФ; ПВК: 1 мол. НАД·H2 ¦ 3 мол АТФ ЦТК: 3 мол. НАД·H2 ¦ 9 мол АТФ 1 мол. ФАД·Н2 ¦ 2 мол. АТФ Субстратное фосфорилирование ¦ 1 мол. АТФ Всего образуется 15 мол. АТФ.
ЛЕКЦИЯ 11 ОБМЕН УГЛЕВОДОВ Углеводы, их классификация. Углеводы – это органические соединения, содержащие альдегидную или кето- группы, и являющиеся производными многоатомных спиртов. Термин «углеводы» предложен в 1844г. К. Шмидтом, т.к. в то время полагали, что их общая формула представляет собой: Сх(Н2О) n – т.е. углерод + вода. Дальнейшие исследования показали, что это не так. Например: формула дезоксирибозы С5Н1oО4. Поэтому позднее было предложено этот класс веществ называть глицидами. Углеводы широко распространены в природе. В растениях их соединения ~ 80%, в тканях животных всего ~ 2%. Для животных организмов их значение велико. Функция углеводов. - энергетическая: при окислении У выделяется энергия, используемая в биохимических реакциях (при распаде 1г У выделяется ~ 4,1% ккал). - пластическая: продукты обмена У являются источниками для синтеза Ж, Б, НК, АК. - опорная: целлюлоза оболочек растительных клеток образует опорные ткани растений. - защитная: У учувствует в построении клеточных мембран.
Классификация углеводов
Моносахариды – это производные многоатомных спиртов, у которых одна гидрокси-группа (ОН) замещена на карбонильную С=О- (альдегидную или кето) группу. Если карбонильная группа находится в коне цепи, то моносахарид представляет собой альдегид и называется альдозой, при любом другом положении моносахарид является кетоном и наз-ся кетозой.
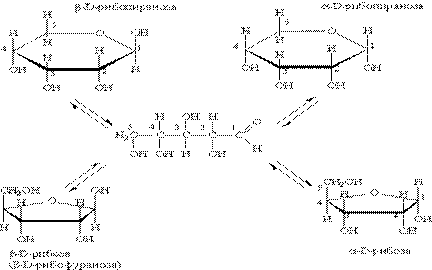
Номенклатура: наименования моносахарам дают в зависимости от числа атомов С + окончание – оза. З атома С - триоза, 4 - тетроза, 5 - пентоза, 6 - гексоза, 7 - гептоза, и т.д. Н2С - ОН Н2С – ОН Н С = О | | | С = О! НС – ОН " НС* - ОН | | | Н2С – ОН Н2С – ОН СН2 ОН дегидроксиацетон трехатомный спирт глицеральдегид (кетотриоза) (глицерин) (альдотриоза).
- Моносахара обладают оптической активностью и пространственной изомерией. N=2n, где N – число изомеров, n - количество хиральных атомов. Т.о. у альдотриозы м.б. 21=2 изомера. - Если ОН-гр. у последнего хирального атома С находится слева, то это L – ряд, а если справа, то это моносахара Д-ряда. У нас изображен Д – глицеральдегид.
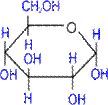
, D- глюкопираноза - Если раствор этого соединения вращает плоскость поляризованного луча вправо, то обозначает «+», а если влево, то знаком «-». Направление угла вращение заранее непредсказуемо: например природная глк (+), а фрк (-). - Формулы моносахаридов м.б. линейными и циклическими. Их называют соответственно формулами Фишера и Хеуорса.
- В зависимости от того, ОН-гр. какого из углеродов атомов участвует в образовании полуацетеля, могут образоваться пяти – или шестичленные циклы, которые по аналогии с органическими соединениями называются фуранозными или пиранозными структурами. - В циклических молекулах пентоз и гексоз появляется еще один хиральный атом и новая пара изомеров (α- и ß- формы). Если Он-гр. у С1 располагается над плоскостью, то это ß- форма, а если под плоскостью, то это α -форма.
Олигосахариды – это сложные молекулы, содержащие в своем составе от 2-х до 10 мономеров звеньев. Различают дисахариды, трисахариды и т.д. Дисахариды– это сложные молекулы, которые при гидролизе распадаются на 2 молекулы моносахаридов. Мальтоза – состоит из 2-х молекул α-глюкозы, соединенных 1"4 гликозидной связью
α -Д-глюкопиранозил (1"4) α –Д-глюкопираноза Изомальтоза –состоят из 2-х молекул α -Д-глюкозы, (1"6) гликозидной связью α -Д-глюкопиранозил (1"6) α –Д-глюкопираноза Целлобиоза – состоит из 2-х молекул ß-глюкозы, соединненых 1"4 глик. связью
Сахароза – состоит из α-глюкозы и ß-фруктозы, соединенных 1"2 гликозидной связью
α -Д-глюкопиранозил (1"2) ß –Д-глюкофуранозаранозид
Трисахариды – раффиноза (фруктоза+глюкоза+галактоза) Полисахариды – это глициды, содержащие от 10 до несколько тысяч мономеров. По строению высшие полиозы делят на следующие группы: I. Гомополисахариды, состоящие из остатков одного какого-либо моносахарида: а) из остатков глюкозы — крахмал, гликоген, декстран, целлюлоза и др.; б) из остатков маннозы, галактозы, ксилозы, L-арабинозы — маннаны, галактаны, ксиланы, арабаны; в) из остатков галактуроновой кислоты — пектиновые вещества; г) из остатков глюкозамина — хитин насекомых и грибов II. Гетерополисахариды, состоящие из остатков различных моносахаридов и их производных: а) гемицеллюлозы(в-ва крови); б) камеди, слизи; в) мукополисахариды или протеиногликаны (свободные и связанные с белками, например, в гликопротеинах: гепарин, хондроитинсульфаты, групповые вещества крови). По биологическим функциям высшие полиозы делят на следующие группы: I. Структурные полисахариды, играющие опорную роль в организмах растений и животных: целлюлоза и пектиновые вещества растений, хитин насекомых и грибов. П. Резервные полисахариды, являющиеся источником энергии для живых организмов: крахмал, гликоген, инулин.
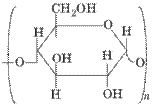
Крахмал [C6 H10 O5]n; Мr 105 – 107 Д. Это резервный гомополисахарид, состоит из 2-х гомополисахаридов; амилозы – линейной формы, и амилопектина – разветвленной формы. Доля амилозы ~10-30%, сод. до 1 тысяч остатков глк. в амилопектине (его доля в крахмале ~ 90-70%) глюк. остатков в 20-30 раз больше. Остатки глк в амилозе и линейных участках амилопектина соединяется 1"4 гликозидной связью; в (·) разветвления 1"6 гликозидной связью.
Амилопектин амилоза Гликоген – главный энергетический резерв человека и животных. Особенно много его в печени (до 10%) и мышцах (до 4% от сухой массы). Состоит также из амилопектина, только молекула более компактная, т.к. имеет более разветвленную структуру. [C6 H10 O5]n – формула аналогична формуле крахмала. Mr 105 – 108Да Крахмал и гликоген при кислотном гидролизе распадаются сначала на декстрины, затем на дисахариды – мальтозу и изомальтозу, затем на две глк. Целлюлоза (клетчатка) – это структурный полисахарид растительного происхождения, состоящий из ß - D – глюкопиранозных остатков, соединенных 1"4 гликолизидной связью. Mr=1-2млн Да. В организме человека и животных не переваривается; т.к. отсутствует фермент ß–глюкозидаза. В присутствии в пище оптимального количества целлюлозы формируются каловые массы.
Обмен углеводов Складывается из 1) расщепления полисахаридов в ЖКТ до моносахаров, которые всасываются из кишечника в кровь; 2) синтеза и распада гликогена в тканях; 3) анаэробного и аэробного расщепления глк; 4) взаимопревращения гексоз; 5) аэробного метаболизма ПВК; 6) глюконеогенеза - синтеза глк из неуглеводных компонентов – ПВК, лактата глицерина, АК и др. источников. Основной метаболит в обмене углеводов – это глюкоза. Её источники: 1) углеводы пищи 2) гликоген 3) ПВК, АК, глц и т.д.
Переваривание углеводов (крахмала). 1. Ротовая полость. Слюна содержит ф-т амилазу α, ß, γ (различаются по конечным продуктам их ферментативного действия). α–амилаза – это эндоамилаза, которая действует на 1"4 внутренние связи полисах. ß- и γ-амилазы – это экзоамилазы – расщепляют концевые 1"4 связи ß–амилаза – дисахарид мальтозу; γ амилаза – один за другим концевые остатки глк. Амилаза слюны представлена только α–амилазой, поэтому результатом ее действия являются крупные обломки гликогена и крахмала – декстрины и в небольшом количестве мальтоза. 2. Желудок. Далее пища, более или менее смоченная слюной, поступает в желудок. В результате кислой среды желудка (рН 1,5 – 2,5) α–амилаза слюны инактивируется. В глубоких слоях пищевого комка действие амилазы продолжается и происходит расщепление полисахаридов с образованием декстринов и мальтозы. В самом желудке распада У нет, т.к. здесь отсутствует специфические энзимы. 3. Основной этап расщепления У происходит в 12 перстной кишке. В просвет кишечника выделяется панкриатическая α-амилаза (рН – 7). Панкреатическая амилаза расщепляет только 1"4 гликозидные связи. Но, как известно, молекула гликогена разветвленная. В точках ветвления 1"6 гликозидной связи, на нее воздействует специфические ф-ты: (глюкоза) олиго–1,6–глюкозидаза и (крахмал) а мило-1,6–глюкозидаза. В кишечнике под действием этих 3-х ф-тов У расщепляются до дисахаридов (мальтоза и др.). На связи в дисахаридах эти ферменты не воздействуют. Для этих целей в кишечнике существует свои ферменты: их название – корень дисахарида + аза: мальтаза, сахараза и т.д. В результате суммарного воздействия этих Е образуется смесь моносахаридов – глк, галактоза, фруктоза. Основную массу составляет глюкоза.
4.Всасывание глк происходит за счет активного транспорта с Na+. Глк + Na+ образует комплекс, который поступает внутрь клетки, здесь комплекс распадается, Na+ выводится наружу. Другие моносахара всасываются диффузно (т.е. по градиенту концентрации). Поступающая из просвета кишечника глк большей частью (> 50%) с кровью воротной вены поступает в печень, остальная глк через общий кровоток транспортируется в другие ткани. Концентрация глк в крови в норме поддерживается на постоянном уровне и составляет 3,33 – 5,55 мкмоль/л, что соответствует 80-100 мг в 100 мл. крови. Транспорт глк в клетки носит характер облегченной диффузии, но в многих клетках регулируется гормоном поджелудочной железы инсулино м (исключение – мозг и печень – здесь содержание глк. прямо пропорционально конц. глк в крови). Действие инсулина приводит к перемещению белков переносчиков из цитозоля в плазматическую мембрану. Затем с помощью этих белков глк транспортируется в клетку по град. концентрации. Инсулин т.о. повышает проницаемость клеточной мембраны для глк.
Влияние инсулина на перемещение транспортёров глюкозы из цитоплазмы в плазматическую мембрану. 1 - связывание инсулина с рецептором; 2 - участок инсулинового рецептора, обращённый внутрь клетки, стимулирует перемещение транспортёров глюкозы. 3,4-транспортёры в составе содержащих их везикул перемещаются к плазматической мембране клетки, включаются в её состав и переносят глюкозу в клетку. . ЛЕКЦИЯ 12 СИНТЕЗ И РАСПАД ГЛИКОГЕНА Наиболее важным углеводом организма человека является глюкоза. Она поступает с пищей, в глюкозу превращаются углеводы в печени, из глюкозы могут образоваться все остальные углеводы в организме. Она является универсальным топливом. Глюкоза превращается в гликоген в печени, и гликоген служит источником глюкозы в организме. Биосинтез гликогена – гликогенез происходит в процессе пищеварения (в течении 1-2 часов после приема углеводной пищи). Особенно активно гликогенез происходит в печени и мышцах: 1– 2. Фосфорилирование глк
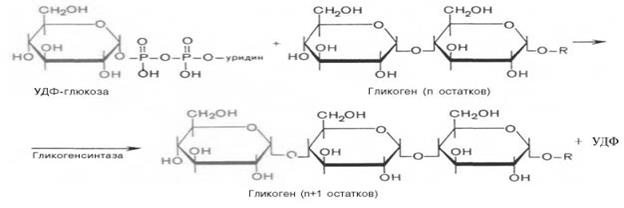
Катализирует реакцию фермент гексокиназ а. В печени также есть фермент глюкокиназа класс Трансферазы. Клеточная мембрана проницаема для глк, но не проницаема для фосфорилирования, глк как бы запирается в клетке. 3. Через фосфодиэфирную связь глюкоза соединяется с УДФ. УДФ–глк. является активированной формой глк, непосредственно включающейся в реакцию полимеризации. УДФ – глюкоза переносит глюкозный остаток на затравочное количество гликогена, уже имеющегося в мышцах или печени. Глюкозо-1-фосфат + УТФ < = > УДФ-глюкоза + Н4Р2О7 (пирофосфат)
4.
5. УДФ + Н3РО4 нуклеозиддифосфаткиназа УТФ Ост. АТФ При этом АТФ → АДФ
Т.о. строятся линейные отрезки гликогена, т.е. образуется 1→4 гликозидные сязи. Образование разветвлений в молекуле гликогена происходит под действием специфического гликогенветвящего фермента амило(α1,4→α1,6)трансгликозилазы, который переносит короткие фрагменты (по 2-3 глюкозных остатка) с одного участка гликогена на другой и образует 1,6-гликозидные связи (точка ветвления). Путем чередования действия этих двух ферментов наращивается молекула гликогена. Е гликогенсинтетаза находится в организме в двух формах: фосфорилированная или неактивная форма, которая называется гликогенсинтетаза Д; нефосфорилированная или активная гликогенсинтетаза I. Переход этих форм друг в друга происходит с помощью двух ферментов: Киназы гликогенсинтетазы Фосфотазы гликогенсинтетазы АДФ
гликогенсинтетаза I фосфотаза гликогенсинтетаза Д
Среднее содержание гликогена в печени колеблется в пределах 5-7% а) при нормальном смешанном питании глк превращается в - гликоген 3% - жиры 30% - окисляется до СО2, Н2О – 70% б) при обильном углеводном питании глк превращается в - гликоген 10% - жиры 40% - окисляется до СО2, Н2О – 50% в) при голодании в течении суток почти весь гликоген без остатка утилизируется и его не удается обнаружить в печени обычными биохимическими реакциями. Содержание гликогена в печени зависит от его синтеза (гликогенеза) или распада (гликогенолиза). Распад гликогена (гликогенолиз) происходит двумя путями
_______________________________________________________________
Фосфоролиз (+Фн) гидролиз (+Н2О)
Лактат (гликолиз) Гидроли з гликогена (крахмала) происходит в ЖКТ под действием специфических амилаз. Энергетически более выгодным является второй путь расщепления гликогена – фосфоролиз. Фосфоролитический распад играет ключевую роль в мобилизации полисахаридов. гликогенфосфорилаза
где (С6Н10О5)n означает полисахаридную цепь гликогена, а (С6Н10О5)n,– ту же цепь, но укороченную на один глюкозный остаток. В этой реакции от нередуцирующего конца отщепляется один остаток глюкозы и соединяется в фосфорной кислотой, процесс повторяется многократно, пока весь полимер не будет расщеплен до точки ветвления. Образуется остаточный декстрин. Другой фермент изоамилаза, разрывает 1→6 гликозидные сязи, далее для действия фосфорилазы отрывается новый участок полисахаридной цепи. Фосфоролиз энергетически более выгоден, т.к. в результате образуется глюкоза уже в активированном состоянии – глюкоза-1-фосфат, которая легко вступает в различные реакции
Гликоген
Фн 1
Глюкоза-6-фосфат
Анаэробный гликолиз Синтез глюкозы (лактат)
Синтез глюкозы из глицерина
|
||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-12-14; просмотров: 699; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.62 (0.01 с.) |





 АК Глюкоза глн. Ж.К. (моносахара)
АК Глюкоза глн. Ж.К. (моносахара) СН3 S
СН3 S | | ЛК-Е2 ¦ ТПФ-Е1 + Н3С-С-S-ЛК-Е2
| | ЛК-Е2 ¦ ТПФ-Е1 + Н3С-С-S-ЛК-Е2
 ацетил липоатЕ2 + НSКоА ¦ НS ЛК·Е2 + СН3СО~SКоА
ацетил липоатЕ2 + НSКоА ¦ НS ЛК·Е2 + СН3СО~SКоА НS ЛК·Е2 + Е3ФАД¦ S
НS ЛК·Е2 + Е3ФАД¦ S
 S
S амид ЛК (окисл. форма).
амид ЛК (окисл. форма).

 (мальтоза)
(мальтоза) ß-целлобиоза (1"4)
ß-целлобиоза (1"4)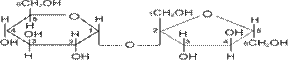 (сахароза)
(сахароза)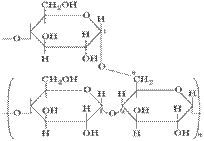






 АТФ киназа
АТФ киназа
 Нефосфорил-я, активнаяфосфорилир.неактивная
Нефосфорил-я, активнаяфосфорилир.неактивная гликоген
гликоген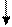

 Глюкоза-1-фосфат глюкоза
Глюкоза-1-фосфат глюкоза
 (C6H10O5)n+ H3PO4 (C6H10O5)n–1+ Глюкозо-1-фосфат,
(C6H10O5)n+ H3PO4 (C6H10O5)n–1+ Глюкозо-1-фосфат,

 Глюкоза-1-фоосфат
Глюкоза-1-фоосфат

 1. глк-1-ф фосфоглюкомутаза глк-6-ф
1. глк-1-ф фосфоглюкомутаза глк-6-ф


