
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Строение атома и систематика химических элементовСодержание книги Похожие статьи вашей тематики
Поиск на нашем сайте
ХИМИЯ Методические указания для самостоятельной работы студентов очной и заочной форм обучения
Часть 1
Факультеты: ИСФ, ЭЭФ, ФПМ и ИТ, ФЭ Для всех направлений бакалавриата
Вологда УДК 620.1
Химия: Методические указания для самостоятельной работы студентов очной и заочной форм обучения. Часть 1. – Вологда: ВоГТУ, 2012, - 32 с.
Первая часть включает в себя контрольные вопросы и задачи по основным разделам химии 1 части программы. В каждой теме предлагается 25 задач различной степени сложности. В конце методических указаний приведена таблица с вариантами выполнения работ для студентов.
Утверждено редакционно-издательским советом ВоГТУ
Составители: Тихановская Г.А., канд. биол. наук, доцент Воропай Л.М., канд. хим. наук, доцент Мальцева С.Б., канд. техн. наук, доцент Фокичева Е.А., канд. техн. Наук, доцент Ерехинская О.П., ассистент
Рецензент: Лебедева Е.А. канд. техн. наук, доцент кафедры ВиВ Вологодского государственного технического университета
ОБЩИЕ МЕТОДИЧЕСКИЕ УКАЗАНИЯ
Курс общей химии - одна из основных дисциплин, которая является фундаментом для изучения общеинженерных и специальных дисциплин. Работа студента над курсом общей химии состоит из самостоятельного изучения материала по учебникам и учебным пособиям, выполнения контрольных и самостоятельных работ, сдачи зачета и экзамена по всему курсу. Курс общей химии включает следующие большие темы: 1. Введение. Основные законы и понятия химии. 2. Строение атома и систематика химических элементов. 3. Химическая связь. 4. Типы взаимодействия молекул. Комплексные соединения. 5. Химия вещества в конденсированном состоянии. 6. Энергетика химических процессов. Химическое равновесие в гомогенных и гетерогенных системах. 7. Химическая кинетика. 8. Растворы. 9. Электрохимические процессы. 10. Коррозия и защита металлов и сплавов. 11. Химия металлов. 12. Химия неметаллических элементов. 13. Химия вяжущих веществ. 14. Элементы органической химии. Органические полимерные материалы. 15. Химия воды. 16. Электрохимические процессы в энергетике и машиностроении. 17. Химия и охрана окружающей среды. В процессе изучения курса общей химии студенты - заочники должны выполнить контрольную работу.
Перед выполнением контрольной работы необходимо изучить соответствующие разделы курса по учебникам. Ответы на вопросы должны быть ясными и четкими. Решение задач должно включать расчетные формулы, уравнения химических реакций, математическое выражение законов и правил, числовые значения констант с указанием, откуда они взяты. В случае необходимости следует проводить краткое пояснение при выполнении вспомогательных расчетов. Задача должна быть решена простейшим путем. Контрольная работа выполняется аккуратно в отдельной тетради, четким почерком. Для замечаний рецензента необходимо оставлять поля 4-5 см. Номера и условия задач следует переписывать в том порядке, в каком они указаны в задании. Контрольная работа должна быть подписана студентом с указанием даты ее выполнения. В соответствии с замечаниями рецензента студент вносит исправления и дополнения в конце тетради, а не в рецензируемом тексте. Если контрольная работа не зачтена, ее нужно выполнить заново с учетом замечаний рецензента и выслать на повторное рецензирование вместе с незачтенной работой. Контрольная работа, выполненная не по своему варианту, преподавателем не рецензируется и не зачитывается. Каждый студент выполняет вариант контрольной работы, номер которой совпадает с двумя последними цифрами номера его студенческого билета (шифра). ОСНОВНЫЕ ПОНЯТИЯ И ЗАКОНЫ ХИМИИ 1. Сравните число молекул, содержащееся в 4 кг H2SO4, с числом молекул, содержащемся в 4 кг HNO3. В каком случае и во сколько раз число молекул больше? 2. Масса 10–3 м3 газа (н.у.) равна 1,175 3. Масса 87 4. Какой объем оксида азота (II) образуется при взаимодействии 0,5 5. Где содержится больше молекул: в 10–3 м3 хлора при 230С и давлении 98 500 Па или в 10–3 м3 оксида углерода при 550С и давлении 10 600 Па? 6. Газовая смесь состоит из 5
7. Газовая смесь состоит из оксида и диоксида азота. Вычислите объемные доли газов в смеси, если парциальные давления газов соответственно равны 39 990 и 66 650 Па. 8. На восстановление 3,6 9. Олово образует два оксида. Первый содержит 78,8%, второй - 88,2% олова. Вычислите эквивалентную массу олова в этих соединениях и эквивалентную массу оксидов. 10. Из 1,35 г оксида металла получается 3,15 г его нитрата. Вычислите эквивалентную массу этого металла. 11. Из 1,3 г гидроксида металла получается 2,85 г его сульфата. Вычислите эквивалентную массу этого металла. 12. Оксид трехвалентного элемента содержит 31,58% кислорода. Вычислите эквивалентную, мольную и атомную массы этого элемента и эквивалентную массу оксида. 13. Избытком гидроксида калия подействовали на растворы: а) дигидрофосфата калия; б) нитрата дигидроксовисмута (III). Напишите уравнения реакций этих веществ с КОН и определите их эквиваленты и эквивалентные массы. 14. В каком количестве Cr(OH)3 содержится столько же эквивалентов, сколько в 174,96 г Mg(OH)2? 15. Найдите эквивалентную массу двух металлов по следующим экспериментальным данным: навеска первого металла массой 2,0000 г и навеска второго массой 1,0582 г образуют оксиды массой соответственно равной 2,5036 и 2,0000 г. 16. Определите эквивалентную массу алюминия и количество выделившегося газа, если известно, что для растворения 5,4 г алюминия потребовалось 99,6 мл 20%-ного раствора соляной кислоты, плотностью ρ=1,1 г/см3. 17. Эквивалентная масса некоторого элемента равна 24,99 г/моль. Вычислите: а) массовую долю (%) кислорода в оксиде этого элемента; б) объем (м3) водорода, который потребуется для восстановления 4,95 18. Вычислите эквивалентную массу цинка, если 1,168 19. При восстановлении 5,1 20. Определите эквивалентную массу двухвалентного металла, если 14,2 21. Рассчитайте эквивалентную массу металла, если при получении средней соли некоторого металла на каждые 2 22. 4,086 23. В лаборатории имеются два различных хлорида железа. Анализ их показал, что в одной соли содержится 34,5% железа, в другой - 44,1%. Определите эквивалентную массу железа в этих соединениях, если известно, что 2,24 л (н.у.) хлора соединяются с 2,24 л (н.у.) водорода. 24. Для растворения 8,43 25. Определите массу металла, вытеснившего из кислоты 0,7 ХИМИЧЕСКАЯ СВЯЗЬ 76. Что называют линией связи и углом связи, или валентным углом? Как называют связь, которая образуется перекрыванием электронных облаков вдоль линии связи? Приведите примеры образования σ-связи.
77. Почему при наличии одной связи между атомами она может быть только σ-связью? При каких условиях образуются π-? Для всех ли форм электронных облаков возможно образование этих связей? 78. Приведите примеры молекул, которые содержат между соседними атомами: а) только σ-связи; б) одну σ- и одну π-связи, в) одну σ- и две π-связи. Сколько σ- и π-связей содержат молекулы: CC14, SO3, C2H4, C2H2? 79. Перечислите возможные типы гибридизации s- и p-орбиталей. В каком из них гибридные орбитали по энергии и форме в наибольшей степени приближаются к исходной s- или p-орбитали? 80. Какие АО не могут участвовать в гибридизации? Возможна ли гибридизация орбиталей: а) 3p- и 4s-; б) 4s- и 5р-; в) 4s- и 4р-; е) 4s-, 4p- и 4d-? Почему? 81. Какое влияние оказывает не поделённая электронная пара на углы между связями? Как это можно объяснить? Почему угол НОН в молекуле Н2О меньше угла HNH в молекуле NH3? 82. Какую связь называют водородной и почему ее образуют только те атомы водорода, которые связаны с атомами наиболее электроотрицательных элементов? Назовите их. 83. Почему для молекул H2S и НС1 в отличие от Н2О и НF образование водородных связей не характерно? 84. Чем объяснить значительно более высокие температуры плавления и кипения воды и фтороводородной кислоты по сравнению с теми, которые должны соответствовать их молярным массам? 85. Покажите схемами два возможных механизма образования ковалентной связи. При какой структуре электронных оболочек атомов возможен тот и другой случай? Влияет ли механизм образования ковалентной связи на ее свойства? 86. Какие атомы или ионы называют донорами и акцепторами электронных пар? Приведите примеры. 87. Кроме таких параметров, как энергия и длина связи, какими тремя свойствами характеризуется ковалентная связь? Что понимается под насыщаемостью ковалентной связи и чем она определяется? 88. Чем объясняется способность многих элементов к образованию числа связей, превышающего число неспаренных электронов в их атомах? Какое состояние атома называют основным и возбужденным? Приведите примеры. 89. Сравните возможности промотирования электронов в атомах азота, кислорода и фтора с теми же возможностями в атомах аналогов по группе, например, фосфора, серы и хлора. 90. Сколько валентных электронов и валентных АО имеют атомы: С и Si; N и Р; О и S? Чему равна максимальная ковалентность элементов 2-го и 3-го периодов?
91. На примере ряда соединений объясните, как влияет на устойчивость гибридного состояния центрального атома плотность гибридизируемых облаков. Ряд соединений: NH3 92. Что такое sр3-гибридизация электронных облаков? Какую пространственную конфигурацию имеют молекулы веществ с таким типом гибридизации? Приведите примеры соответствующих соединений. 93. Какую ковалентную связь называют полярной? Что служит количественной мерой полярности ковалентной связи? Исходя из значений электроотрицательности атомов соответствующих элементов определите, какая из связей: HJ, JCl, BrF - наиболее полярна. 94. Распределите электроны атома серы по атомным орбиталям. Сколько неспаренных электронов имеет атом серы в основном и возбужденном состояниях? Чему равна валентность серы, обусловленная неспаренными электронами? 95. Нарисуйте энергетическую схему образования молекулы He2 и молекулярного иона He 96. Какую химическую связь называют ионной? Каков механизм ее образования? Какие свойства ионной связи отличают ее от ковалентной? Приведите два примера типичных ионных соединений. Напишите электронные уравнения превращения соответствующих ионов в нейтральные атомы. 97. Что следует понимать под степенью окисления атома? Определите степень окисления атома углерода и его валентность, обусловленную числом неспаренных электронов, в соединениях СН4, СН3ОН, НСООН, СО2. 98. Какие силы молекулярного взаимодействия называют ориентационными, индукционными и дисперсионными? Когда возникают эти силы и какова их природа? 99. Нарисуйте энергетическую схему образования молекулярного иона Н 100. Нарисуйте энергетическую схему образования молекулы О2 по методу молекулярных орбиталей (МО). Как метод МО объясняет парамагнитные свойства молекулы кислорода? ХИМИЧЕСКАЯ КИНЕТИКА 151. Начальные концентрации веществ, участвующих в реакции СО + Н2О 152. Начальные концентрации веществ, участвующих в реакции N2 + 3H2 ↔ 2NH3, равны (моль 153. Написать выражение скорости химической реакции, протекающей в гомогенной системе по схеме А + 2В = С, и определить, во сколько раз увеличится скорость реакции, если: а) концентрация А увеличится в 2 раза; б) концентрация В увеличится в 2 раза; в) концентрация А и В увеличится в 2 раза. 154. Во сколько раз следует увеличить давление, чтобы скорость образования NO2 по реакции 2NO + O2 = 2NO2 возросла в 1000 раз? 155. Реакция между веществами А и В выражается уравнением 2А + В ↔2С. Начальная концентрация вещества А равна 0,3 моль
156. Реакция идет по уравнению 2NO + O2 ↔ 2NO2. Начальные концентрации реагирующих веществ были (моль 157. Чему равна скорость химической реакции, если концентрация одного из реагирующих веществ в начальный момент была равна 1,2 моль 158. При взаимодействии SO2 и О2 концентрация последнего уменьшилась за 1 ч на 0,25 моль 159. На сколько градусов следует повысить температуру, чтобы скорость реакции возросла в 8 раз (γ = 2)? 160. При повышении температуры на 600 скорость реакции увеличилась в 4000 раз. Вычислить γ. 161. При повышении температуры на 420 скорость реакции увеличилась в 320 раз. Вычислить γ. 162. При повышении температуры на 200 скорость реакции возросла в 9 раз. Чему равен температурный коэффициент этой реакции? ХИМИЧЕСКОЕ РАВНОВЕСИЕ РАСТВОРЫ. СВОЙСТВА РАСТВОРОВ 201. Требуется вычислить давление пара раствора, содержащего 0,2 моля сахара в 450 г воды. Давление пара чистой воды при 200С равно 17,5 мм рт.ст. 202. Давление пара воды при 200С составляет 17,54 мм рт.ст. Сколько граммов сахара С12Н22О11 следует растворить в 720 г воды для получения раствора, давление пара которого на 0,14 мм рт.ст. ниже давления пара воды? 203. Определите относительную молекулярную массу анилина, если при 300С давление пара раствора, содержащего 3,09 г анилина в 370 г эфира С4Н10О равно 643,6 мм рт.ст. а давление пара чистого эфира при той же температуре равно 647,9 мм рт.ст. 204. При растворении 0,94 г фенола С6Н5ОН в 50 г спирта точка кипения повысилась на 0,2320. Определите относительную молекулярную массу фенола, если эбуллиоскопическая константа спирта 1,160С. 205. Вычислите, на сколько градусов понизится температура замерзания бензола, если в 100 г его растворить 4 г нафталина С10Н8. Криоскопическая константа бензола 5,120С. 206. При какой температуре будет кипеть 50%-ный водный раствор С12Н22О11? Эбуллиоскопическая константа воды 0,512. 207. В каком количестве воды следует растворить 23 г глицерина С3Н8О3, чтобы получить раствор с температурой кипения 100,1040С. Эбуллиоскопическая константа воды 0,5120С. 208. Раствор, содержащий 5,4 г неэлектролита в 200 г воды, кипит при 100,0780С. Вычислить относительную молекулярную массу растворенного вещества, если эбуллиоскопическая константа воды 0,5120С. 209. Раствор, приготовленный из 2 кг этилового спирта С2Н5ОН и 8 кг воды, залили в радиатор автомобиля. Вычислить температуру замерзания раствора, если криоскопическая константа воды 1,860С. 210. Для охлаждения цилиндров автомобильных, тракторных и авиационных двигателей в морозную погоду, когда вода может замерзнуть во время стоянок, применяют антифризы - водные растворы, не замерзающие при низких температурах. Допустив, что закон Рауля справедлив для раствора нижеуказанного состава, вычислите, при какой температуре замерзнет раствор этиленгликоля С2Н4(ОН)2 массовой долей 0,40. Криоскопическая константа воды 1,860С. 211. Какой массы сахароза находится в растворе объемом 200 мл, если осмотическое давление этого раствора при 00С равно 6,61 212. Раствор, содержащий глюкозу массой 7,252 г в воде массой 200 г, замерзает при –0,3780С. Криоскопическая константа воды 1,860С. Определите относительную молекулярную массу глюкозы и относительную ошибку в процентах по сравнению с величиной, найденной по таблице Д.И.Менделеева. 213. Сколько граммов глюкозы нужно растворить в воде массой 100 г, чтобы повышение температуры кипения было равно 10? Считать, что в этом случае применим закон Рауля. Эбуллиоскопическая константа воды 0,5120С. 214. Сколько бензойной кислоты (С7Н6О2) растворено в уксусной кислоте массой 100 г, если температура замерзания последней понизилась на 0,8240? Криоскопическая константа уксусной кислоты 3,90С. 215. Температура замерзания бензола 5,50С, а раствора, содержащего в бензоле массой 25,04 г неизвестное вещество массой 0,4678 г, 4,8720С. Криоскопическая константа воды 5,120С. Вычислите относительную молекулярную массу неизвестного вещества. 216. Раствор, содержащий 2,7 г фенола С6Н5ОН в 75 г бензола, замерзает при 3,50С, тогда как чистый бензол замерзает при 5,50С. Вычислите криоскопическую константу бензола. 217. Вычислить давление пара 10%-ного водного раствора сахара С12Н22О11 при 1000С. 218. При растворении камфоры (С10Н15О) массой 0,298 г в бензоле массой 21,2 г температура кипения повысилась на 0,2360. Эбуллиоскопическая константа бензола 2,60С. Вычислите относительную молекулярную массу камфоры и относительную ошибку опыта в процентах по сравнению с величиной, найденной по атомным массам элементов. 219. При 100С давление пара воды равно 1227,8 Па. Для того, чтобы понизить давление пара до 1200 Па, в воде какой массы надо растворить СН3ОН массой 16 г? 220. Определите относительную молекулярную массу глюкозы, если осмотическое давление раствора, содержащего 6 г глюкозы в 1 л раствора, равно 0,82 атм при 270С. 221. Вычислите осмотическое давление 4%-ного раствора сахара С12Н22О11 при 200С, если плотность раствора равна 1,014 г 222. Сколько граммов глюкозы С6Н12О6 содержится в 200 мл раствора, осмотическое давление которого при 370С составляет 8 атм.? 223. Осмотическое давление раствора, в 250 мл которого содержится 0,66 г мочевины, равно 836 мм рт.ст. при 330С. Вычислите относительную молекулярную массу мочевины. 224. Чему равно при 170С осмотическое давление раствора глюкозы, в котором ее массовая доля составляет 0,10 (ρ=1,0377 г 225. При 200С плотность раствора в котором массовая доля сахарозы составляет 0,17, равна 1,067 г ГИДРОЛИЗ СОЛЕЙ 251. При смешивании растворов Al2(SO4)3 и Na2S в осадок выпадает гидроокись алюминия Al(OH)3. Объяснить причину и привести соответствующие уравнения реакций. 252. При сильном разбавлении водой раствора Bi(NO3)3 выделяется обильный белый осадок, представляющий собой смесь основных солей висмута (дигидроксонитрат и гидроксодинитрат висмута). Написать уравнения реакций образования указанных солей. В какую сторону сместится рН среды в результате гидролиза нитрата висмута? 253. Гидролиз раствора FeCl3 при нагревании идет ступенчато и заканчивается образованием осадка Fe(OH)3. Представить уравнениями все три ступени этого процесса (3 уравнения) и вывести суммарное уравнение. 254. При смешении растворов Al2(SO4)3 и Na2CO3 в осадок выпадает Al(OH)3. Указать причину образования осадка и составить соответствующие уравнения. 255. При взаимодействии ацетата свинца с карбонатом натрия в водной среде получился осадок состава (PbOH)2CO3 и PbCO3. Составить уравнение. 256. При смешении концентрированных растворов FeCl3 и Na2CO3 образуется Fe(OH)3 и выделяется CO2. Представить ионные уравнения соответствующих реакций. 257. В какую сторону сместится равновесие гидролиза КСN, если к раствору прибавить: а) щелочь; б) кислоту? Напишите уравнение гидролиза в молекулярном и ионном виде. 258. Подберите по два уравнения в молекулярном виде к каждому из кратких ионных уравнений: а) Fe3+ + 2H2O↔Fe(OH) б) (CO3)2– + H2O↔(HCO3)– + oh–; в) (NH4)+ + H2O↔NH4OH + H+. 259. К раствору FeCl3 добавили следующие вещества: а) Hcl; б) koh; в) ZnCl2; г) Na2CO3. В каких случаях гидролиз хлорида железа (III) усилится? Почему? Составьте ионно-молекулярные уравнения гидролиза соответствующих солей. 260. К раствору Na2CO3 добавили следующие вещества: а) Hcl; б) NaOH; в) Cu(NO3)2; г) K2S. В каких случаях гидролиз карбоната натрия усилится? Почему? Составьте ионно-молекулярные уравнение гидролиза соответствующих солей. 261. К раствору Al2(SO4)3 добавили следующие вещества: а) H2SO4; б) KOH; в) Na2SO3; г) ZnSO4. В каких случаях гидролиз сульфата алюминия усилится? Почему? Составьте ионно-молекулярные уравнения гидролиза соответствующих солей. 262. Какая из двух солей при равных условиях в большей степени подвергается гидролизу: Na2CO3 или Na2SO3; FeCl3 или FeCl2? Почему? Составьте ионно-молекулярные и молекулярные уравнения гидролиза этих солей. 263. Какая из двух солей при равных условиях в большей степени подвергается гидролизу: NaCN или NaClO; MgCl2 или ZnCl2? Почему? Составьте ионно-молекулярные и молекулярные уравнения гидролиза этих солей. 264. Составить ионные и молекулярные уравнения реакций, протекающих при смешивании растворов: Cr2(SO4)3 и K2CO3, FeCl3 и Na2CO3, FeCl3 и NaCN. Иметь в виду, что в каждой реакции гидролиз обеих солей доходит до конца. 265. Составить молекулярное и ионное уравнения реакций, протекающей при смешивании растворов FeCl3 и NaC2H3O2, считая, что гидролиз FeCl3 идет до образования основной соли FeOH(C2H3O2)2. 266. Указать характер среды растворов солей: K2SiO3, NaBr, KClO3, Cu(NO3)2. 267. Составить молекулярные и ионные уравнения гидролиза солей: CaS, Na2SiO3, ZnSO4, CrCl3, Fe2(SO4)3. 268. При смешивании растворов сернокислого алюминия и соды Na2СO3 гидролиз обеих солей доходит до конца, вследствие чего реакция протекает по ионной схеме Al3+ + CO
H2O CO2 Составить ионное и молекулярное уравнения реакции, имея в виду, что при взаимодействии ионов число их находится в обратном отношении к валентности. 269. При смешивании растворов CrCl3 и (NH4)2S гидролиз обеих солей доходит до конца Cr3+ + HOH S2– + HOH Составить ионные и молекулярные уравнения реакции гидролиза обеих солей при их смешивании, имея в виду, что образующиеся при гидролизе ионы Н+ и ОН– нейтрализуют друг друга. 270. При смешивании растворов Pb(C2H3O2)2 и Na2CO3 выпадает осадок состава (PbOH)2CO3 и PbCO3. Составить ионное и молекулярное уравнения реакции. 271. Какие из пар солей в водных растворах взаимно усиливают гидролиз: Cr2(SO4)3 и K2S; Al(NO3)2 и ZnCl2; Al(NO3)3 и Na2S. Написать уравнения реакций, мотивирующие ответ. 272. Почему растворы К2СО3 и NaCN имеют щелочную реакцию, а растворы NH4Cl и ZnCl2 - кислую? Ответ подтвердите, составив уравнения гидролиза в молекулярном и ионном виде. 273. При сливании растворов CrCl3 и Na2CO3 образуется осадок гидроксида хрома (III). Объясните причину этого явления и напишите соответствующие уравнения в молекулярном и ионном виде. 274. Составьте ионно-молекулярное и молекулярное уравнения совместного гидролиза, происходящего при смешивании растворов K2S и CrCl3. Каждая из взятых солей гидролизуется необратимо до конца с образованием соответствующих основания и кислоты. 275. Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей Pb(NO3)2, Na2CO3, Fe2(SO4)3. Какое значение рН (>7<) имеют растворы этих солей?
ВАРИАНТЫ КОНТРОЛЬНЫХ РАБОТ
|

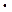 10–3 кг. Вычислите молекулярную массу газа и массу одной молекулы газа.
10–3 кг. Вычислите молекулярную массу газа и массу одной молекулы газа. PH3
PH3  по методу МО и объясните невозможность существования молекулы He2?
по методу МО и объясните невозможность существования молекулы He2? и молекулы Н2 по методу молекулярных орбиталей. Где энергия связи больше? Почему?
и молекулы Н2 по методу молекулярных орбиталей. Где энергия связи больше? Почему? = 0,6. Как изменится скорость реакции, если концентрацию кислорода увеличить до 0,9 моль
= 0,6. Как изменится скорость реакции, если концентрацию кислорода увеличить до 0,9 моль  + 2H+;
+ 2H+; + HOH
+ HOH 




