
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Прилади, лабораторний посуд, реактивиСодержание книги
Поиск на нашем сайте
Оптична лава, мікроскоп, електроди, хімічна склянка, пробірки, піпетки, неорганічні солі та органічні речовини. Завдання на виконання роботи 1. Одержати колоїдні розчини за допомогою стандартних методик Бредига, Крекке, Грема. Всі одержані гідрозолі перевірити на наявність світлорозсіювання (ефект Тіндаля). 2. Приготувати емульсії різних типів. 3. Приготувати рідкі піни. Порядок виконання роботи № 9.1 Одержання гідрозолю срібла методом Бредига Для одержання гідрозолю металевого срібла в пристрої Бредига через заглиблені у воду срібні електроди пропускають електричний струм. Процес росту частинок срібла припиняється в області колоїдної дисперсності, якщо в систему ввести стабілізатор у вигляді 1 %-го розчину желатину або розчину електроліту, наприклад лугу. Частинки утвореного золю заряджені негативно.
Порядок виконання роботи № 9.2
Одержання золю методом заміни розчинника Сірка розчинна у спирті і не розчинна у воді; якщо спиртовий розчин сірки влити у воду, виникає гідрозоль сірки. Стабілізатором одержаного золю є оксиди сірки, присутні в ній, як домішки. Аналогічно розчиняючи водою 2 %-й розчин парафіну або каніфолі, можна одержати відповідні гідрозолі. Для приготування колоїдного розчину в пробірку з водою доливають з крапельниці спиртовий розчин сірки або каніфолі до виникнення опалесценції.
Порядок виконання роботи № 9.3
Одержання гідрозолю гідроксиду заліза гідролізом хлорного заліза за Крекке В конічній пробірці нагрійте до кипіння 85 мл дистильованої води. Відміряйте піпеткою 15 мл 2%-го розчину хлорид заліза і невеликими порціями вилийте в кип’ячу воду. Кип’ятіння продовжуйте ще 2-3 хв. Спостерігайте утворення червоно-коричневого золю гідроксиду заліза. Утворення гідрозолю гідроксиду заліза відбувається в результаті гідролізу FeCl3. Метод гідролізу часто застосовують для отримання золів гідроксидів важких металів. Наприклад, хлорид заліза реагує з водою за рівнянням: FeCl3 + 2H2O= Fe(OH)2Cl + 2HCl. З підвищення температури ступінь гідролізу збільшиться і утворюються частинки малорозчинного компоненту Fe(OH)3: Fe(OH)2Cl +Н2О= Fe(OH)3 + HCl. При охолодженні реакція іде в зворотному напрямку. Тому отриманий гідрозоль необхідно ще теплим піддати діалізу. Запишіть склад міцели гідрозолю гідроксиду заліза. Отриманий розчин піддайте діалізу.
Порядок виконання роботи № 9.4 Одержання золю гідроксиду заліза Гремом методом пептизації Для одержання золю до 1 н розчину FeCl3 поступово додають (чекаючи переходу в золь утворюваного осаду) при перемішуванні по краплях 2 н розчин (NH4)2CO3 до одержання темно-червоного прозорого золю гідроксиду заліза:
Порядок виконання роботи № 9.5
Перевірка на ефект Тіндаля Всі одержані золі слід перевірити на наявність світлорозсіювання. Для цього пробірку з колоїдним розчином встановлюють на оптичну лаву і збоку освітлюють пучком світла або направляють на розчин лазерний промінь. Якщо шлях променя видно – у дисперсній системі наявні колоїдні частинки, що розсіюють світло. Якщо пучок світла пропускають через справжній розчин, світлорозсіювання майже відсутнє, шлях променя непомітний, і систему можна вважати гомогенною, оптично порожньою. Порядок виконання роботи № 9.6 Одержання емульсії типу М/В У пробірку наливають рівні об’єми води і бензолу, перемішують за допомогою скляної палички, яка вільно переміщується вздовж пробірки. Одержана емульсія швидко розшаровується. Потім у ту саму пробірку додають кілька краплин 2 %-го розчину мила або желатину. Після перемішування утворюється стійка емульсія. Для визначення типу емульсії в пробірку з нею вносять кілька краплин бензольного розчину барвника і перемішують.
Порядок виконання роботи № 9.7 Одержання емульсії типу В/М У пробірку наливають 6 мл 1 %-го розчину каучуку в бензолі, 2 мл води і перемішують. Додають дві краплі розчину барвника. Тип утвореної емульсії визначається під мікроскопом або методом розтікання краплини по парафіновій поверхні.
Порядок виконання роботи № 9.8 Одержання емульсій, стабілізованих порошками У пробірку з бензолом або з керосином насипають золу і додають 2 мл води, перемішуючи вміст скляною паличкою. За методом зафарбовування визначають вид одержаної емульсії. Для одержання емульсії типу м/в у пробірку з водою вносять порошок глини або крейди, потім додають масло і перемішують.
Порядок виконання роботи № 9.9 Емульсії соняшникової олії у воді До 5 мл Н2О додають дві краплі масла і п’ять крапель 0,1 н розчину NaOH. Утворюється стійка емульсія масла у воді, стабілізована утвореним натрієвим милом. Вид одержаної емульсії можна визначити одним з описаних способів.
Порядок виконання роботи № 9.10 Властивості пін У воду додати кілька крапель 2 %-го розчину мила або желатину. При струшуванні утворюється стійка піна, час життя якої зростає зі збільшенням концентрації піноутворювача. Для зруйнування піни, в циліндр вносять одну-дві краплі 2 %-го розчину ізоамілового спирту або сірчистого ефіру. Вплив концентрації та природи піноутворювача на стійкість піни можна спостерігати, якщо в циліндр місткістю 100 мл з притертою пробкою налити 50 мл дистильованої води і дві краплі ізоамілового спирту. Після стандартного струшування (5 – 10 разів) за допомогою секундоміра визначають час життя піни. Дослід повторюють, збільшуючи загальну кількість спирту до 30 краплин. Дослід повторюють в аналогічній послідовності з розчинами желатину, сапоніну або мила.
Опрацювання результатів
На основі аналізу результатів дослідів та перевірки наявності світлорозсіювання слід зробити висновок про можливість отримання колоїдних розчинів та емульсій різними методами.
Питання для самоперевірки
1. Які розчини називають колоїдними? 2. Які існують методи одержання колоїдних розчинів? 3. Які існують методи одержання емульсій? 4. Сформулюйте основні умови одержання колоїдних розчинів. 5. Поясність будову міцели гідро золю. 6. Запишіть формулу колоїдної міцели AgJ з позитивно зарядженою частинкою та вкажіть її структурні одиниці. 7. Запишіть формулу колоїдної міцели AgJ з негативно зарядженою частинкою та вкажіть її структурні одиниці. 8. Сформулюйте правило Панета-Фаянса.
Лабораторна робота № 10
|
||||
|
Последнее изменение этой страницы: 2016-08-14; просмотров: 360; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.191.237.176 (0.008 с.) |

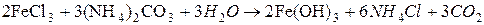 .
.


