
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Феноменологическое описание фазовых переходов в нефтяных дисперсных системах.Содержание книги
Поиск на нашем сайте
Нефть с позиций физической химии (и механики сплошных сред) может рассматриваться как молекулярный раствор и как коллоидно-дисперсная система. Границы такого определения являются размытыми и определяются составом нефтяной системы, а также термодинамическими условиями, в которых она находится. С позиций коллоидной химии нефть – многокомпонентная смесь, которая в зависимости от внешних условий проявляет свойства молекулярного раствора или дисперсной системы (с размером микрогетерогенных частиц 10-5—10-7м). В отличие от нефтяных эмульсий, образование которых связано с диспергированием макроскопических фаз нефтяные дисперсные системы в большинстве случаев образуются в результате протекания фазовых переходов, за счет конденсационного образования дисперсной фазы. Процесс фазового перехода протекает самопроизвольно, если сопровождается убылью термодинамического потенциала Гиббса. Химический потенциал – (парциальный молярный потенциал Гиббса)
где Химический потенциал для реального раствора содержит коэффициент активности:
Фазовые переходы протекают через образование дисперсных частиц. Нефтяные дисперсные системы занимают промежуточное состояние между молекулярными растворами и макроскопическими гетерогенными системами. Дисперсная (коллоидная) структура НДС оказывает несомненное влияние на протекание в них теплообменных и гидродинамических процессов (т. е на их физико-химические макросвойства). В общей теории рассматриваются все стадии фазовых переходов от формирования зародышей с существенно искривленной поверхностью раздела фаз до полного перехода в макрофазу с плоской границей раздела.
СПОСОБЫ ФОРМИРОВАНИЯ НДС. Диспергирование газообразных, жидких и твердых тел. При этом образуются дисперсные системы со значительной межфазной поверхностью. В процессе диспергирования возрастает свободная поверхностная энергия и энтропия, связанная с тепловым движением коллоидных частиц. В случае превышения энтропии над свободной поверхностной энергией формирование коллоидной системы оказывается термодинамически выгодным процессом и может протекать самопроизвольно, особенно в дисперсных системах с газообразной и жидкой дисперсионной средой. Диспергирование является результатом воздействия следующих факторов. o Механических воздействий; o Воздействие химических реагентов — регуляторов межмолекулярного взаимодействия; o Комбинирования механических и химических факторов; o Физические превращения —конденсация, кипение, экстракция, кристаллизация; o Химические превращения (крекинг, полимеризация, поликонденсация, алкилирование). Для того, чтобы произошел фазовый переход необходимо пресыщение исходной фазы. Степень пресыщения оценивается отношением давления или концентрации вещества в перенасыщенном растворе к аналогичным показателям насыщения над плоской поверхностью. Путем введения дополнительного вещества (добавок) возможно изменить степень пресыщения и регулировать скорость образования и размер формирующихся зародышей Формирование фазообразующих компонентов. Кинетика образования новой фазы определяется двумя факторами скоростью образования зародышей v1 и скоростью их роста v2. Для получения значительного числа зародышей необходимо, чтобы v1 -v2>0. В этом случае возможно образование коллоидных растворов. Введение различных веществ в систему позволяет регулировать значение ΔV и его знак стимулировать необходимое направление процессов. Фаза и межфазный слой Фазой — называется однородная часть системы с тождественным химическим составом, одинаковым физическими и термодинамическими свойствами, отделенная от других частей межфазной поверхностью при переходе через которую свойства меняются скачкообразно. Состояние системы строго определяется совокупностью ее термодинамических параметров (Р,V,T). Еще в работах Гиббса показано, что при термодинамическом анализе систем следует различать состояния устойчивого, неустойчивого и относительно устойчивого равновесия. Состояние устойчивого термодинамического равновесия (стабильное) характеризуется тем, что если каким-либо внешним воздействием вывести из него рассматриваемую систему, а затем снять это внешнее воздействие, то система сама возвратится в исходное состояние равновесия. Неустойчивое (лабильное) состояние характеризуется тем, что если систему вывести из него, то она уже не вернется в исходное состояние, а перейдет в новое — состояние устойчивого равновесия. Для выведения системы из лабильного состояния достаточно весьма малых внешних воздействий. Состояние относительно устойчивого равновесия (метастабильное) — это состояние, в котором система может находиться достаточно долго. При этом небольшие по величине внешние воздействия, вызывающие малые отклонения системы из метастабильного состояния, не приводят к переходу в другое состояние; после того как такое внешнее воздействие снято, система возвращается в исходное метастабильное состояние. С другой стороны, достаточно сильное воздействие выведет систему из метастабильного состояния в равновесное. Тоже самое должно произойти, если система будет находиться в метастабильном состоянии в течение большого промежутка времени. Одним из наиболее часто встречающихся в природе примеров являются состояния перенасыщения (переохлаждения) паров или перегрева жидкости. На примере НДС перенасыщение одним (или несколькими) растворенным компонентом.
Для иллюстрации на рис показан характер изотерм пара при переохлаждении и жидкости при ее перегреве в PV- диаграмме.
Линия s-s характеризует равновесный изобарно-изотермический процесс в двухфазной области, соответствующей стабильным состояниям среды. Линии sa и sb соответствуют метастабильному состоянию вещества (переохлажденный пар или перегретая жидкость). Точки a и b характеризуемые равенством Геометрическое место точек, определяемых равенствами Связь между размером такого критического зародыша и перенасыщением (переохлаждением) устанавливает уравнение Кельвина:
Где σ –поверхностное натяжение жидкости
Теория зародышеобразования и соотношения для определения скорости ядрообразования нами рассматриваться не будет. Далее используем модель, согласно которой перенасыщенный раствор состоит из смеси одиночных молекул растворенного вещества и молекулярных ассоциаций, которые могут рассматриваться как зародыши новой фазы. Межфазный (сольватный) слой – состоит из элементов структуры дисперсионной фазы (межфазный продукт) и характеризуется высотой H, т. е имеет объем. Кинетика формирования сольватного слоя для одного из вариантов НДС рассматривается позднее. Процесс фазообразования в нефтяных дисперсных системах можно разделить на три стадии 1. Образование дозародышей, имеющих докритические размеры (фазообразования не происходит, так как возникающие вследствие флуктуаций дозародыши термодинамически неустойчивы и раcпадаются в исходной фазе); 2. Формирование зародышей критических размеров, находящихся в неустойчивом равновесии с исходной фазой, по гомогенному или гетерогенному механизму; 3. Самопроизвольный рост критических зародышей, приводящий к развитию фазообразования во всем объеме нефтяной системы.
Рис.2. Стадия фазового перехода в нефтяной системе Третья стадия характеризуется агрегативной и кинетической неустойчивостью двухфазной системы, в которой начинается перемещение дозародышей или структурных единиц СЕ (слой А), переход путем седиминтации СЕ в развитый межфазный слой (В), последующим разрушением (коалесценцией) СЕ и образованием фазы с минимальной межфазной поверхностью (слой С). Работа формирования зародышей критических размеров по гетерогенному и гомогенному механизмам связана соотношением [117]: Агет= K Агом Коэффициент К зависит от краевого угла смачивания и может изменяться от 1 до 0. При хорошем смачивании поверхности посторонних включений, работа образования новой фазы будет снижаться и составлять только часть работы формирования зародышей по гомогенному механизму. Независимо от механизма фазообразования поведение сформировавшихся гетерогенных систем будет определяться соотношением сил тяжести возникших частиц и противодействием движению за счет сил вязкого сопротивления, ( определяемых законом Стокса F= 6πηrυ, Где η - вязкость дисперсной среды; r – радиус частицы; υ – скорость движения. В случае очень вязких сред образовавшиеся частицы фиксируются во все объеме дисперсионной среды в строго определенном положении. Характерна постоянная частичная концентрация частиц в объеме дисперсной среды (ДС) В этой стадии неоднородности имеют некоторые возможности для роста своих размеров, но они не могут преодолеть сил сопротивления среды и в ней зависают – «замораживаются». Так формируются материалы, имеющие важное значение в промышленности (коксы, сажи, адсорбенты, нефтеносные породы), различные вяжущие и пластичные нефтепродукты (битумы, пеки,пластичные смазки и др.) Пек (от голл. pek — смола) — остаток от перегонки каменноугольного, торфяного, древесного дёгтя, а также нефтяной смолы (после пиролиза ). При ударе раскалывается с раковистым изломом; под постоянной нагрузкой проявляет пластичность. Твердая (иногда вязкая) масса черного цвета. В составе каменноугольного пека преобладают высокомолекулярныеароматические углеводороды; содержатся высшие фенолы и органическиеоснования. Нерастворимая часть включает свободный углерод (8-30 %, в зависимости от температуры размягчения П.), золу (0,2 % и выше) и асфальтены. Плотность пека 1,2-1,3 г/см³. Пеки неэлектропроводны, нерастворимы в воде (торфяной и древесный содержат малые количества водорастворимых веществ), растворяются во многих органических растворителях ( пиридине, бензоле и др.); устойчивы к действию кислот. Применяют в производстве гидроизоляционных материалов, пекового электродного (беззольного) кокса, топливных брикетов, в дорожном строительстве, для изготовления толя, рубероида, при изготовлении лаков для окраски металлоконструкций и др. Углеродный пек используется в качестве исходного сырья для получения углеродных волокон. Первая стадия формирования НДС уже влияет на ее физико-химические свойства (появляется структурно-механическая прочность, происходит перераспределение углеводородов, возникают каталитические эффекты и др,). На второй стадии фазовые переходы в гетерогенной системе полностью еще не происходят, они находятся в состоянии, устойчивом против расслоения (образование структурных единиц критических размеров). Лекция №4 На третьей стадии вокруг надмолекулярных структур (структурных единиц второй стадии) образуется сольватный слой, что приводит к образованию ССЕ. ССЕ может взаимодействовать с дисперсионной средой. В этом случае возможны два варианта. Первый, когда поверхностное натяжение дисперсионной среды меньше, чем у сольватных оболочек ССЕ. В результате взаимодействия части сложной структурной единицы с дисперсионной средой формируется активная ССЕ с нескомпенсированной поверхностной энергией. Активированная ССЕ стремится к компенсации свободной энергии, что достигается при слиянии двух или нескольких активированных ССЕ друг с другом,, сопровождающимся ростом размеров надмолекулярной структуры во вновь созданной ССЕ. Чем больше разница между поверхностными энергиями надмолекулярной структуры и дисперсионной среды ( Второй вариант— поверхностное натяжение дисперсионной среды значительно больше, чем у сольватного слоя ССЕ. Такое соотношение Самые распространенные факторы воздействия на фазовые переходы дисперсных систем — температура, давление, введение активных добавок, применение механических и ультразвуковых полей. При определенном групповом составе и совокупности внешних условий нефтяная дисперсная система имеет оптимальную структуру, которая соответствует экстремумам в изменении ее физико-химических и эксплуатационных свойств Переход в экстремальное состояние сопровождается изменением состава надмолекулярной структуры и сольватной оболочки структурных единиц при соответствующем изменении межфазной энергии и поверхности, раздела фаз. Перевод нефтяных дисперсных систем в экстремальное состояние под действием совокупности внешних факторов — основа интенсификации нефтетехнологических производств. Коллоидно-дисперсное строение нефтяных систем. Формирование дисперсной фазы в нефтяных системах обусловлено различной склонностью углеводородов к межмолекулярным взаимодействиям, которые проявляются при исследовании ряда физико-химических свойств системы, в том числе и спектральных. Однако при исследовании многокомпонентных нефтяных систем последние малоэффективны из-за наложения в спектрах многообразных форм межмолекулярных взаимодействий. Необходимость оценки межмолекулярных взаимодействий в многокомпонентных углеводородных системах требует разработки специальных способов их теоретического описания и экспериментальных методик. Согласно современному уровню представлений о межмолекулярных взаимодействиях возможно их количественное описание для двух молекул с учетом их природы. Теоретические соотношения типа уравнения Леннарда — Джонса описывают взаимодействие двух молекул как взаимодействие двух микроскопических шариков. (Если бы молекулы только притягивались друг к другу, это привело бы к их слиянию. Но на очень малых расстояниях их электронные оболочки начинают отталкиваться. Энергия отталкивания дается выражением E = + k / rn, Где k - постоянная отталкивания, n принимает различные целые значения (5-15). Силы межмолекулярного отталкивания действуют на очень малых расстояниях. Общее уравнение межмолекулярного взаимодействия при постоянной температуре (уравнение Леннарда-Джонсона) в большинстве случаев имеет вид E M = − a / r 6 + b / r 12 и носит название "потенциала 6-12", поскольку энергия притяжения пропорциональна 1 / r 6, а энергия отталкивания - 1 / r 12. Читать дальше >>> ) Потенциальная энергия взаимодействия U двух изолированных молекул в зависимости от расстояния между их центрами имеет форму кривой с минимумом (рис. 1). Уравнения Лондона для универсальных дисперсионных сил и Кеезома для диполь-дипольных взаимодействий молекул в первом приближении описывают интервал правой ветви кривой, отвечающий большим значениям R. Левая ветвь кривой, характеризуемая резким возрастанием потенциала при сближении молекул, отвечает их отталкиванию и описывается эмпирическим потенциалом Буккингема.
Рис. 1. Потенциальная энергия взаимодействия U двух молекул в зависимости от расстояния R между ними. Рис. 2. Модель строения структурной единицы: — радиус ассоциата; H — толщина сольватной оболочки.
Интервал значений R, соответствующий минимуму U, определяет область устойчивого взаимодействия двух молекул — наиболее интересную и наименее изученную область в теории жидкостей. В данной области значений R действуют так называемые слабые химические связи, в основном лишь количественно отличающиеся от сильных: энергия образования слабых связей на 1—2 порядка меньше, чем энергия образования сильных валентных связей. Один из распространенных типов слабых химических связей — водородные X—,., Y, образующиеся между многими атомами X и Y, где X — атом, имеющий сильную химическую связь с водородом, a Y — практически любой атом. Так, наряду с обнаруженными давно связями вида О—Н... О, характеризуемыми энтальпией образования около 21 кДж/моль, установлено образование водородных связей вида С—Н... О и С—Н... С, энтальпия образования которых ниже, примерно, на порядок по сравнению с энтальпией связи О—Н... О. Основной вклад в образование молекулярных ассоциатов вносят водородные связи. Энергия образования каждой связи составляет 5,5 ± 1,5 кДж/моль. Обнаружена ассоциация жидких алканов за счет водородных связей С—Н... С с энергией образования в зависимости от типа углеродного атома (первичный, вторичный, третичный) 2—4 кДж/моль. Для жидкостей, состоящих из неполярных и малополярных молекул, потенциальная энергия межмолекулярного взаимодействия определяется слабыми химическими связями. В сложных по составу многокомпонентных нефтяных системах происходят коллективные взаимодействия молекул, теоретическое описание которых представляет собой весьма трудную и пока не разрешенную задачу. Результат коллективных взаимодействий молекул низко- и высокомолекулярных (с молекулярной массой 1000 и выше, а также смолы и асфальтены) соединений в нефтяных системах описывается с помощью модельных представлений о формировании структурных элементов различных типов. Для обозначения структурного элемента нефтяных дисперсных систем в общем случае принят термин «сложная структурная единица». Структурная единица представляет собой элемент структуры преимущественно сферической формы, способный к самостоятельному существованию при данных неизменных условиях. В составе сложной структурной единицы различают внутреннюю область (или ядро) и сольватную оболочку, окружающую ядро (рис. 2). Классификация структурных единиц в нефтяных дисперсных системах (НДС) приведена в табл. 7 Таблица 7. Классификация структурных единиц в НДС.
Внутренняя область сложных структурных единиц представлена соответственно кристаллитом, ассоциатом или пузырьком газовой фазы. В отличие от двух последних кристаллиты карбенов, карбоидов являются необратимыми надмолекулярными структурами, не способными к разрушению до молекулярного состояния под действием внешних факторов. Исторически первая попытка описания строения структурной единицы применительно к асфальтенам принадлежит Пфейферу. Согласно его представлениям, ядро структурной единицы асфальтенов образовано высокомолекулярными полициклическими углеводородами и окружено компонентами с постепенно снижающейся степенью ароматичности. Нейман подчеркивает, что энергетически
Рис. 3. Экстремальная зависимость радиуса ассоциата R от состава системы бутанол — вода
выгодно обращение полярных групп (СООН, СО, ОН к др.) внутрь сложной структурной единицы, а углеводородных радикалов— наружу, что находится в соответствии с правилом уравнивания полярностей Ребиндера. Благодаря современным методам анализа установлены способы построения структурной единицы смолисто-асфальтеновых веществ различных нефтей. Согласно данным рентгеноструктурного анализа надмолекулярная структура асфальтенов состоит из 5—б слоев полиядерных двухмерных пластин общей толщиной 1,6—2,0 нм. Размеры надмолекулярных структур, определенные рентгенографически, имеют заниженные значения по сравнению с таковыми, найденными электрономикроскопически, что, вероятно, связано с включением при определении размеров по электронным микрофотографиям алифатической части молекул, в то время как рентгеновские лучи рассеиваются только упорядоченной частью или ядром молекулы. Ассоциат и пузырек газовой фазы — лабильные образования, состав и размеры которых изменяются обратимо под воздействием внешних факторов. При смешении чистых компонентов происходит распад ассоциатов, характерных для данных компонентов (или компонента), и образование новых, свойственных уже данной смеси. Возможность такого процесса подтверждается тем, что при формировании многих систем наблюдается расширение и поглощение теплоты, которая, очевидно, расходуется на подобные преобразования ассоциатов. Следствием образования ассоциатов различных размеров и состава являются отклонения в поведении систем от законов Рауля. Анализ изобар бинарных систем показывает возможность существования следующих типов температурных кривых кипения: 1) кривые, отвечающие изменению температуры кипения смеси без образования азеотропной точки (как известно, состав пара и жидкости азеотропной смеси одинаков); 2) кривые, отвечающие изменению температуры кипения смеси с образованием азеотропа. Сведения об изменении давления паров чистых компонентов по сравнению со смесью этих компонентов наряду с другими справочными данными позволяют рассчитать с использованием формулы Томсона — Кельвина размеры ассоциатов (рис. За).
Рис. 3а. Экстремальные кривые кипения системы бутанол — вода: D — диаметр пузырей. В пользу справедливости предположения о том, что ассоциаты являются центрами образования, пузырей при кипении системы, свидетельствует факт, что характер кривых зависимости диаметр пузырей — состав системы, полученных экспериментальным и расчетным путем, одинаков (рис. 3а). Литературные данные по степеням агрегации сложных структурных единиц различных типов и распределению их по размерам малочисленны. Имеются сведения о том, в достаточно разбавленных асфальтенсодержащих системах размеры основной части диспергированных асфальтенов (70 %) колеблются в интервале 0,1—1 мкм Методом рассеяния рентгеновского излучения под малыми углами установлено [123], что коллоидная структура битумов состоит из набора частиц квазисферической формы с размерами от 2,3—3,0 до 20—40 нм. Число частиц наименьшего размера на 4—6 порядков превышает число частиц больших размеров, что дает основание считать частицы с размерами 2,3—3,0 нм основными структурными элементами коллоидной структуры битумов. При фазообразовании, вследствие неоднородности полей, в исходной фазе обычно получаются как первичные, так и вторичные ССЕ различных размеров, различной степени дисперсности, т. е. образуется ряд полидисперсных ССЕ, поведение которых существенно отличается от монодисперсных. Полидисперсность ССЕ удобно характеризовать кривыми распределения, наглядно показывающими долю частиц определенного размера (рис. 15).
Рис. 15. Типичные кривые распределения дисперсных частиц в дисперсионной среде: 1 — система, наиболее приближающаяся к монодисперсной; 2 — наиболее полидисперсная система; Кривые распределения могут иметь один или два максимума, которые определяют наиболее вероятный радиус частиц — преимущественное содержание фракций частиц в полидисперсной НДС. Форма кривой распределения ССЕ в НДС имеет важное научное и практическое значение: чем меньше интервал кривой распределения и чем выше ее максимум, тем НДС ближе к монодиспероной. На основании кривых распределения рассчитывают средние размеры частиц НДС. Внешними воздействиями (смешение нефтей различной природы, добавки поверхностно-активных или инактивных веществ, изменение веществ, изменение рН среды, различных полей: тепловых, механических — акустических, электромагнитных, ультразвуковых, изменение скоростей нагревания и охлаждения и др.; электрических и др.) представляется возможным в значительных пределах изменять средние размеры ССЕ в НДС.
Формирование сольватных слоев определенной толщины и строения вокруг надмолекулярных структур оказывает существенное влияние на структурно-механические свойства нефтяных дисперсных систем. Термодинамическое обоснование их формирования было дано Гиббсом [124], допустившим, что переходный слой (межфазная граница) имеет определенную толщину и термодинамические параметры, промежуточные между значениями параметров сосуществующих фаз. Межфазная граница становится неустойчивой при натяжении порядка ~10 дин/см. Для нефтяных систем неустойчивость межфазной границы структурных единиц возрастает из-за воздействия следующих факторов: 1. Отдельные компоненты нефтяной системы представляют собой набор гомологов. В зависимости от строения, длины цепи гомологи имеют различное поверхностное натяжение. Обладающие большей подвижностью и меньшим значением поверхностного натяжения гомологи концентрируются в межфазной области и облегчают процесс диспергирования при нагреве или действии механических напряжений. 2. Наличие в смеси естественных, а также введенных извне в систему ПАВ приводит к их поглощению структурными единицами. 3. Обогащение межфазного слоя низкомолекулярным компонентом происходит из-за влияния искривления граничной поверхности раздела фаз [125]. Межфазная граница в нефтяных системах может быть двух типов: а)непроницаемой по отношению к ряду растворителей (кристаллиты карбенов и карбоидов) в) частично проницаемой (ассоциаты). В первом случае на межфазной границе образуется адсорбционный слой, непосредственно примыкающий к кристаллиту, и граничный (поверхностный) слой, включающий в себя адсорбционный, свойства которого в результате влияния поля поверхностных сил отличаются от объемного слоя. При рассмотрении нефтяных смесей с дисперсной фазой в виде ассоциатов следует, по-видимому, считать, что сольватный слой на границе раздела фаз возникает как результат адсорбционного взаимодействия и локальной диффузии ее компонентов, что обусловлено их различной склонностью к межмолекулярным взаимодействиям. Обобщая случаи адсорбции и абсорбции (твердое тело — газ, раствор — газ, твердое тело — раствор), следует сказать, что во всех случаях формируются адсорбционно-сольватные слои различной толщины (от моно- до полислоя). В одних случаях адсорбционно-сольватные слои образуются с внешней стороны (пузырек, ассоциат, кристаллит), в других — с внутренней (поры, трещины). Общие закономерности: 1. Толщина адсорбционно-сольватного слоя h зависит от природы ядра, кривизны его поверхности и качества дисперсионной среды. В одной и той же дисперсионной среде при равных значениях размера ядра (r = const) h растет в ряду газ—жидкость- твердое тело. В такой же последовательности растет значение силового поля вокруг ядра ССЕ. 2. При изменении внешними воздействиями баланса сил в НДС представляется возможным в широких пределах (от /г монослоя до /г полислоя) регулировать геометрические размеры адсорбционно-сольватных слоев. 3. Изменение геометрических размеров адсорбционно-сольватного слоя влияет на его физико-химические свойства и в целом на свойства ССЕ и НДС. В связи с этим одни и те же соединения, находящиеся в адсорбционно-сольватном слое и дисперсионной среде, принципиально отличаются по своим физико-химическим свойствам. 4. Избирательный переход в результате внешних воздействий соединений из дисперсионной среды в адсорбционно-сольватный слой и, наоборот, приводит к перераспределению углеводородов между фазами, что имеет важное значение для практики. 5. Наличие и значение толщины адсорбционно-сольватных слоев вокруг ядер ССЕ влияет на температуру фазовых переходов в НДС (температуры кипения, застывания, кристаллизации и др.). Толщина адсорбционно-сольватных слоев измеряется различными методами. Впервые понятие о сольватном слое асфальтеновых частиц ввел Нейман []. Образование межфазных слоев в асфальтенсодержащих системах определяется природой и адсорбционными свойствами асфальтенов. Исследованиями структурно-механических свойств граничных слоев в нефтяных системах установлено, что толщина поверхностного слоя в битумах может меняться от 10 мкм до 5 мкм при увеличении их прочности. Характеристики поверхностного слоя в битумах зависят от полярности образующих его компонентов. При изучении адсорбции пленок нефти и битума на минеральных подложках установлено повышение концентрации асфальтенов в адсорбционном слое, что приводит не только к изменению его свойств, но и свойств поверхностных слоев, прилегающих к адсорбционному. Классификация нефтяных дисперсных систем по агрегатному состоянию дисперсной фазы и дисперсной среды приведены в табл. 8. Наиболее распространены в практике трубопроводного транспорта дисперсные системы с жидкой дисперсионной средой. ТАБЛИЦА 8. Типы нефтяных дисперсных систем (НДС)
Наименьшим временем жизни из рассматриваемых дисперсных систем характеризуется газовая эмульсия, неустойчивость которой связана с достижением критических значений толщины сольватных слоев. Ассоциаты различного строения являются структурными элементами алкансодержащих дисперсий, топливных и масляных фракций, нефтяных остатков. Активно исследуемым коллоидным объектом нефтяного происхождения являются алкансодержащие дисперсии. Высокомолекулярные нормальные алканы в обычных условиях, начиная с гексадекана и выше, представляют собой твердые вещества. По мере понижения температуры из нефти выделяются кристаллы алкана. Благодаря действию адсорбционных сил часть жидкой фазы ориентируется вокруг надмолекулярных структур и образует сольватные оболочки различной толщины. Сцепление кристаллов приводит к возникновению пространственной гелеобразной структуры, в ячейках которой иммобилизована часть дисперсионной среды, при этом система в целом приобретает структурную прочность. Установлено стабилизирующее действие смолисто-асфальтеновых веществ на устойчивость дисперсий алканов. Влияние термообработки на снижение температуры застывания нефтяных алканов объясняется уменьшением толщины сольватной оболочки их надмолекулярных структур. Исторически первыми среди объектов нефтяного происхождения, подвернутыми изучению именно с позиций их коллоидно-дисперсного строения, были остаточные фракции нефти — битумы. Впервые экспериментально была обнаружена коллоидная природа битумов в 1923 г. Неллештейном. При исследовании модельных бинарных систем обнаружено, что самопроизвольно образующиеся обратимые эмульсии существуют в определенном интервале концентраций и температур, вне которого они разрушаются с образованием двух макрофаз или являются гомогенной системой.
ЛЕКЦИЯ 5 Мерой оценки степени развития фазообразования является соотношение размеров сверхкритического зародыша и дозародыша. В результате интенсивного фазообразования формируется грубо-дисперсная система с ее характерной склонностью к агрегативной неустойчивости. Если плотность ρ вновь формиру
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2016-08-06; просмотров: 1120; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.41 (0.013 с.) |


 - стандартный химический потенциал компонента i при том же давлении и температуре, что и рассматриваемый раствор (идеальный).
- стандартный химический потенциал компонента i при том же давлении и температуре, что и рассматриваемый раствор (идеальный).
 const или
const или  являются предельными точками метастабильных состояний. Методами статистической физики показано, что при
являются предельными точками метастабильных состояний. Методами статистической физики показано, что при  const в любой точке диаграммы состояния, кроме критической точки, флуктуации плотности, которые могут играть роль центров образования устойчивой фазы, становятся бесконечно большими. В этом случае обязательно должен произойти переход в стабильное состояние. Следовательно, существование перегретой жидкости правее точки a и переохлажденного пара левее точки b невозможно.
const в любой точке диаграммы состояния, кроме критической точки, флуктуации плотности, которые могут играть роль центров образования устойчивой фазы, становятся бесконечно большими. В этом случае обязательно должен произойти переход в стабильное состояние. Следовательно, существование перегретой жидкости правее точки a и переохлажденного пара левее точки b невозможно. или
или 
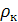 - плотность жидкой фазы;
- плотность жидкой фазы; - температура насыщения, соответствующая давлению P;
- температура насыщения, соответствующая давлению P; – теплота фазовых переходов.
– теплота фазовых переходов.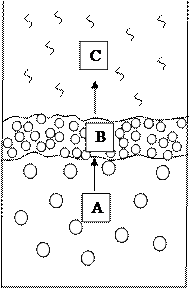
 ), тем быстрее увеличиваются размеры надмолекулярной структуры и тем больше снижается толщина сольватного слоя в ССЕ.
), тем быстрее увеличиваются размеры надмолекулярной структуры и тем больше снижается толщина сольватного слоя в ССЕ. δ приводит к вытеснению из сольватного слоя ССЕ углеводородов, обладающих малыми значениями поверхностного натяжения. При высоких значениях
δ приводит к вытеснению из сольватного слоя ССЕ углеводородов, обладающих малыми значениями поверхностного натяжения. При высоких значениях  может не только уменьшаться толщина сольватного слоя и изменяться углеводородный состав в нем, но и разрушаться надмолекулярная структура, вплоть до полного ее исчезновения.
может не только уменьшаться толщина сольватного слоя и изменяться углеводородный состав в нем, но и разрушаться надмолекулярная структура, вплоть до полного ее исчезновения.







