Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Защитные покрытия представляют собой пленки (металлические, оксидные, лакокрасочные и т.п.).Содержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте
Металлические покрытия бывают двух типов — анодные и катодные. Для анодного покрытия используют металлы, обладающие более отрицательным электродным потенциалом, чем основной металл (например, цинк, хром). Для катодного покрытия выбирают металлы, имеющие меньшее отрицательное значение электродного потенциала, чем основной металл (медь, олово, свинец, никель и др.). Металлические покрытия наносят горячим методом, гальваническим и металлизацией. При горячем методе покрытия изделия погружают в ванну с расплавленным защитным металлом, температура которого ниже, чем температура плавления изделия (цинк, олово, свинец). Гальванический метод защиты состоит в том, что на поверхности изделия путем электролитического осаждения из растворов солей создается тонкий слой защищаемого металла. Покрываемое изделие при этом служит катодом, а осаждаемый металл — анодом. Металлизация — покрытие поверхности детали расплавленным металлом, распыленным сжатым воздухом. Преимуществом этого метода защиты металла является то, что покрывать расплавом можно уже собранные конструкции. Недостаток заключается в том, что получается шероховатая поверхность. Металлические покрытия можно наносить также посредством диффузии металла покрытия в основной металл— алитирование, силицирование, хромирование (см. с. 316), а также способом плакирования, т.е. наложения на основной металл тонкого слоя защитного металла (биметалл) и зарепления его путем горячей прокатки (например, железо — медный сплав, дюралюминий — чистый алюминий). Оксидирование — защита оксидными пленками. Для этого естественную оксидную пленку, всегда имеющуюся на металле, делают более прочной путем обработки сильным окислителем, например концентрированной азотной кислотой, растворами марганцевой или хромовой кислот и их солей. Частным случаем оксидирования является воронение стали. В этом случае на поверхности также создается оксидная пленка, но более сложными приемами, связанными с многократной термической обработкой при температуре ЗО0...40О°С в присутствии древесного угля. Фосфатирование состоит в получении на изделии поверхностной пленки из нерастворимых солей железа или марганца в результате погружения металла в горячие растворы кислых фосфатов железа или марганца.
Лакокрасочные покрытия основаны на механической защите металла пленкой из различных красок и лаков. Ванны, раковины, декоративные изделия для защиты от коррозии покрывают эмалью, т. е. наплавляют на металл при температуре 750...800°С различные комбинации силикатов. При временной защите металлических изделий от коррозии (транспортировании, складировании) используют для покрытия металла невысыхающие масла (технический вазелин, лак этиноль), а также ингибиторы, т. е. вещества, замедляющие протекание реакции (нитрит натрия с углекислым аммонием, с уротропином, ингибитор ную бумагу и др.).
Изменение свойств коррозионной среды достигается или соответствующей обработкой среды, при которой уменьшается ее агрессивность (уменьшается концентрация компонентов, особенно опасных в коррозионном отношении, например, удаление кислорода деаэрацией или др. методами, подщелачивание, снижение общего содержания солей), или введением в коррозионную среду небольших добавок специальных веществ – замедлителей (ингибиторов) коррозии. Ингибиторы коррозии разделяют в зависимости от условий их применения на жидкофазные и парофазные (летучие); жидкофазные ингибиторы делят, в свою очередь, на ингибиторы коррозии в нейтральных, щелочных и кислых средах. До настоящего времени еще не удалось найти эффективных ингибиторов коррозии металлов в щелочных растворах. В качестве ингибиторов кислотной коррозии применяются почти исключительно органические вещества, содержащие азот, серу или кислород. Действие ингибиторов кислотной коррозии связано с их адсорбцией на границе раздела металл-кислота. Действие большинства ингибиторов кислотной коррозии усиливается при одновременном введении добавок поверхностно-активных анионов (галогенидов, сульфидов, роданидов). Комбинированные методы сочетают в себе два или несколько способов защиты: битумные композиции + катодная защита (подземные трубопроводы); покраска + ингибитор коррозии как один из ингредиентов красителя (механическая защита + электрохимическая); катодная поляризация + ингибиторы (в нейтральных и кислых средах). Результативный эффект комбинированной защиты обычно выше суммарного эффекта соответствующих индивидуальных методов.
Токоведущие элементы транспортной инфраструктуры, например рельсы поездов и трамваев, не имеют надежной электрической изоляции от земли. А поскольку ток возвращается по рельсам на тяговую подстанцию, то часть этого тока проходит и по земле. Заземленные сильноточные установки, а также утечки от линий электропередач аналогичным образом способствуют возникновению токов по земле. Такие токи, попросту уводящие электричество в землю, не имеют постоянной формы, амплитуды и направления, их пути распространения по земле разнообразны, потому они и называются блуждающими токами.
Понятно, что в этих случаях земля играет роль токопроводящей среды, и не только грунт является здесь проводником, но и металлические конструкции, находящиеся полностью или частично под землей, такие как трубопроводы, кабельные линии, опоры контактных сетей и т.д. Даже просто соприкасающиеся с землей металлические конструкции подвержены действию блуждающих токов. По отношению к расположенным в земле токопроводящим конструкциям, сама земля имеет потенциал более низкий. И если, например, сильноточная установка использует заземление или ток от нее отводится в землю, то он идет по пути наименьшего сопротивления, то есть проходит по находящимся в земле металлоконструкциям, что приводит к возникновению на них коррозии. Это же касается и тягового тока протекающего по ходовым рельсам. Разность потенциалов между рельсами и землей, с учетом отсутствия изоляции, обуславливает протекание части тяговых токов по земле с аналогичными, для попадающихся на пути этих токов металлических конструкций, последствиями.
Встречая на своем пути канализационную трубу, газопровод, или оболочку кабеля, которые имеют намного меньшее удельное сопротивление, чем окружающий их грунт, блуждающие токи натекают на них, и такие места называются катодными зонами. Пройдя по металлическому пути малого сопротивления, блуждающий ток выходит из него, и это место называется анодной зоной, здесь и происходит вызывающая коррозию электрохимическая реакция. Аналогичная коррозия имеет место и в анодной зоне при входе тока в землю из самого источника блуждающего тока, например из самих рельс, и рельсы тоже поэтому страдают. Таким образом, рельсы разрушаются в местах выхода из них токов в землю, а подземные коммуникации – в местах возвращения тока в рельсы.
Проблема в том, что когда утечка блуждающего тока имеет постоянный характер, металл постепенно будет разрушаться, и такая электрокоррозия может быть довольно интенсивной. Новые стальные трубопроводы могут прийти в негодность за три года, а кабели связи повреждаются еще быстрее. Аналогичным образом разрушаются рельсовые скрепления на мостах и рельсы различного назначения. Особенно опасны в коррозийном отношении источники постоянного или выпрямленного токов. В анодных зонах скорость разрушения металла может достигать 10 мм в год. Как правило, металлические конструкции оснащены специальным защитным покрытием, призванным уберечь от коррозии, однако в случае повреждения покрытия порча коммуникаций неизбежна, и в местах небольших анодных зон возникают характерные язвы и дыры.
Для защиты стальных трубопроводов от воздействия блуждающих токов применяют катодную защиту. Она осуществляется при помощи постоянного электрического тока внешнего источника. Отрицательный полюс источника тока подключается к защищаемому трубопроводу, а положительный к специальному заземлению – аноду. Схема катодной защиты - Как защитить металлические оболочки кабелей от коррозии Для уменьшения блуждающих токов связанных с рельсами, увеличивают проводимость рельсовых путей и повышают переходное сопротивление между рельсами и землёй. Для этого на главных путях укладывают рельсы тяжёлых типов, осуществляют переход на бесстыковой путь, а рельсовые стыки шунтируют медными перемычками повышенного сечения, многопутные участки соединяют параллельно. Рельсы укладывают на щебёночном или гравийном балласте, устанавливают изолирующие детали между рельсами и арматурой железобетонных шпал, а деревянные шпалы пропитывают масляными антисептиками и т.д.
22 - 24 Электролиз - это окислительно-восстановительный процесс, который происходит на электродах во время прохождения электрического тока через расплав или раствор.
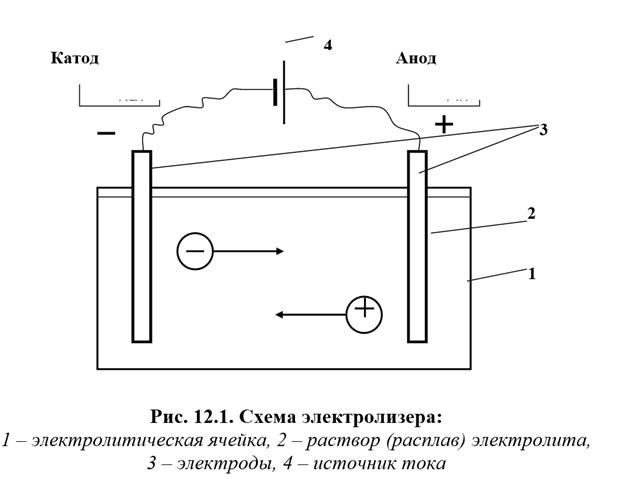
Электролизеры состоят из электролитической ячейки (в промышленности – электролизной ванны), содержащей раствор или расплав электролита, погруженных в нее электродов и источника тока. Электрод, подключенный к положительному полюсу источника тока, называется анодом, а к отрицательному полюсу – катодом. При осуществлении электролиза протекают следующие процессы: · направленное движение ионов электролита к электродам. Положительно заряженные ионы перемещаются к катоду (отсюда название этих ионов – катионы М n +), а отрицательно заряженные – к аноду (отсюда название таких ионов – анионы А nn –). · окислительно-восстановительные процессы на электродах. При достижении соответствующего электрода, ионы разряжаются (отдают или принимают электроны). При электролизе, как при любой электрохимической реакции, на аноде протекает процесс окисления, т.е. процесс отдачи электронов, а на катоде – процесс восстановления, т.е. процесс присоединения электронов · образовавшиеся на электродах вещества (ионы или нейтральные молекулы) могут покидать поверхность электродов, кроме того, они могут вступать во вторичные взаимодействия.
Характер процессов окисления на аноде и восстановления на катоде зависит от условий электролиза. При этом соблюдается строгая очередность разряда ионов.
|
||||||||
|
Последнее изменение этой страницы: 2016-06-07; просмотров: 450; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.118.1.63 (0.013 с.) |