
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Методы биофизических исследованийСодержание книги
Похожие статьи вашей тематики
Поиск на нашем сайте Биофизика. Цели науки · Познание природы · Управление природой
Используются 2 подхода познания сущности – · Интуитивный подход · Научный метод
Интуиция – форма непосредственного знания – чутье, догадка, она не требует доказательств.
Атрибутами научного метода будут являться · Опыт(эксперимент) – изучение реакций на определенные стимулы. · Измерение изучаемых параметров · Математический анализ – изучение достоверности данных явлений.
Познание функций человека – одна из труднейших задач. Развитие науки на первых этапах происходит – дифференциация дисциплин, направленных на глубокое изучение тех или иных проблем. На первом этапе мы пытаемся познать определенную часть и когда это удается сделать возникает другая задача – как составить общее представления. Возникают научные дисциплины на стыке первоначальных специальностей. Это относится и к биофизике, которая появилась на стыке физиологии, физики, физической химии и открыла новые возможности в понимании биологических процессов
Биофизика – наука, изучающая физические и физико-химические процессы на разных уровнях живой материи (молекулярном, клеточном, органном, целого организма), а также закономерности и механизмы воздействия физических факторов внешней среды на живую материю. Выделяют- · молекулярная биофизика - кинетики и термодинамика процессов · биофизика клеток – изучение структуры клеток и физико-химические проявления – проницаемость, образование биопотенциалов · биофизика органов чувств – физико-химические механизмы рецепции, трансформацию энергии, кодирование информации ив рецепторах. · Биофизика сложных системы – процессы регулирования и саморегулирования и термодинамические особенности этих процессов · Биофизика воздействия внешних факторов - исследует влияние на организм ионизирующей радиации, ультразвука, вибрации, воздействия света Задачи биофизики
Эйлер(1707-1783) – законы теории гидродинамики, для объяснения движения крови по сосудам Лавуазье (1780) – изучал обмен энергии в организме Гальвани (1786) – основоположник учения о биопотенциалах, о животном электричестве Рентген – пытался объяснить механизмы мышечного сокращения с позиции пьезо - эффектов Аррениус – законы классической кинетики для объяснения биологических процессов Ломоносов – закон сохранения и превращения энергии Сеченов - изучал транспорт газа в крови Лазарев – основоположник отечественной биофизической школы Полинг – открытие пространственной структуры белка Уотсон и Крик – открытие двойной структуры ДНК Ходжкин, Хаксли, Катц – открытие ионной природы биоэлектрических явлений Пригожин – теория термодинамики необратимых процессов Эйген – теория гиперциклов, как основа эволюции Сакман, Неер – установили молекулярную структуру ионных каналов
Биофизика становилась в связи с развитием медицины, т.к. там использовались методы физического воздействия на организма. Развивалась биология и было необходимо проникнуть в тайны биологических процессов, протекающих на молекулярном уровне Потребность промышленности, развитие которой привело к действию ан организм различных физически факторов – радиоактивное излучение, вибрации, невесомость, перегрузки Методы биофизических исследований · Рентгеноструктурный анализ – исследование атомной структуры вещества, с помощью дифракции рентгеновских лучей. По дифракционной картине устанавливают распределение электронной плотности вещества, а уже по ней можно определить, какие атомы содержатся в веществе и как они расположены. Исследование кристаллических структур, жидкостей и белковых молекул. · Колоночная хроматография – различное распределение и анализ смесей между 2 фазами – подвижной и неподвижной. Она может быть связана с различной степенью вещества абсорбции или к различной степени ионного обмена. Может быть газовой, либо жидкостной. Распределение веществ используют в капиллярах - капилярная, либо в трубках, заполненных сорбентом – колончатая. Можно проводить на бумаге, пластинках · Спектральный анализ – качественное и количественное определение вещества по оптическим спектрам. Вещество определяют либо по спектру испускания – эмиссионный спектральный анализ или по спектру поглощения – абсорбционный. Содержание вещества определяется по относительной или абсолютной толщине линий в спектре. Также относят радиоспектроскопию – электронный парамагнитный резонанс и ядерно-магнитный резонанс. · Изотопная индикация · Электронная микроскопия · Ультрафиолетовая микроскопия – исследование в УФ лучах биологических объектов повышает контрастность изображения, особенно внутриклеточных структур и она позволяет исследовать иные клетки без предварительной окраски и фиксации препарата
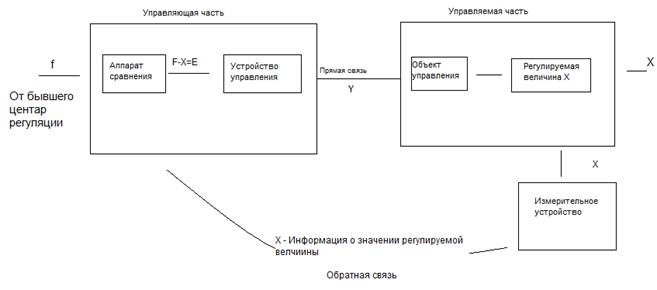
Одним из важнейших условий существования является адекватное приспособлений функций, органов и тканей, систем к среде обитания. Происходит постоянное уравновешивание организма и среды. В этих процессах основной процесс – регуляция и управление физиологическими функциями. Общие законы реализации, управления и переработки информации в разных системах изучаются наукой кибернетикой(кибернетика – искусство управления) Законы управления являются общими как у человека, так и у технических устройств. Возникновение кибернетики было подготовлено разработкой теорией автоматического регулирования, развитием радиоэлектроники, созданием теории информации. Эта работа была изложена Шенноном(1948) в «Математическая теория связи» Кибернетика. Кибернетика занимается изучением систем любой природы, способных воспринимать, хранить и перерабатывать информацию и использовать ее для управления и регулирования. Кибернетика изучает те сигналы и факторы, которые приводят к определенным процессам управления. Имеет большое значения для медицины. Анализ биологических процессов позволяет качественно и количественно изучить механизмы регулирования. Информационные процессы управления и регулирования являются определяющими в организме, т.е. являются первичными, на основе которых происходят все процессы. Системы – организованный комплекс элементов, связанных друг с другом и выполняющих определенные функции в соответствии с программой всей системы. Элементами мозга будут являться нейроны. Элементы коллектива – люди, входящие в него. Только толпа не является кибернетической системой. Программа – последовательность изменений системы в пространстве и времени, которые могут быть заложены в структуре смой системы или поступить в нее извне. Связь – процесс взаимодействия элементов друг с другом, при котором происходит обмен веществом, энергией, информацией.
Сообщения бывают непрерывными и дискретными. Непрерывное имеют характер непрерывно меняющейся величины(артериальное давление, температура, напряжение мышц, музыкальные мелодии). Дискретное – состоят из отдельных, отличающихся друг от друга ступеней или градаций(порции медиаторов, азотистое основание ДНК, точки и тире азбуки Морзе)
Важен также процесс кодирования информации. Кодируется нервными импульсами, для восприятия информации нервными центрами. Элементы кода – символы и позиции. Символы являются безразмерными величинами, которые отличают что либо(буквы алфавита, математические знаки, нервный импульс, молекулы пахучих веществ, а позиции определяет пространственное и временное расположение символов). Код информации содержит такую же информацию, как и исходное сообщение. Это явление изоморфности. Кодовый сигнал обладает очень малой энергетической величиной. Поступление информации оценивается по наличию или отсутствию сигнала. Сообщение и информация – это не одно и тоже, ибо по теории информации Информация – мера того количества неопределенности, которая устраняется после получения сообщения. Возможность наступления события - априорная информация. Та вероятность события после получения информации – апостериорная информация. Информативность сообщения будет больше, если полученные сведенья повышают апостериорную вероятность. Свойства информации. 1. Информация имеет смысл только при наличии ее приемников(потребителя) – «если в комнате стоит телевизор, и в ней никого нет» 2. Наличие сигнала не обязательно говорит о том, что предается информации, т.к. есть сообщения, которые не несут ничего нового, для потребителя. 3. Информация может предаваться как на сознательном, так и на подсознательном уровнях. 4. Если событие достоверно(т.е. его вероятность Р=1), сообщение о том, что оно произошло не несет никакой информации для потребителя 5. Сообщение о событии, вероятность которого Р < 1, содержит в себе информацию, и тем большую, чем меньше вероятность события, которого произошло.
Дезинформация – отрицательное значение информации. Энтропия (H) – Мера неопределенности событий.
H=log2 N Если log2 N=1, тогда N=2
Единица информации – бит (двойничная единица информации)
H=lg N (хартли) 1 хартли – количество информации, необходимое для выбора одной из десяти равновероятных возможностей. 1 хартли = 3,3 бит
Теория регулирования
Для осуществления регулирования используются 2 принципа – по рассогласованию и по размещению.
Регулятор может работать по возмещению, когда воздействие на организм является компенсирующим действием регулятора, что приводит к нормализации функции Управление направлено на запуск физиологических функций, на их коррекцию и на согласование процессов. Наиболее древний – гуморальный механизм регуляции. Нервный механизм. Нервно-гуморальный механизм. Развитие механизмов регуляции приводит к тому, что животные способны к движению и могут уходить из неблагоприятной среды в отличие от растений. Форпостный механизм (у человека) – в форме условных рефлексов. На сигнальные раздражители мы можем осуществлять меры воздействия на окружающую среду.
02.05.09
Внутренняя энергия
Внутренняя энергия – сумма потенциальной энергии взаимодействия частиц системы и кинетической энергии беспорядочного теплового движения частиц. Кинетическая энергия беспорядочного теплового движения пропорциональна температуре, а потенциальная энергия зависит от взаимодействия частиц, от расстояния между ними, то есть от объема. Поэтому в классической термодинамике внутреннюю энергию может выразить как произведение температуры на величину объема. Свободная энергия – часть внутренней энергии тела, которая способна совершать работу. Связанная энергия – та часть внутренней энергии, которая не может быть превращена в одну из форм полезной работы. Закрытые термодинамические системы стремятся перейти в состояние термодинамического равновесия, которое характеризуется прекращением в системе всех макроскопических процессов, а также в таком состоянии система может оставаться сколь долго угодно без внешних воздействий. Термодинамические процессы
В термодинамических системах происходят термодинамические процессы – переход системы из одного состояния в другое, причем различают термодинамические процессы: 1. квазистатические - обратимые; 2. нестатические - необратимые.
Обратимые процессы допускают возвращение термодинамической системы в первоначальное состояние без изменений в окружающей среде, такие процессы встречаются только в изолированных термодинамических системах (термос). Однако это идеализированная система, ибо в природе не встречается. Необратимые характерны для закрытых и открытых систем, все процессы протекают с конечной скоростью, они необратимы. Поэтому какой-либо процессы не протекал бы, он всегда имеет окончание. Термодинамические процессы, протекающие в системах, подчиняются двум законам (началам) термодинамики Первый закон был установлен в 1848 году немецким врачом Робертом Майером: «Энергия в изолированных системах не может увеличиваться или уменьшаться, а может переходить из одного вида в другой». Возникновение первого закона связано с началом изучения физиологических процессов, аналогичен закону сохранения энергии Ломоносова, однако Михаил Васильевич не опирался столь на физиологию. В путешествии на шхуне Майер отметил, изучая работы Лавуазье, что при жарких температурах происходит меньшее потребление энергии. По прибытии на сушу у членов экипажа началась лихорадка, с лечебными целями делали кровопускания. Майер обнаружил, что во время осуществления кровопускания венозная кровь очень яркая, насыщенная, похожа на артериальную. Сделал заключение, что в условиях жаркого климата кислорода из крови на окислительные процессы тратится меньше. Далее пришел к выводу, что энергия, которая поступает в организм, равна тому количеству энергии, которое выделяется. Изучение чисто физиологических явлений легли в основу фундаментального закона сохранения и превращения энергии. В неизолированных термодинамических системах изменение внутренней энергии равно разности между полученным количеством теплоты Q и работой A, совершаемой самой системой: ∆U=Q-A. Внутренняя энергия является суммой кинетической и потенциальной энергии, изменяется в процессе совершения работы и теплопередачи.
теплопередача конвекция излучение Следствие первого закона термодинамики - правило Гесса 1836 год: «Термодинамический процесс, развивающийся через ряд промежуточных реакций, не зависит от промежуточных стадий, а определяется лишь начальным и конечным состоянием системы». ∆U = U1-U2, где U1 - энергия начального состояния, U2 - энергия конечного состояния, ∆U- изменение внутренней энергии. Отношение работы к количеству тепла, сообщенного системе, есть величина постоянная: A/Q =1 – T2/T1, T2<T1, A/Q=const, 1ккал – 427 кг/м, 1 кал – 4,184 Дж.
В живых организмах совершаются различные виды работы, источником поступления энергии являются химические вещества, мы являемся хемотрофами. Лишь у растений из воды, углекислого газа и минеральных веществ синтезируются органические соединения, которые являются началом жизни, ибо они поглощаются травоядными животными, которых поедают плотоядные, а также и мы. Таким образом, мы получаем солнечную энергию в виде энергии химических связей, которая превращается в энергию макроэргических соединений - «универсальная валюта обменных процессов». При превращении энергии происходит образование тепла. Различают первичную теплоту – результат теплового рассеивания энергии в ходе обмена веществ и в ходе протекающих химических и биохимических реакций. Но химические реакции, которые протекают в организме, дают нам возможность совершения разных форм работы: поддержание осмотичности, свечение, совершение механической работы и другие виды. Какую бы работу мы не совершали конечный итог – тепловая энергия. Та тепловая энергия, в которую переходят различные виды работ – вторичная теплота, пропорциональна активности ткани, причем основным источником вторичной теплоты будут являться мышцы.
Производились следующие исследования термодинамических процессов в биологических системах: 1. Лавуазье и Лаплас при помещении морской свинки в ледяную каломель, сравнивали количество энергии, поступающей с пищей, и количество выделившегося тепла. Обнаружили, что эти показатели одинаковы. Питательные вещества, которые окисляются в организме, дают такое же количество энергии, как и при сгорании тех же веществ в калориметре. 2. Уоттер изучал энергетический баланс в организме, какое количество энергии выделялось при сжигании жиров, белков и углеводов. При изучении сжигания веществ в калориметре выделялось 1859 ккал, разница 20 ккал. Разница обусловлена тем, что в таких исследованиях возможна ошибка, или же часть энергии запасалась на структурных компонентах протоплазмы клеток.
Эти исследования показали, что первый закон термодинамики и его следствие применимы к биологическим объектам, при этом учитывается количество энергии, поглощенной с пищей, и количество выделенной организмом тепловой энергии. В этом энергетическом балансе не рассматриваются промежуточные этапы превращения энергии. Первый закон характеризует лишь количественные изменения и превращения энергии в термодинамических системах, но не показывает вероятности процесса и его направленности. Второй закон термодинамики был установлен Карно и Клаузисом: «Для совершения работы одного лишь наличия энергии недостаточно. Для совершения работы необходимо наличие разности потенциалов энергетических уровней». Таким образом, второй закон показывает направленность изменений, которые происходят в термодинамических системах, ибо самопроизвольно теплота переходит лишь от нагретого тела к более холодному, от вещества с большей концентрацией в сторону меньшей. Для работы необходимо создание и поддержание градиента параметра – отношение разности величин параметра в двух точках к расстоянию между ними (концентрационный, электрохимический градиент, градиент автоматии в проводящей системе). Первый закон термодинамики дает на возможность представления о том, что некоторые явления могли бы произойти, однако этого не происходит, ибо, роняя предмет со стола, он обратно не возвращается, хотя первый закон это допускает. При падении потенциальная энергия покоящегося тела переходит в кинетическую энергию движения. При соударении кинетическая энергия движения переходит в тепловую энергию. По первому закону все происходит в эквивалентных количествах, можем допустить, что тепловая энергия переходит в кинетическую, что обеспечивает подъем, однако этого не происходит, ибо большинство процессов необратимо – пролитая вода не соберется обратно в кувшин, разбитая ваза не восстановится из осколков.
Энтропия
По мере превращения энергии системы теряют разность энергетических уровней и утрачивают способность совершать работу. Энтропия (от греч. превращение) - мера утраты способности системы совершать работу, мера рассеяния энергии: S = Q/T, Q = S*T. Больцман исследовал эти процессы, дал понятие энтропии. S = K*ln W, K-постоянная Больцмана, равна 1,38 * 10-23 Дж/К.
Количество способов комбинации элементов системы, с помощью которых может быть реализовано данное состояние – термодинамическая вероятность W, следует отличать ее от математической вероятности - среднее значение частоты появлений событий при испытании P. Термодинамическая вероятность показывает возможность расположения частиц в системе, которое может реализовать данное состояние. Например, в системе 6 молекул: 6 слева и ни одной справа, далее справа может быть 1 молекула, может быть справа 2 молекулы, а остальные слева, что показывает, в каком состоянии находится термодинамическая система. Число размещений молекул 26 = 64– термодинамическая вероятность. Положение молекул 6 слева, 0 справа - единственное состояние системы, 5 слева и 1 справа – шесть возможностей, 4 слева и 2 справа -15 размещений, 3 слева и 3 справа -20 размещений, далее изменяется все в такой же последовательности. Математическая вероятность этих состояний 1/64 = 0,016. Такое состояние с математической точки зрения маловероятно, самой большой вероятностью будет обладать распределение 3 и 3. Если в какой-то части термодинамической системы сконцентрировано много свободной энергии, такая система – неравновесная, энтропия такой системы буде мала, энергия будет перемещаться из области большей концентрации в область меньшей, то есть движение энергии будет упорядочено. Вероятность существования такой системы очень мала, ибо система стремится к беспорядку, стремится стать равновесной. То есть система стремится к тому, чтобы в двух ее частях энергия распределилась равномерно. Вероятность существования такой системы будет значительно больше, а энтропия равновесной системы будет велика, ибо перемещение частиц в такой системе подчиняется лишь тепловому Броуновскому движению. При этом нет определенного направления движения частиц, исходя из этого, система будет беспорядочной. Второй закон показывает ограниченность превращения энергии в работу, ибо не вся внутренняя энергия может быть превращена в работу, КПД<1, A/Q=1-T1/T2, T1>T2. Если возьмем температуру тела внутри человека 310 К, а снаружи 303 К, возможность совершения работы за счет тепловой энергий 2 %, но мы используем для совершения работы химическую энергию, что позволяется увеличить КПД = A/∆F ≤ 1. Соотношение биологического процесса и КПД в %: гликолиз 36, окислительное фосфорилирование 55, фотосинтез 75, сокращение мышц 40, свечение бактерий до 96. Живые организмы, совершая работу, не приходят в состояние термодинамического равновесия. Закрытые системы подчиняются закону увеличения энтропии, а живые организмы – открытые термодинамические системы, стремятся к минимуму энтропии. Совершая непрерывную работу, они постоянно расходуют энергию, но при этом живой организм удерживает разницу энергетических уровней. Наша деятельность направлена на поддержание градиента, что возможно благодаря поступлению в нашу систему веществ из окружающей среды, которые имеют большой запас свободной энергии. Поэтому понятие энтропии для живых организмов было заменено понятием потока энтропии. Поступление питательных веществ в организм рассматривается как поток отрицательной энтропии, ибо в ходе обмена веществ происходит уменьшение свободной энергии и запасании энергии в живом организме (продукты, которые мы получаем, являются строго упорядоченными, а то, что выделяем – продукты беспорядочные). Энергия, которая уходит в ходе совершения работы, представляет собой поток положительной энтропии. Поток отрицательной энтропии возникает в процессе ассимиляции, а положительной - в процесс диссимиляции, что позволяет нам поддерживать стационарное равновесие.
Экспоненциальное приближение отображает кривая А – оптимальное состояние, здесь происходит медленное возвращение к стационарному состоянию, но реакции в организме могут быть разнообразными. Кривая Б показывает возможность с избыточным отклонением, а кривая В переход к сложному старту, когда энергетические ресурсы уменьшены.
Второй закон затрагивает и состояние информации в живых объектах, ибо согласно второму закону в системе есть стремление переходить к беспорядку – универсальный закон. В организме происходят сложные реакции синтеза и восстановление структур, которые погибают. Информация на восстановление заложена в азотистых основаниях, что позволяет заменить структуры, заменить отмершие клетки и продолжить жизнь. Если способность утратится, то организм погибнет, ибо неумолимо будет действовать второй закон термодинамики, а именно будет осуществляться переход к беспорядку. Законы термодинамики имеют приложение к биологическим объектам.
07.05.09 Фотобиологические процессы
При поглощении лучистой энергии биологическими объектами происходят фотобиологические процессы, которые делятся на: 1. процессы фотосинтеза – синтез биологических важных соединений за счет поглощения солнечной энергии (синтез углеводов в зеленых растениях, некоторых простейших и водорослях, образуется хлорофилл). Процессы фотосинтеза удалось наблюдать в водных растворах смесей, которые содержали метан, аммиак, углекислый газ, при облучении смеси удавалось получать жирные кислоты, аминокислоты, пуриновые и пиримидиновые азотистые основания. Эксперименты легли в основу возникновения жизни внутри клеток; 2. зрение животных, фототаксис, фототропизм и фотопериодизм растений. В ходе явлений организм получает информацию об изменениях в окружающей среде, которые возникают при действии света; 3. деструктивные процессы в биологических структурах, которые возникают при действии коротковолнового УФ излучения.
Свет может оказывать стимулирующее действие на развитие животных. При действии видимого света наблюдается реакция фотореактивации – снятие поражающего действия УФ излучения при последующем действии видимого света. Сверхслабое свечение возникает при биохимических реакциях. В основе всех фотобиологических процессов лежат фотохим реакции: 1. фотоионизация – под действием света происходит выбивание электронов за пределы молекулы, образуются ионы или свободные радикалы; 2. фотовосстановление или фотоокисление - перенос электронов с одной молекулы на другую при действии света; 3. фотодиссоциация – процесс распада молекул при действии света; 4. фотоизомеризация – изменение пространственной структуры, конфигурации молекулы; 5. фотодимеризация – образование химических связей между мономерами, образование полимеров.
Во всех реакциях молекулы теряют или приобретают электроны, подвергаются деструкции. Процессы протекают в две стадии: 1. световая – чисто физический процесс поглощение молекулой кванта лучистой энергии, молекула при этом переходит в возбужденное состояние. Электроны, которые участвуют в поглощении квантов, переходят с основного на более высокий энергетический уровне. Величина энергии возрастает на величину поглощенного кванта. Состояние длится до 10-12-10-8. Энергия, полученная молекулой, может перейти в тепло или выделиться в форме кванта люминесценции. Возбужденные молекулы могут вступать в фотохимические реакции с другими молекулы с образованием радикалов, ионов или ион-радикалов – первичные окислители и первичные восстановители; 2. темновая – образовавшиеся первичные окислители и восстановители вступают в сопряжение с биохимическими реакциями в организме и изменяются, что приводит к совершению физиологических процессов (выделение кислорода при фотосинтезе, движение листьев растений на солнце, реакции животных на освещение, гибель животных при сильном облучении).
В ходе фотохимических реакций возможны следующие превращения энергии: 1. может высвечиваться в форме люминесценции; 2. может передаваться в тепло; 3. может передаваться другой молекуле (миграция энергии); 4. молекула может переходить в триплетное состояние.
Поглощательная способность биологических систем определяется общим количеством поглощенной энергии или числом квантов, поглощаемых системой в единицу времени. Показатель определяется на основе оптической плотности объекта. Второй фактор – величина поглощенного кванта, который определяет энергетику самой фотохимической реакции. При пропускании световых квантов через систему, которая содержит какие-то вещества, происходит ослабление светового потока, что связано с тем, что часть квантов захватывается и поглощается молекулами вещества. Изменение интенсивности светового потока подчиняется закону Ламберта-Бера: «Интенсивность светового потока, проходящего через вещество, экспоненциально уменьшается в зависимости от длины оптического пути и концентрации вещества». –dl=k*I*C*dl, I=I0*e-kcl, lg I0/I=D – оптическая плотность, I0-интенсивность падающего света, I-интенсивность выходящего света.
Вещество неодинаково поглощает свет различной длины волны. Кривая зависимости оптической плотности вещества от длины волны поглощаемого света будет представлять собой спектр поглощаемого света. Построение таких кривых при спектральном анализе позволяет выявить максимум поглощения определенных длин волн, которые характерны для определенных веществ. Спектры поглощения белка имеют максимум поглощения в области длины волны 280 нм, нуклеиновые кислоты 260 нм, родопсин 500 нм, хлорофилл 430 и 680 нм – два максимума поглощения. Изучение спектров поглощения позволяет определить вещество, которое ответственно за поглощение света, определить длину волны света, которая преимущественно поглощается, и рассчитать энергию поглощаемых квантов, определить положение электронных и колебательных энергетических уровней, время перехода из одного состояния в другое. Спектральный анализ позволяет определить концентрацию вещества в исследуемом объекте. Спектры поглощения могут быть получены при адсорбционной спектрофотометрии. Спектрофотометр имеет источник света, монохроматор, который позволяет выделить лучи разной длины волны из общего светового потока, кювету, куда помещается исследуемое вещество. Луч света, проходящий через вещество, попадает на фотоэлектронный умножитель, затем на регистрирующее устройство, которое прокалибровано в единицах оптической плотности. Таким образом, направляя разные длины волн на вещество, получим кривые спектрального анализа с определенными максимумами поглощения. При невозбужденном состоянии электроны в молекулах находятся на нижнем основном энергетическом уровне, электронные оболочки находятся в синглетном состоянии, при котором спиновый момент равен 0. При поглощении кванта лучистой энергии происходят переходы электронов в молекулах на более высокие удаленные возбужденные уровни. Первый переход происходит при поглощении кванта 5,7 мВ, осуществляется переход на второй уровень, молекула переходит в возбужденное состояние, но способна воспринимать очередной квант, в зависимости от которого электроны будут уходить либо на более высокий, либо на более низкий уровень. Таким образом, молекулы находятся в состоянии возбуждения, электронные переходы в молекулах затрагивают вращательные, колебательные и электронные уровни. При таких переходах в молекулах может наблюдаться процесс свечения.
Процессы свечения молекул
Люминесценция – процесс свечения молекул, сопровождающий переход электронов с возбужденных уровней на основной: 1. флюоресценция – свечение молекулы в момент облучения; 2. фосфоресценция – свечение после прекращения облучения.
При переходе электронов с возбужденных уровней на основной происходит испускание кванта люминесценции. Закон Стокса устанавливает, что «Длина волны света испускаемого при люминесценции всегда больше длины волны света, который ее вызвал». Это связано с тем, что электроны с возбужденных уровней не сразу попадают на основной. Изначально электроны переходят с более высоких уровней на менее, но которые являются также возбужденными. Переходы сопровождаются потерей части энергии, которая переходит в тепло. Электроны должны перейти на самый низкий возбужденный уровень (S0*-уровень), с которого могут возвращаться на основной (S0-уровень). Квант люминесценции выделяется при этом переходе, при этом часть энергии растрачена, поэтому длина волны кванта люминесценции будет больше. Возбуждение молекулы, которое происходит при флюоресценции, длится 10-9-10-8 c, поэтому ее можем наблюдать в момент освещения, ибо период возбуждения имеет короток. Процесс фосфоресценции связан с переходом электронов с триплетного уровня (Т-уровень) на основной (S0-уровень), что длится от 10-3 с до нескольких секунд. Триплетный уровень располагается ниже минимального возбужденного S0*. Электроны при поглощении энергии не попадают на триплетный уровень, а могут попадать на него при переходе с нижнего возбужденного. При этом электрон меняет свой спин на противоположный. На уровне появляются не спаренные электроны, переход с триплетного уровня на основной сопровождается высвечиванием кванта, при этом квант будет иметь еще большую длину волну, чем при флюоресценции. Процессы люминесценции оцениваются квантовым выходом - отношение количества квантов люминесценции к числу поглощенных квантов, φ = n / N. Закон Вавилова устанавливает: «Квантовый выход люминесценции не зависит от длины волны света, вызвавшего люминесценцию». Изучение спектров люминесценции позволяет судить о величине квантов энергии, запасаемых в молекуле, рассчитать положение энергетических уровней, определить время возбужденного состояния по скорости появления и ухода люминесценции, исследовать состояние вещества. При химических реакциях может высвобождаться энергия, достаточная для высвечивания кванта люминесценции – хемилюминесценция – свечение молекул, сопряженное с химическими реакциями: 1. биохемилюминесценция; 2. фотохемилюминесценция - наблюдается при обратных фотохимических реакциях.
Светлячки, грибы, морские организмы обладают биохемилюминесценцией, которая связана с ферментативными процессами. Связано свечение с веществами люцеферинами, которые приобретают свойство свечения при действии фермента люциферазы. Свечение происходит, когда энергия АТФ в присутствии кислорода и ионов магния переходит с люциферазы на люциферин. При исследовании процессов в биологических объектах было обнаружено слабое свечение. Гурвич 1924 год обнаружил свечение в корешках лука, что усиливало процессы митоза в других клетках (митогенетические лучи). Тарусов выявил процессы свечения при неферментативном окислении липидов. Обнаружено свечение митохондрий при нарушении их нормальной функции. Изучение биолюминесценции позволяет исследовать состояние молекул на молекулярном и субмолекулярном уровне.
Миграция энергии |



 Наш организм стремится к созданию постоянной величины энтропии, но эмоциональная нагрузка и заболевания приводят к нарушению потоков энтропии, что выводит нас из состояния равновесия. Организм работает на то, чтобы при выходе из стационарного состояния вернутся к нормальному состоянию, при этом переходы могут быть различными.
Наш организм стремится к созданию постоянной величины энтропии, но эмоциональная нагрузка и заболевания приводят к нарушению потоков энтропии, что выводит нас из состояния равновесия. Организм работает на то, чтобы при выходе из стационарного состояния вернутся к нормальному состоянию, при этом переходы могут быть различными.


