
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Дослід 6.2.4. Утворення аміакату нікелюСодержание книги
Поиск на нашем сайте До 3 крапель розчину солі нікелю додати по краплях розчин амоніаку до розчинення осаду основної солі, що утворився. Визначити колір отриманого розчину. Записати рівняння реакцій (координаційне число Ni2+ дорівнює 6.) Дослід 6.2.5. Стійкість іона диамінсрібла (I) Внести у дві пробірки по 2-3 краплі розчину аргентум нітрату і додати в одну пробірку кілька крапель розчину лугу, в іншу – декілька крапель розчину калій йодиду. Визначити колір осаду, що утворюється. Записати рівняння реакцій. У дві інших пробірки внести по 2-3 краплі розчину аргентум нітрату і потім долити в обидві пробірки концентрований розчин амоніаку до розчинення осадів. До отриманого розчину комплексної сполуки срібла додати: в одну пробірку декілька крапель розведеного розчину лугу, в іншу – декілька крапель розчину калій йодиду. Пояснити відсут-ність осаду в першій пробірці і наявність жовтого осаду в другій. Скласти рівняння реакцій. 6.3. Контрольні запитання
ЛАБОРАТОРНА РОБОТА № 7 ХІМІЯ S-ЕЛЕМЕНТІВ Теоретична частина Гідроген належить до найпоширеніших елементів у природі. У вільному стані він зустрічається в незначних кількостях, головним чином, у верхніх шарах атмосфери, тому що густина вільного водню у 14,5 разів менша, ніж густина повітря. Вільний водень виділяється при виверженні вулканів, з бурових свердловин та при розкладанні бактеріями органічних речовин в умовах нестачі повітря. Лабораторні способи одержання водню полягають у витісненні його із води або розведених кислот, що не виявляють окисних властивостей. 1. Дією розведених кислот на метали: Fe + H2SO4 → FeSO4 + H2↑ Zn + 2HCl → ZnCl2 + H2↑ 2Al + 3H2SO4 → Al2(SO4)3 + 3H2↑ З кислот можуть витісняти водень лише ті метали, які в ряду активності займають місця ліворуч від Гідрогену. Причому чим лівіше знаходиться метал в ряду, тим він більш активний. Так лужні і лужноземельні метали дуже активні, при їх взаємодії з кислотами спостерігається вибух. Тому при одержанні водню в лабораторних умовах користуються металами середньої активності – цинком або залізом. 2. Взаємодією лужних і лужноземельних металів з водою: 2K + 2H2O → 2KOH + H2↑ Ca + 2H2O → Ca(OH)2 + H2↑ 3. У промисловості для добування водню використовують природні та нафтозаводські гази, складовою частиною яких є метан. Природний газ змішують з киснем у кількості, яка недостатня для повного окиснення метану, і проводять реакцію при 850 - 900°С у присутності каталізатора (Ni + Al2O3): 2CH4 + O2 → 2CO↑ + 4H2↑ + 71,4 кДж.
Молекулярний Гідроген може виявляти відновні властивості по відношенню до окисників неметалічного походження, а також по відношенню до окиснених форм металів. При звиайних умовах Гідроген малоактивний завдяки стійкості молекул Н2 і безпосередньо взаємодіє лише з фтором: H2 + F2 ® 2HF, а під дією світла відбувається ланцюгова реакція з хлором: H2 + Cl2 ® 2HCl. У сіміші з киснем водень горить голубим полум’ям з виділенням великої кількості тепла: 2H2 + O2 → 2H2O + 575.4 кДж. Відновна здатність водню використовується у металургії для одержання деяких високочистих металів з їх оксидів: Ag2O + H2 → 2Ag + H2O; CuO + H2 → Cu + H2O; MoO3 + 3H2 → Mo + 3H2O. У реакціях з активними металами (лужні, лужно-земельні) водень утворює гідриди. У цих реакціях атом водню приєднує електрон, перетворюючись у негативно заряджений іон з оболонкою інертного газу гелію: 2Na + H2 → 2NaH Гідриди – солеподібні, тверді, кристалічні речовини з іонним зв’язком. Вони виявляють дуже сильні відновні властивості і легко розкладаються водою, кислотами та взаємодіють з іншими різними окисниками: CaH2 + 2H2O → Ca(OH)2 + 2H2 До найважливіших оксидів Гідрогену відноситься вода. Організми тварин і рослин містять від 50 до 90 % (макс.) води. Вода потрібна рослинам протягом усього їх життя. Починаючи з проростання насіння вода обумовлює важливі біохімічні процеси. Встановлено, що хлібні злаки витрачають до 300 кг води на 1 кг сухої рослинної маси. Для отримання високого урожаю необхідно в достатку забезпечити культурну рослину вологою. Частково це досягнення агротехнічними прийомами; після прибирання хлібів лущать стерню, прагнучи “закрити” вологу, тобто припинити сильний випар води з грунту. У областях, що відрізняються недостатнім зволоженням, багато уваги приділяється зрошуванню, що дозволяє істотно підвищити урожай сільськогосподарських культур. Взагалі гідромеліора-тивні роботи завжди пов’язані з підвищенням врожайності сільськогоспо-дарських культур і освоєнням нових земель. Окрім води Гідроген утворює з Оксигеном ще одну сполуку – гідроген пероксид Н2О2. Він застосовується головним чином завдяки його сильній окисній дії. У агрономічних і грунтових лабораторіях гідроген пероксид використовують для озолення (спалювання) зразків грунту або рослинного матеріалу. Натрій та Калій є елементами ІА групи періодичної системи і відносяться до лужних металів. Атоми цих елементів мають на зовнішньому рівні по одному s-електрону, які вони легко віддають під час хімічних реакцій, перетворююючись на позитивно заряджені іони (ступінь окиснення +1). Зі збільшенням радіуса атома (Na, K) виникає збільшення відновних і металічних властивостей, зростають електропровідність, густина та хімічна активність. Металічний Натрій і Kалій одержують електролітичним відновленням розплавлених солей або відповідних гідроксидів. При цьому на катоді проходить реакція відновлення: Me+ + е- → Meо З елементами IIА і IIIА груп та між собою лужні метали утворююють сплави, з галогенами – лише найпростіші бінарні сполуки, з вуглецем – ацетиленіди, з сіркою – сульфіди і полісульфіди, з фосфором – фосфіди, кремнієм – силіциди, з водою – гідроксиди: 2Na + Cl2 → 2NaCl 2К + S → К2S 2Na + O2 → Na2O2 2Na + 2C → 2Na2C2 2K + 2H2O → 2KOH + H2↑ В атмосфері кисню ці метали згоряють, а при нагріванні спалахують утворюючи оксиди та пероксид чи надпероксид: 2Na + O2 → Na2O2 – натрій пероксид K + O2 → KO2 – калій надпероксид Пероксиди і надпероксиди підлягають гідролізу: Na2O2 + 2H2O → 2NaOH + H2O2 2KO2 + 2H2O → 2KOH + H2O2 + O2 Оксиди лужних металів також реагують з водою з утворенням гідроксидів: Na2O + H2O → 2NaOH NaOH і KOH – безбарвні кристалічні речовини, добре розчиняються у воді з виділенням великої кількості тепла. Розчини цих гідроксидів називають лугами. При слабкому нагріванні калію та натрію в атмосфері водню утворю-ються гідриди. Наявність в гідридах Гідрогену зі ступенем окиснення -1 надає їм сильні відновні властивості, які виявляються в реакціях з водою, кислотами та іншими окисниками: NaH + H2O → NaOH + H2 КН + HCl → KCl + H2 NaH + Cl2 → NaCl + HCl 2KH + CO2 → 2KOH + C При взаємодії твердих бінарних сполук з оксидами, сульфідами, гало-генідами утворюються солі: Na2O + CO2 → Na2CO3 K2O + SiO2 → K2SiO3 У сільському господарстві використовують як добрива натрій нітрат (чилійська селітра) та калій хлорид. Калій сульфат – калійне добриво, що використовується для вирощування культур, які не витримують надлишку хлоридів. Натрій хлорид підсилює ріст і розвиток буряків, сприяє швидкостиглості рослин. Є відомості про те, що натрій активізує переміщення калію до молодих частин рослин і підвищує ефективність калію, азоту та інших поживних речовин. Калій потрібен рослинам для постачання клітин водою, забезпечення проникності клітинних мембран. Якщо його достатньо – рослина краще утримує воду, стійка до засухи і заморозків. Магній та Кальцій, що утворюють ІІА-групу періодичної системи, також відносяться до s-елементів. Атоми цих елементів на зовнішньому рівні мають по два електрони в стані s2. Всі елементи ІІА групи зустрічаються у природі лише у вигляді сполук. Кальцій та Магній є найважливішими біогенними елементами. Вони також входять до складу важливих первинних і грунто-утворюючих мінералів і є необхідними елементами грунтового харчування рослин. Кальцій отримують електролізом кальцій хлориду або алюмотермічним методом: СаСl2 → Са + Сl2 2Al + 6CaO → Ca3(AlO3)2 + 3Ca Магній одержують відновленням вуглецем при температурі 2000°С: MgO + C → CO + Mg Кальцій та Магній мають сильні відновні властивості, поступаючись лише лужним металам. Внаслідок хімічної активності переважна більшість бінарних сполук цих металів може бути одержана прямим синтезом із простих речовин. При високих температурах магній і кальцій реагують з галогенами, азотом, сіркою, фосфором, вуглецем та кремнієм з утворенням відповідних галогені дів, нітридів, сульфідів, карбідів та силіцидів: 3Ca + Br2 → CaBr2 3Mg + N2 → Mg3N2 Ca + S → CaS 3Mg + 2P → Mg3P2 Ca + 2C → CaC2 2Mg + Si → Mg2Si Магній і кальцій при нагріванні окиснюються воднем з утворенням гідридів – кристалічних речовин з іонною структурою: Ca + H2 → CaH2 Гідриди легко реагують з водою з утворенням гідроксидів: CaH2 + 2H2O → Ca(OH)2 + 2H2↑ При підвищенні температури кальцій і магній згоряють у повітрі з утворенням оксидів: 2Ca + O2 → 2CaO Оксиди кальцію та магнію у промислових масштабах одержують прожарюванням карбонатів (вапна чи магнезиту): СаСО3 → СаО + СО2 Вони взаємодіють з водою з утворенням відповідних гідроксидів. СаО + Н2О → Са(ОН)2 Усі оксиди і гідроксиди лужноземельних металів мають основні властивості. Деякі хімічні властивості сполук Кальцію і Магнію наведені у наступних реакціях: MgS + H2O → Mg(OH)2 + H2S Ca3N2 + 6H2O → 3Ca(OH)2 + 2NH3 Mg3P2 + 6H2O → 3Mg(OH)2 + 2PH3 CaO + SiO2 CaO + 3C Ca(OH)2 Ca(OH)2 + CO2 Ca(OH)2 + HCl На відміну від солей лужних металів солі кальцію та магнію малорозчинні. У біологічному кругообігу речовин Кальцію належить одна із головних функцій. Він приймає участь у процесах грунтоутворення, покращує структуру грунтів, впливає на реакцію середовища і, як наслідок, рухомість інших біологічно необхідних елементів. Кальцій сприяє фіксації атмосферногоь азоту, мінералізації органічних сполук і вивільненню з них різних поживних речовин. Цей елемент приймає участь у синтезі білкових речовин, сприяє утворенню хлорофілу, впливає на переміщення асимілятів у рослинах. При відсутності кальцію у грунті погано розвивається коренева структура рослин. Іони Магнію суттєво впливають на окисно-відновні процеси у рослинах. При магнієвій нестачі у рослин підвищується окисний потенціал, підсилюються окисні процеси, що призводить до руйнування хлорофілу. Магній посилює рухомість фосфатів у грунті і надходження їх до рослин, він сприяє відновним процесам у рослинах і позитивно впливає на біосинтез відновлених сполук. Солі CaCO3 і CaCO3 × MgCO3 – основні речовини для хімічної меліорації грунтів, завдання якої полягає у ліквідації надлишкової кислотності грунтвого розчину (вапнування) або усунення його надлишкової лужності (гіпсування). Експериментальна частина
|
||||||||||||||||
|
Последнее изменение этой страницы: 2016-04-19; просмотров: 215; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.216 (0.008 с.) |

 CaSiO3
CaSiO3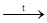 CaC2 + CO
CaC2 + CO


