
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Химические свойства галогеновСодержание книги
Поиск на нашем сайте Галогены обладают большим сродством к электрону и являются сильными окислителями. Окислительные свойства их возрастают от йода к фтору. Они активно взаимодействуют почти со всеми элементами периодической системы. Фтор реагирует практически со всеми металлами и неметаллами, кроме He, Ne, Ar. Реакции протекают очень бурно, часто сопровождаются взрывом, образуются соединения, в которых элементы, как правило, находятся в высшей степени окисления, например: 2Na + F2 = 2NaF (на холоде); 2Au + 3F2 = 2AuF3; 2P + 5F2 = 2PF5; 3F2 + S = SF6; 3F2 + Xe = XeF6. Фтор при обычной температуре не взаимодействует с некоторыми металлами (Fe, Cu, Ni, A1, Zn), на поверхности этих металлов образуется защитная фторидная пленка. В виде порошка железо горит в хлоре без предварительного нагревания, компактное железо реагирует при нагревании: 2Fe + 3Cl2 Однако в отсутствие воды на поверхности металлов может образоваться плотная солевая пленка, предохраняющая металл от разрушения, поэтому сжиженный сухой хлор перевозят в стальных баллонах. С помощью сухого хлора извлекают олово из отходов белой жести, используемой главным образом для приготовления консервных банок. Сухой хлор не реагирует с железом, но взаимодействует с оловом, образуя жидкий SnС14. С неметаллами: 2P + 3Cl2(недост) 2P + 5Cl2(изб) 2Cl2 + S = SCl4. Активность брома и йода значительно ниже, но и они со многими металлами и неметаллами могут реагировать при обычных условиях: 2А1 + 3I2 = 2А1I3 (Н2О – катализатор); 2P + 3Br2 = 2PBr3; 2P + 3I2 Галогены вступают в реакцию с водородом, образуя соединения НГ: Н2 + Г2 = 2НГ. Реакция взаимодействия фтора с водородом сопровождается взрывом, при этом выделяется большое количество энергии. Хлор при обычных условиях очень медленно взаимодействует с водородом, но на прямом солнечном свету или при нагревании реакция идет также со взрывом. Реакция водорода и хлора протекает по цепному механизму, поэтому для нее необходимо инициирование (нагревание или освещение): Н2 + Сl2 Взаимодействие брома и йода с водородом происходит лишь при нагревании. Иод с водородом реагирует незначительно, так как образующийся в условиях синтеза иодоводород легко разлагается, и равновесие сильно смещено в сторону исходных веществ. Поэтому только НCl в промышленности получают из простых веществ. Азот и кислород непосредственно с галогенами не взаимодействуют. Лишь фтор взаимодействует с кислородом в тлеющем разряде, образуя при низких температуpax фториды кислорода: O2F2, O3F2 и другие. Взаимодействие с водой. Фтор энергично разлагает воду, продукты реакции зависят от температуры: (H2O) + F2 = 2HF + 0,5O2 (t > 90ºС, с водяным паром – с взрывом); {2Н2О} + 4F2 = 4НF + 2ОF2↑ (при t = 0‒90ºС). Фтор активно взаимодействует со спиртом, ацетоном, бензолом. Поэтому эти вещества не могут быть использованы в качестве растворителей фтора. Хлор, бром и иод растворяются в воде, причем их растворимость в воде при 20ºС характеризуется следующими значениями, моль/л: хлор – 0,103, бром – 0,225, то есть растворимость брома несколько выше растворимости хлора. Растворимость иода в воде значительно меньше – 0,0013 моль/л. Растворы хлора и брома в воде носят название хлорной и бромной воды. Эти растворы обладают всеми свойствами хлора и брома соответственно. Их окислительные свойства превосходят окислительные свойства сухих хлора и брома. Это объясняется тем, что в водных растворах галогенов (за исключением фтора) происходят реакции диспропорционирования, например, для хлора при стандартных условиях: Cl2 + Н2О ⇄ НClО + НCl. При переходе от хлора к иоду равновесие все больше смещается в сторону исходных веществ, о чем свидетельствуют значения констант равновесий данных реакций:
Как видно из приведенных значений констант, рассматриваемые равновесия существенно смещены влево и, наряду с продуктами взаимодействия галогенов с водой, в растворах галогенов присутствуют преимущественно молекулярные формы галогенов. Бактерицидное действие водных растворов хлора связано как с образованием атомарного кислорода, образующегося при разложении НClО, так и с хлорирующим действием хлорноватистой кислоты. Образующаяся в хлорированной воде соляная кислота безвредна, поэтому вода пригодна для употребления. Растворимость I2 в воде можно повысить, если добавить к ней KI. В результате образуется красно-бурый раствор хорошо растворимых (но нестойких) полииодидов калия (KI3 и др.): n I2 + KI = KI2 n +1 (n = 1÷7). Бром и йод лучше растворяются в органических растворителях. Это свойство брома и йода используется в качественном анализе. Взаимодействие со щелочами. При взаимодействии фтора со щелочами продукты реакции зависят от концентрации щелочи: 2F2 + 2NaOH(разб) = 2NaF + OF2 + H2O; 2F2 + 4NaOH(конц) = 4NaF + O2 + 2H2O. Продукты взаимодействия хлора со щелочами зависят от температуры: Сl2 + 2KОН = KСlО + KСl + Н2О; 3Сl2 + 6KОН Раствор, полученный при пропускании хлора через раствор гидроксида натрия, называют «жавелевой водой». Он обладает окислительными свойствами и применяется для отбеливания тканей, бумаги и т. д. Отбеливающее действие «жавелевой воды» связано с поглощением ею углекислого газа из воздуха, который переводит гипохлорит-ионы в молекулы слабой хлорноватистой кислоты: NaС1О + СО2 + H2O ⇄ NaНСО3 + НС1О; С1О– + СО2 + H2O ⇄ НСО Молекулы хлорноватистой кислоты неустойчивы и легко отщепляют кислород, который отбеливает материал, окисляя окрашенные примеси. При взаимодействии хлора с гашеной известью Ca(OH)2 образуется хлорная (белильная) известь CaOCl2: C12 + Ca(OH)2 = CaOCl2 + H2O. Хлорную известь можно рассматривать как смесь СаС12 и Са(С1О)2 или как смешанную соль соляной и хлорноватистой кислот:
При взаимодействии щелочи с I2 уже при обычных условиях образуется NaIO3: 6I2 + 12NaOH = 10NaI + 2NaIO3 + 6H2O. Взаимодействие с сероводородом. Галогены способны отнимать водород от других веществ: H2S + Br2 = S + 2HBr. Реакция замещения водорода в предельных углеводородах: CH4 + Cl2 Реакция присоединения к непредельным углеводородам: C2H4 + Cl2 = C2H4Cl2. В ряду Cl2 – Br2 – I2 – неметаллические свойства ослабевают. У I2 появляются приметы металлических свойств. I2 реагирует с концентрированной HNO3, в неводном растворе образует катион I+: I2 + 10HNO3(конц) = 2HIO3 + 10NO2 + 4H2O; I2 + AgNO3 Для иода характерна особая реакция – он соединяется с крахмалом с образованием синего продукта: (С6Н10 O5) n + I2 ⇄ (С6Н10 O5) n ·I2 белый синий При нагревании равновесие смещается влево, и синяя окраска исчезает. Крахмал применяют как индикатор для обнаружения иода, присутствующего в малых концентрациях. Особые свойства фтора. Из всех галогенов у фтора наименьший радиус. Это самый электроотрицательный элемент, во всех соединениях имеет степень окисления –1. Исключительная химическая активность фтора обусловлена, с одной стороны, большой прочностью образуемых им связей: так, например, энергия связи H‑F равна 566 кДж/моль, с другой стороны ‑ низкой энергией связи в молекуле F2 (159 кДж/моль). Большая энергия связей Э–F является следствием значительной электроотрицательности фтора и малого размера его атома. Низкое значение энергии связи в молекуле F2, объясняется сильным отталкиванием электронных пар, находящихся на р -орбиталях, обусловленным малой длиной связи F–F. Благодаря малой энергии связи молекулы F2 легко диссоциируют на атомы, и энергия активации реакций с участием фтора обычно невелика, поэтому реакции протекают с большой скоростью. Фтор в реакциях проявляет только окислительные свойства. В атмосфере фтора горят H2O, песок (SiO2): SiO2 + 2F2 = Si+4F4 + O2. Эта реакция происходит вследствие того, что тетрафторид кремния ‒ более прочное соединение, чем оксид. Галогеноводороды Получение галогеноводородов. Поскольку взаимодействие простых веществ H2 + F2 = 2HF сопровождается взрывом, фтороводород получают из фторидов: СaF2 + H2SO4 = CaSO4↓ + 2HF ↑; KHF2 В промышленности HCl получают взаимодействием простых веществ, хлорированием углеводородов: Н2 + Сl2 CH4 + Cl2 В лаборатории HCl получают взаимодействием концентрированной серной кислоты на твердые хлориды, гидролизом кислотных галогенидов: NaCl(тверд) + Н2SO4(конц) BCl3 + 3H2O = H3BO3 + 3HCl↑. Поскольку восстановительные свойства бромоводорода и иодоводорода более ярко выражены, HI и HBr нельзя получить реакциями обменного взаимодействия соответствующих галогенидов с концентрированной серной кислотой. NaBr и NaI окисляются H2SO4(конц): 2NaBr + 2H2SO4(конц) = Br2 + SO2 + Na2SO4 + 2H2O; 8NaI + 5H2SO4(конц) = 4I2 + H2S + 4Na2SO4 + 4H2O. HBr и HI получают гидролизом галогенидов фосфора: PBr3 + 3H2O = 3HBr↑ + H3PO3; PI3 + 3H2O = H3PO3 + 3HI. При стандартных условиях галогеноводороды ‒ газообразные вещества с резким запахом, хорошо растворимые в воде. Водные растворы галогеноводородов являются кислотами.Характеристика галогеноводородов:
 В молекулах галогеноводородов образуется ковалентная полярная связь. Общая электронная пара, за счет которой осуществляется связь, сильно смещена в сторону галогена. Особенно сильно происходит поляризация связи в HF, что обусловлено самой высокой электроотрицательностью фтора. Вследствие этого между молекулами HF образуются прочные водородные связи: В молекулах галогеноводородов образуется ковалентная полярная связь. Общая электронная пара, за счет которой осуществляется связь, сильно смещена в сторону галогена. Особенно сильно происходит поляризация связи в HF, что обусловлено самой высокой электроотрицательностью фтора. Вследствие этого между молекулами HF образуются прочные водородные связи:
Наличие водородных связей объясняет аномально высокие температуры плавления и кипения фтороводорода (рис. 1.4). От НСl к HBr и HI температуры плавления и кипения увеличиваются. Жидкий HF образует цепочки, состоящие из молекул HF: (HF)4, (HF)6, (HF)8. Вследствие наличия сильной водородной связи даже в парах молекулы HF ассоциированы. При t = 3500ºС связь H–F разрывается. HF может смешиваться с Н2О в неограниченном количестве, образуя раствор слабой плавиковой кислоты. Между молекулами HF и Н2О также возникают водородные связи. Безводный HF – неэлектролит, а в водном растворе возможны процессы ионизации:
2HF + H2O ⇄ H3O+ + HF HF хранят в сосудах из платины или полиэтилена. В стеклянном сосуде плавиковую кислоту хранить нельзя, т. к. основным компонентом стекла является SiO2, и стекло разрушается: SiO2 + 4HF = SiF4 + 2H2O (реакция травления стекла). В избытке плавиковой кислоты образуется гексафторокремниевая кислота: SiF4 + 2HF = H2[SiF6]. Водные растворы Н Cl, Н Br, Н I – сильные кислоты. Галогенид-ионы проявляют восстановительные свойства, например: 4HCl + O2 ⇄ 2H2O + 2Cl2 (процесс Дикона)
Расчет показывает, что процесс может протекать как в прямом направлении (при t > 903 К), так и обратном (при t < 903 К). Однако при обычных условиях кислород не взаимодействует с HCl с заметной скоростью, для ускорения реакции смесь хлороводорода и кислорода необходимо нагревать и использовать катализатор (хлориды меди(II) и железа(III)). Ранее процесс Дикона использовали для получения хлора. Восстановительные свойства НГ усиливаются. Иодоводород окисляется на воздухе до иодноватой кислоты: 2HI- + 3O2 → 2HI+5O3. Усиление восстановительных свойств НГ прослеживается в реакциях с H2SO4: HCl + H2SO4(конц) ‒ реакция не идет; 2HBr + H2SO4(конц) = Br2 + SO2 + 2H2O; 8HI + H2SO4(конц) = 4I2 + H2S + 4H2O. НCl при взаимодействии с сильными окислителями окисляется до свободного хлора: PbO2 + 4HCl = PbCl2 + Cl2 + 2H2O. Соляная кислота представляет собой бесцветную, дымящую на воздухе жидкость. Она проявляет свойства, характерные для кислот. Химические свойства соляной кислоты:
Для HF также характерны реакции с металлами, с основными оксидами, с основаниями и некоторыми солями, например:
Как и в случае других бинарных соединений, выделяют фториды различной природы: основные – фториды металлов; амфотерные – фториды Al, Zn, Be, Sn; кислотные – соединения фтора с неметаллами:
Галогениды различной природы могут реагировать между собой: 2KF + SiF4 = K2[SiF6]; 3NaF + AlF3 = Na3[AlF6]; 2KF + BeF2 = K2[BeF4]; 2AlF3 + 3SiF4 = Al2[SiF6]3. Основные фториды гидролизуются, если они растворимы в воде: 2NaF + H2O = NaHF2 + NaOH. Кислотные фториды гидролизуются с образованием двух кислот:
2SiF4 + 4HF = 2H2 [ SiF6 ]; 3SiF4 + 3H2O = H2SiO3 + 2H2 [ SiF6 ]. Аналогичная классификация на основные, амфотерные и кислотные существует у хлоридов, бромидов, иодидов:
2KI + HgI2 = K2[HgI4]; KBr + AlBr3 = K[AlBr4]. С увеличением степени ионности повышается термическая устойчивость галогенидов. Гидролиз галогенидов протекает по различным схемам. Подвергающиеся гидролизу основные хлориды, бромиды, иодиды гидролизуют по катиону: MgCl2 + HOH ⇄ MgOHCl + HCl. Кислотные галогениды гидролизуют с образованием двух кислот: PCl5 + 4H2O → H3PO4 + 5HCl; PI3 + 3H2O → H3PO3 + 3HI; BCl3 + 3H2O = H3BO3 + 3HCl. SF6, СCl4, CF4 не подвергаются гидролизу. В соединениях СCl4, CF4 атом углерода координационно и валентно насыщен. Относительная устойчивость SF6 по сравнению с SF4 обусловлена кинетическими факторами. Шесть атомов фтора стерически экранируют атом серы и мешают приближению возможных атакующих групп. Термодинамически же гидролиз SF6 возможен, поскольку стандартное изменение энергии Гиббса этого процесса меньше нуля: SF6(газ) + 3H2O(газ) → SO3(газ) + 6HF(газ); В связи с инертностью и диэлектрическими свойствами SF6 широко используется в качестве газообразного изолятора в высоковольтных аппаратах. Галогениды практически всех металлов хорошо растворимы в воде. Исключение ‒ соли серебра и свинца. Качественная реакция на галогенид-ионы ‒ выпадение осадка белого цвета AgCl в реакциях нитрата серебра с соляной кислотой и хлоридами: KCl + AgNO3 = AgCl ↓ + KNO3. С бромоводородной кислотой и ее солями образуется светло-желтый осадок Ag Br, с иодоводородной кислотой и ее солями ‒ желтый осадок Ag I. Осадки не растворимы в воде и азотной кислоте.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2022-09-03; просмотров: 523; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.119 (0.01 с.) |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 2FeCl3.
2FeCl3. 2НCl.
2НCl. + НС1О.
+ НС1О.
 AgI + INO3.
AgI + INO3.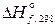 (SiO2) = –910,9 кДж/моль, а
(SiO2) = –910,9 кДж/моль, а  Увеличение
Увеличение Уменьшение
Уменьшение Сильные килоты
Сильные килоты ы кислот
ы кислот
 Возрастание от HCl
Возрастание от HCl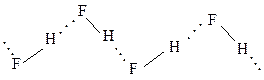
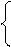 HF + H2O ⇄ H3O+ + F–;
HF + H2O ⇄ H3O+ + F–; F– + HF ⇄ HF
F– + HF ⇄ HF 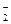 ;
;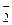 .
.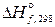 , кДж/моль –91,8 0 –241,82 0
, кДж/моль –91,8 0 –241,82 0 , Дж/(моль × К) 186,8 205,04 188,72 222,9
, Дж/(моль × К) 186,8 205,04 188,72 222,9 = –116,44 кДж;
= –116,44 кДж; 
 =
=  основные
основные кислотные
кислотные SiF4 + 3H2O = H2SiO3 + 4HF;
SiF4 + 3H2O = H2SiO3 + 4HF; = –301,2 кДж.
= –301,2 кДж.


