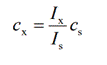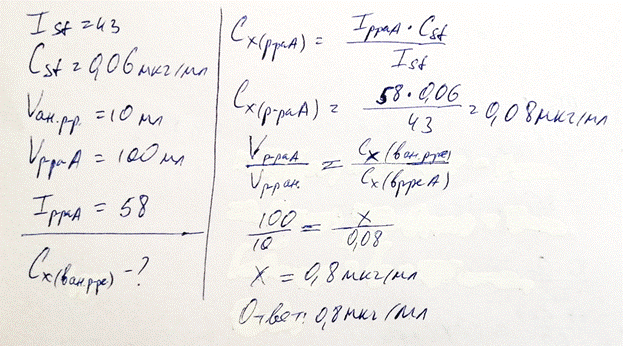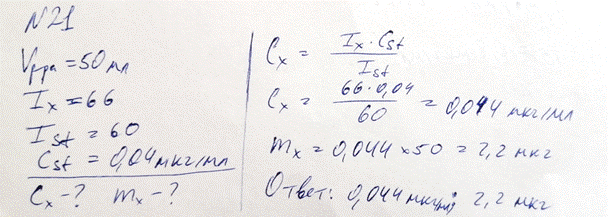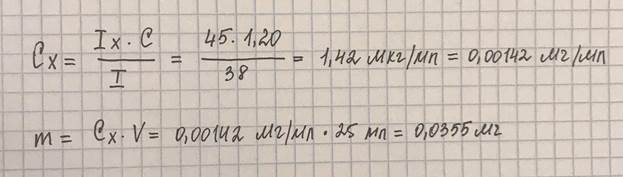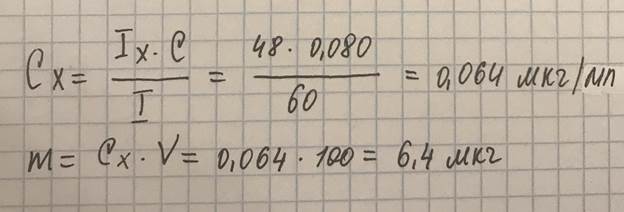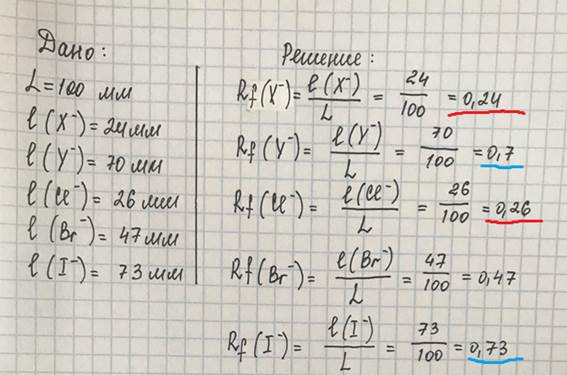Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Концентрацию определяемого вещества в анализируемом растворе при использовании флуориметрии находят методом градуировочного графика или методом одного стандарта.
Метод градуировочного графика. Готовят серию эталонных растворов определяемого вещества с постепенно возрастающей концентрацией с1, с2, с3, …. Измеряют интенсивность флуоресценции Ilm каждого эталонного раствора в одних и тех же условиях. По полученным данным строят градуировочный график в координатах Ilm – c. Затем измеряют интенсивность люминесценции анализируемого раствора в тех же условиях и по градуировочному графику находят концентрацию определяемого вещества в анализируемом растворе. Метод одного стандарта. Готовят стандартный раствор с точно известной концентрацией сs определяемого вещества, близкой к концентрации cx того же определяемого вещества в анализируемом растворе. В одинаковых условиях измеряют интенсивность флуоресценции стандартного Is и анализируемого Ix растворов. Концентрацию cx рассчитывают по формуле
17. Декларируемое содержание тиамина хлорида – витамина B1 – в таблетке лекарственного препарата составляет 0,005 г. Для проведения анализа растерли в порошок две таблетки, растворили порошок в воде, профильтровали и получили 100 мл водного фильтрата. Из фильтрата отобрали 1 мл раствора и разбавили его водой до 100 мл. После проведения экстракции тиамина хлорида бутанолом измерили интенсивность флуоресценции полученного экстракта Ix = 58. Интенсивность флуоресценции стандартного раствора, содержащего 0,001 мг/мл тиамина хлорида, в тех же условиях Ist = 60. Рассчитайте массу в граммах тиамина хлорида в одной таблетке и в процентах по отношению к декларируемому содержанию. Может ли флуориметрия применяться для идентификации веществ? На чем основан качественный анализ?
В основе качественного люминесцентного метода анализа лежит зависимость характера свечения от природы люминесцирующего вещества. В основе количественного люминесцентного метода анализа лежит зависимость интенсивности люминесценции (свечения, вторичной эмиссии) от концентрации анализируемого вещества в растворе. В определенном интервале концентраций флуоресцирующего вещества и при постоянных условиях эксперимента интенсивность люминесценции линейно зависит от концентрации этого вещества в растворе. Спектры флуоресценции специфичны для определяемых веществ. Поэтому флуоресценция может быть применена для их идентификации.
18. Для флуориметрического определения рибофлавина (витамина В2) в кристаллическом препарате методом одного стандарта навеску препарата массой 0,0100 г растворили в воде в мерной колбе вместимостью 500 мл, затем отобрали 1 мл полученного раствора и разбавили его водой до 100 мл. Измерили интенсивность флуоресценции конечного раствора Iх = 48. В тех же условиях измерили интенсивность флуоресценции стандартного раствора Iст = 49 с точно известной концентрацией витамина В2 0,20 мкг/мл. Рассчитайте массовую долю (%) витамина В2 в кристаллическом препарате. Какое условие является обязательным для флуориметрического определения вещества в исследуемом диапазоне концентраций методом одного стандарта?
Метод одного стандарта. Готовят стандартный раствор с точно известной концентрацией сs определяемого вещества, близкой к концентрации cx того же определяемого вещества в анализируемом растворе. В одинаковых условиях измеряют интенсивность флуоресценции стандартного Is и анализируемого Ix растворов. Концентрацию cx рассчитывают по формуле
У стандарта и исследуемого р-ра излучение должно происходит в одной области, интенсивности излучения были как можно ближе Главное: прямо пропорциональная зависимость между концентрацией и интенсивностью излучения
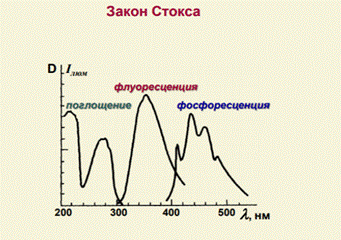
19. Для флуориметрического определения рибофлавина (витамина В2) в кристаллическом препарате методом одного стандарта навеску препарата массой 0,0100 г растворили в воде в мерной колбе вместимостью 250 мл, затем отобрали 1 мл полученного раствора и разбавили его водой до 200 мл. Измерили интенсивность флуоресценции конечного раствора Iх = 59. В тех же условиях измерили интенсивность флуоресценции стандартного раствора Iст = 62 с точно известной концентрацией витамина В2 0,20 мкг/мл. Рассчитайте массовую долю (%) витамина В2 в кристаллическом препарате. Закон Стокса.
Закон Стокса: Спектр флуоресценции лежит в более длинноволновой области по сравнению со спектром поглощения того же вещества
20. Определение магния(II) в растворе провели флуориметрическим методом с применением люмомагнезона ИРЕА. Интенсивность флуоресценции I эталонного раствора, содержащего 0,060 мкг/мл флуоресцирующего комплекса магния с люмомагнезоном ИРЕА, составила 43. Анализируемый раствор объемом 10 мл поместили в мерную колбу вместимостью 100 мл, разбавили водой до метки и получили раствор А. Измерили интенсивность флуоресценции раствора А Iх = 58. Определите концентрацию (мкг/мл) магния в анализируемом растворе.
21. Анализируемый раствор объемом 50 мл содержит соль алюминия. Для флуориметрического определения алюминия проводят люминесцентную реакцию катионов алюминия с салицилаль-о-аминофеноломманганоном. Измерив интенсивность Ix флуоресценции полученного раствора, нашли Ix = 66. Определите содержание катионов алюминия в мкг/мл, а также их массу в анализируемом растворе, если интенсивность излучения стандартного раствора, имеющего концентрацию 0,04 мкг/мл, I(st) = 60. Сущность метода одного стандарта в флуориметрии.
Метод одного стандарта. Готовят стандартный раствор с точно известной концентрацией сs определяемого вещества, близкой к концентрации cx того же определяемого вещества в анализируемом растворе. В одинаковых условиях измеряют интенсивность флуоресценции стандартного Is и анализируемого Ix растворов. Концентрацию cx рассчитывают по формуле
22. Определение алюминия(III) в растворе провели экстракционно-флуориметрическим методом. После проведения люминесцентной реакции и экстракции хлороформом интенсивность флуоресценции полученного экстракта Iх = 45. Рассчитайте концентрацию алюминия(III) в растворе (в мг/мл) и его массу(в мг) в 25 мл, если интенсивность излучения стандартного раствора (Аl)СНCl3, имеющего концентрацию 1,20 мкг/мл, равна 38. Сущность экстракционно-флуориметрического метода.
C – концентрация вещества в стандартном растворе; Iх – интенсивность света, испускаемого испытуемым раствором; I – интенсивность света, испускаемого стандартным раствором.
Экстракционно-флуориметрический метод – это экстракция продукта реакции соответствующим расворителем и флуориметрическое исследование экстракта. Сам флуоресцирующий реагент не экстрагируется неполярными растворителями (бензол, хлороформ). Метод имеет значение для определения примесей в особо чистых веществах. Определение анионов некоторых ацидокомплексов (например, InBr4-, GaCl4-, SbCl6-), которые с катионами флуоресцирующих основных красителей (например, родамин) и подобными реагентами образуют при определенных значениях pH экстрагируемые ионные ассоциаты. 23. Для определения тиамина в анализируемом растворе применили экстракционно- флуориметрический метод. Интенсивность излучения анализируемого раствора тиамина гидрохлорида равна 48. Рассчитайте массу тиамина гидрохлорида (в мкг) в объеме раствора 100 мл, если интенсивность излучения стандартного раствора, имеющего концентрацию 0,080 мкг/мл, равна 60. На чем основан метод флуориметрии? Основные законы.
C – концентрация вещества в стандартном растворе; Iх – интенсивность света, испускаемого испытуемым раствором; I – интенсивность света, испускаемого стандартным раствором. Флуориметрия (или флуоресцентная спектрофотометрия) является методом анализа, основанным на измерении интенсивности флуоресценции, излучаемой испытуемым веществом, относительно флуоресценции, излучаемой стандартным образцом. Флуоресценция – испускание света химическим веществом, находящимся в возбуждённом состоянии, при переходе в основное состояние.
Измеряют интенсивность испускаемого света под углом 90° относительно возбуждающего света после прохождения сквозь фильтр, избирательно пропускающий свет с длиной волны максимальной флуоресценции. Могут быть использованы и другие типы приборов при условии получения аналогичных результатов. Концентрацию (Сх) испытуемого вещества в растворе рассчитывают по формуле:
Закон Стокса-Ломмеля: спектр флуоресценции всегда смещен в сторону более длинных волн по сравнению со спектром поглощения того же вещества. Закон Вавилова: квантовый выход флуоресценции постоянен, если длина волны возбужденного света (в определенных пределах) меньше длины волны флуоресценции: φ=const, если λabs> λlm
24. Интенсивность излучения анализируемого раствора рибофлавина равна 35. Рассчитайте концентрацию этого раствора (в мкг/100 мл), если интенсивность излучения стандартного раствора рибофлавина, имеющего концентрацию 0,040 мкг/мл, равна 50. Рассчитайте массу рибофлавина в мкг в 75 мл раствора. Методы количественного определения во флуориметрии. В каких координатах строят градуировочный график?
Метод градуировочного графика. Готовят серию эталонных растворов определяемого вещества с постепенно возрастающей концентрацией с1, с2, с3, …. Измеряют интенсивность флуоресценции Ilm каждого эталонного раствора в одних и тех же условиях. По полученным данным строят градуировочный график в координатах Ilm – c. Затем измеряют интенсивность люминесценции анализируемого раствора в тех же условиях и по градуировочному графику находят концентрацию определяемого вещества в анализируемом растворе.
Количественный метод основан на использовании прямой пропорциональной зависимости между интенсивностью люминесценции (флуоресценции) и концентрацией с определяемого вещества в растворе: Ilm = kc где k — коэффициент пропорциональности. Эта зависимость выполняется, если справедлив закон Вавилова, т.е. если квантовый выход постоянен: φ = const. Чем больше квантовый выход φ, тем больше коэффициент пропорциональности k и тем выше чувствительность флуоресцентного анализа.
Флуоресцентный анализ следует проводить в таких условиях, при которых квантовый выход флуоресценции был бы постоянным и максимальным: φ = φmax = const. Условия проведения: 1) В соответствии с законом Вавилова для того, чтобы квантовый выход был постоянным, необходимо, чтобы выполнялось условие: λabs < λlm. Обычно для возбуждающего излучения используют интервал длин волн 250-800 нм. 2) Анализируемый раствор должен быть сильно разбавленным (концентрация с < 10-4 моль/л). Уменьшение интенсивности люминесценции при увеличении концентрации раствора называется концентрационный тушением люминесценции (флуоресценции). Минимальная концентрация, при которой уже наблюдается концентрационное тушение флуоресценции, называется пороговой концентрацией. 3) Посторонние примеси должны быть удалены. 4) Температура во время проведения флуориметрических измерений должна поддерживаться постоянной. При повышении температуры наблюдается температурное тушение флуоресценции. 5) В тех случаях, когда определяемое вещество не обладает собственной флуоресценцией, проводят люминесцентную реакцию. Люминесцентная реакция — такая химическая реакция, протекание которой сопровождается либо возникновением, либо исчезновением люминесценции, либо изменением цвета.
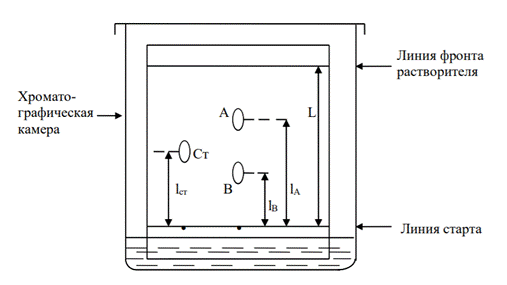
ХРОМАТОГРАФИЧЕСКИЕ МЕТОДЫ АНАЛИЗА 25. После хроматографирования на бумаге анализируемого раствора, содержащего смесь двух галогенид-анионов Х– и Y–, и в качестве свидетелей – растворов, содержащих бромид-, хлорид- и иодид-ионы, получены следующие данные: l(Cl–) = 26 мм, l(Br–) = 47 мм, l(I–) = 73 мм, l(X–) = 24 мм, l(Y–) =70 мм. Расстояние от линии старта до линии фронта растворителя 100 мм. 1. Рассчитайте коэффициенты подвижности аниона Х– и Y–, установите их природу.
Сравнивая рассчитанные коэффициенты подвижности, можно заключить, что Rf (Х-) ≈ Rf (Cl-), Rf (Y-) ≈ Rf (I-). Следовательно, компонент Х – это хлорид-ион, а компонент Y – это йодид-ион.
2. Расскажите, как проводится качественный анализ смесей веществ методом ТСХ. Качественный анализ ТСХ: 1) Идентификация веществ по характерной окраске. Невидимые хроматограммы проявляют соответствующими реагентами. Как правило, групповыми. При обработке пластинки, например, парами йода четко проявляются непредельные соединения, при опрыскивании пластинки тиоцианатом кобальта амины образуют голубые пятна на розово-белом фоне. Некоторые вещества флуоресцируют под действием УФ-света. 2) Сравнение величины Rf с табличными данными (если они получены в тех же условиях опыта). Более надежно использовать значения Rf,отн. 3) Метод свидетелей (стандартных веществ) – самый надежный способ. Стандартное вещество в том же растворителе наносят на пластинку с анализируемой пробой и хроматографируют в тех же условиях.
3.Перечислите основные этапы работы при осуществлении методик ТСХ. 1) Нанесение пробы. Анализируемую жидкую пробу наносят на линию старта (на расстоянии 2–3 см от нижнего края пластинки) с помощью капилляра, микрошприца, микропипетки, осторожно касаясь слоя сорбента (диаметр пятна на линии старта – обычно от одного до нескольких мм).
2) Развитие хроматограммы (хроматографирование). Процесс проводят в закрытых хроматографических камерах, насыщенных парами растворителя, используемого в качестве ПФ, например, в стеклянном сосуде, покрытом сверху крышкой. 3) Расшифровка хроматограмм. Если пятна на хроматограмме окрашены, то после высушивания пластинок определяют расстояние от линии старта до центра каждого пятна и вычисляют коэффициенты подвижности. Если же в состав анализируемой пробы входят бесцветные вещества, дающие неокрашенные, т.е. визуально не идентифицируемые пятна на хроматограмме, то необходимо провести детектирование этих пятен, для чего хроматограммы проявляют. Детекторами могут быть УФ-свет, нагревание, химическая обработка (H2SO4 конц, реактив Драгендорфа и тд.) После детектирования пятен на хроматограмме проводят их идентификацию, т.е. определяют, какому соединению соответствует то или иное пятно. Для этого чаще всего используют эталонные пятна «свидетелей». Иногда пятна идентифицируют по величине коэффициентов подвижности Rf, сравнивая их с известными для данных условий величинами Rf. Однако такая идентификация по величине Rf часто носит предварительный характер. Окраска флуоресцирующих пятен также используется в целях идентификации, поскольку различные соединения флуоресцируют излучением различной длины волны (разного цвета). При химическом детектировании пятен селективные реагенты даютокрашенные пятна с соединениями определённой природы, что также используется в целях идентификации. Коэффициент подвижности Rf зависит от целого ряда факторов: природы и качества растворителя, его чистоты; природы и качества сорбента (тонкого слоя), равномерности его зернения, толщины слоя; активности сорбента (содержания в нём влаги); техники эксперимента (массы образца, длины L пробега растворителя); навыка экспериментатора.
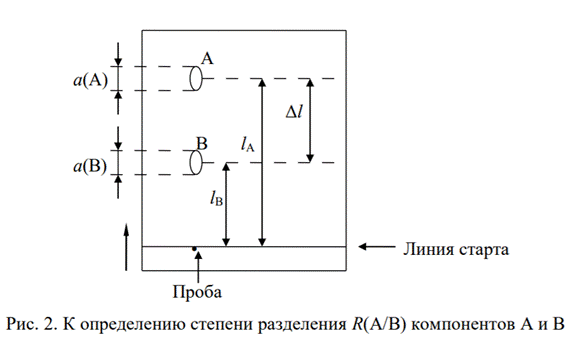
26. Смесь дипразина (I) и динезина (II) разделили в тонком слое сорбента, при этом получили следующие результаты: расстояние от линии старта до центра пятен (I) и (II) соответственно равны 30 мм и 38 мм; диаметр пятен (I) и (II) – 5 мм и 6 мм. Расстояние от линии старта до линии финиша 50 мм. 1. Рассчитайте Rf компонентов смеси и степень (критерий) разделения (динезин / дипразин).
Чем больше величина R(A/B), тем чётче разделяются пятна компонентов А и В на хроматограмме:
2. Расскажите, как проводится качественный анализ смесей веществ методом ТСХ. Качественный анализ ТСХ: 1) Идентификация веществ по характерной окраске. Невидимые хроматограммы проявляют соответствующими реагентами. Как правило, групповыми. При обработке пластинки, например, парами йода четко проявляются непредельные соединения, при опрыскивании пластинки тиоцианатом кобальта амины образуют голубые пятна на розово-белом фоне. Некоторые вещества флуоресцируют под действием УФ-света. 2) Сравнение величины Rf с табличными данными (если они получены в тех же условиях опыта). Более надежно использовать значения Rf,отн. 3) Метод свидетелей (стандартных веществ) – самый надежный способ. Стандартное вещество в том же растворителе наносят на пластинку с анализируемой пробой и хроматографируют в тех же условиях.
3.Перечислите основные этапы работы при осуществлении методик ТСХ 1) Нанесение пробы. Анализируемую жидкую пробу наносят на линию старта (на расстоянии 2–3 см от нижнего края пластинки) с помощью капилляра, микрошприца, микропипетки, осторожно касаясь слоя сорбента (диаметр пятна на линии старта – обычно от одного до нескольких мм). 2) Развитие хроматограммы (хроматографирование). Процесс проводят в закрытых хроматографических камерах, насыщенных парами растворителя, используемого в качестве ПФ, например, в стеклянном сосуде, покрытом сверху крышкой. 3) Расшифровка хроматограмм. Если пятна на хроматограмме окрашены, то после высушивания пластинок определяют расстояние от линии старта до центра каждого пятна и вычисляют коэффициенты подвижности. Если же в состав анализируемой пробы входят бесцветные вещества, дающие неокрашенные, т.е. визуально не идентифицируемые пятна на хроматограмме, то необходимо провести детектирование этих пятен, для чего хроматограммы проявляют. Детекторами могут быть УФ-свет, нагревание, химическая обработка (H2SO4 конц, реактив Драгендорфа и тд.) После детектирования пятен на хроматограмме проводят их идентификацию, т.е. определяют, какому соединению соответствует то или иное пятно. Для этого чаще всего используют эталонные пятна «свидетелей». Иногда пятна идентифицируют по величине коэффициентов подвижности Rf, сравнивая их с известными для данных условий величинами Rf. Однако такая идентификация по величине Rf часто носит предварительный характер. Окраска флуоресцирующих пятен также используется в целях идентификации, поскольку различные соединения флуоресцируют излучением различной длины волны (разного цвета). При химическом детектировании пятен селективные реагенты даютокрашенные пятна с соединениями определённой природы, что также используется в целях идентификации. Коэффициент подвижности Rf зависит от целого ряда факторов: природы и качества растворителя, его чистоты; природы и качества сорбента (тонкого слоя), равномерности его зернения, толщины слоя; активности сорбента (содержания в нём влаги); техники эксперимента (массы образца, длины L пробега растворителя); навыка экспериментатора.
27. При анализе раствора смеси анионов Br–, I–, SCN– и раствора-свидетеля NO3– получили следующие хроматографические данные: L = 70 мм, l(Br–) =36 мм, l(I–) = 47 мм, l(SCN–) = 56 мм, l(NO3–) = 40 мм. 1. Рассчитайте относительные коэффициенты подвижности для указанных ионов.
2. Расскажите, как проводится качественный анализ смесей веществ методом ТСХ. Каков механизм разделения веществ в ТСХ? Качественный анализ ТСХ: 4) Идентификация веществ по характерной окраске. Невидимые хроматограммы проявляют соответствующими реагентами. Как правило, групповыми. При обработке пластинки, например, парами йода четко проявляются непредельные соединения, при опрыскивании пластинки тиоцианатом кобальта амины образуют голубые пятна на розово-белом фоне. Некоторые вещества флуоресцируют под действием УФ-света. 5) Сравнение величины Rf с табличными данными (если они получены в тех же условиях опыта). Более надежно использовать значения Rf,отн. 6) Метод свидетелей (стандартных веществ) – самый надежный способ. Стандартное вещество в том же растворителе наносят на пластинку с анализируемой пробой и хроматографируют в тех же условиях.
|
|||||||||
|
Последнее изменение этой страницы: 2021-07-18; просмотров: 1616; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.220.136.165 (0.067 с.) |