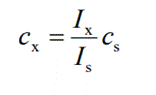Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Выбор оптимальных условий проведения флуоресцентного анализаСодержание книги
Поиск на нашем сайте
Метод флуоресцентного анализа позволяет количественно определять не только вещества, способные к собственному свечению, но и ряд веществ, которые не способны к флуоресценции. Многие органические вещества обладают собственной флуоресценцией и могут быть количественно определены путём измерения интенсивности флуоресценции непосредственно анализируемых растворов. При определении неорганических веществ, большинство из которых не обладает собственной флуоресценцией, предварительно проводят аналитические реакции, в результате которых образуются способные к флуоресценции комплексные соединения. В том случае, когда в результате такой реакции образуется малорастворимое в воде комплексное соединение, его экстрагируют из водной фазы органическим растворителем. При анализе раствора, в котором присутствуют мешающие анализу примеси, проводят аналитическую реакцию с определяемым ионом и образующийся комплекс экстрагируют из водной фазы в органическую фазу. Мешающие ионы остаются в водной фазе. Полученный экстракт определяемого вещества, существующего в составе флуоресцирующего комплекса, анализируют далее обычным образом. Концентрацию определяемого вещества в анализируемом растворе при использовании флуориметрии находят методом градуировочного графика или методом одного стандарта. Метод градуировочного графика. Готовят серию эталонных растворов определяемого вещества с постепенно возрастающей концентрацией с1, с2, с3, …. Измеряют интенсивность флуоресценции Ilm каждого эталонного раствора в одних и тех же условиях. По полученным данным строят градуировочный график в координатах Ilm – c. Затем измеряют интенсивность люминесценции анализируемого раствора в тех же условиях и по градуировочному графику находят концентрацию определяемого вещества в анализируемом растворе. Метод одного стандарта. Готовят стандартный раствор с точно известной концентрацией сs определяемого вещества, близкой к концентрации cx того же определяемого вещества в анализируемом растворе. В одинаковых условиях измеряют интенсивность флуоресценции стандартного Is и анализируемого Ix растворов. Концентрацию cx рассчитывают по формуле
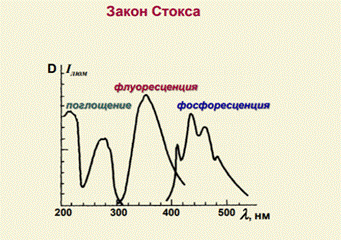
Закон Стокса: Спектр флуоресценции лежит в более длинноволновой области по сравнению со спектром поглощения того же вещества
Для проведения флуориметрического анализа используют приборы двух типов: фильтрационный флуориметр и спектрофлуориметр. Фильтрационный флуориметр состоит из источника излучения, первичного фильтра длин волн, камеры для образца, вторичного фильтра длин волн и системы детектирования флуоресценции. Как правило, детектор помещен под углом 90о к возбуждающему световому потоку. Геометрия прямого угла предусматривает детектирование только произведенного флуоресцентного сигнала. Однако детектор все-таки получает часть возбуждающего излучения в результате рассеивающих свойств самого раствора, а также из-за присутствия в растворе твердых частиц. Для устранения этого остаточного рассеяния используются спектральные фильтры. Первичный фильтр отбирает коротковолновое излучение, способное к возбуждению испытуемых образцов, вторичный фильтр пропускает флуоресценцию в длинноволновой области, но блокирует рассеянное возбуждение. Детекторы флуориметров преобразуют оптический сигнал в электрический с помощью фотоумножителей разных типов. Каждый тип детектора имеет специальные характеристики: спектральная область максимальной чувствительности, степень усиления, соотношение сигнал/шум. Спектрофлуориметры отличаются от фильтрационных флуориметров тем, что вместо спектральных фильтров в них используются монохроматоры типа призмы или решетки. Эти приборы более предпочтительны для аналитических целей. В спектрофлуориметрах монохроматоры снабжены щелями. Чем уже щель, тем выше разрешение и спектральная чистота, но меньше чувствительность. Выбор размера щели определяется разделением между длинами волн возбуждающего и испускаемого излучения и необходимым уровнем чувствительности. В качестве источников возбуждающего излучения в флуориметрах используют: ▪ ртутные лампы низкого давления, предоставляющие большое количество длин волн возбуждения, но не являющиеся источником излучения равномерного спектра; ▪ ксеноновые газоразрядные лампы, обеспечивающие высокоинтенсивное почти равномерное излучение в широком диапазоне спектра (300 – 800 нм) и достаточно интенсивное в коротковолновой области вплоть до 200 нм;
▪ лазеры, излучающие свет высокой интенсивности в очень узком интервале длин волн (не более 0,01 нм) и позволяющие благодаря этому не использовать монохроматоры или первичные светофильтры; ▪ светодиоды и светодиодные матрицы, излучающие свет в определённых диапазонах длин волн. Для размещения анализируемых проб в флуориметрах используют, как правило, прямоугольные кварцевые кюветы, отполированные со всех 4 вертикальных сторон, иногда – цилиндрические кюветы или пробирки. Обычно объем испытуемых образцов составляет 2 – 3 мл, но к некоторым приборам прилагаются кюветы вместимостью от 100 до 300 мкл или капиллярные держатели для еще меньшего объема.
|
||||||
|
Последнее изменение этой страницы: 2021-07-18; просмотров: 274; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.16.15.215 (0.008 с.) |