Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь FAQ Написать работу КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Методы испытания стерильности.Содержание книги
Поиск на нашем сайте 1. методом прямого посева используют для испытания на стерильность ЛС, не обладающих антимикробным действием или антимикробное действие которых можно устранить разведением или инактивированием, а также для препаратов, испытание которых невозможно выполнить методом мембранной фильтрации. 2. Метод мембранной фильтрации используют во всех случаях, когда природа препарата, его физико-химические свойства позволяют фильтровать его через мембранные фильтры.
Питательные среды: 1. жидкая тиогликолевая среда для выявления анаэробных и аэробных бактерий, для ИЛП; 2. жидкая среда на основе гидролизата казеина и соевых бобов (среда Сабуро) для выявления грибов и аэробных бактерий.
ИСПЫТАНИЕ НА СТЕРИЛЬНОСТЬ 2.1. Отбор образов для испытания Отбирают образцы препарата, как указано в Таблице в ОФС, учитывают общее количества единиц в серии.
2.2. Метод мембранной фильтрации: для определения стерильности ЛС - обладающих выраженным антимикробным действием - ЛС в емкостях вместимостью более 100 мл. ! Кроме препаратов с антимикробным действием, нерастворимых в водных разбавителях или ИПМ! Основных стадий: смачивание мембран, подготовка образцов и фильтрация содержимого всех емкостей через мембранные фильтры, отмывка мембранных фильтров соответствующим стерильным раствором, добавление питательной среды и инкубирование посевов.
Метод прямого посева - для ЛС, не обладающих антимикробным действием - тех препаратов, испытание которых невозможно выполнить методом мембранной фильтрации. В том случае, если препарат обладает антимикробным действием в условиях испытания, его нейтрализуют инактиваторами или увеличивая объем питательной среды. Испытуемые образцы засевают непосредственно в питательные среды в соотношении 1:10 или 1:20.
Условия инкубации посевов Посевы инкубируют не менее 14 сут при температуре 32,5 ± 2,5 градусов в жидкой тиогликолевой среде и при температуре 22,5 ± 2,5 градусов в жидких соевоказеиновой среде или среде Сабуро (независимо от метода посева). При испытании ИЛП возможно использование только тиогликолевой среды и инкубирование посевов при двух температурных режимах 32,5 ± 2,5
Учет и интерпретация результатов испытания Наличие роста микроорганизмов определяют визуально в проходящем свете. - Если испытуемое ЛС вызывает помутнение питательной среды и визуально нельзя определить наличие или отсутствие микробного роста, через 14 сут после начала испытания переносят не менее 1 мл помутневшей среды в пробирки с аналогичной стерильной средой. Инкубируют исходные и повторные посевы. Общее время инкубации должно составлять не менее чем 14 + 4 сут от начала испытания.
При отсутствии роста микроорганизмов, считают, что испытуемый препарат соответствует требованиям испытания на стерильность. При обнаружении роста микроорганизмов, определяемого визуально по наличию мутности, осадка, хлопьев и других изменений среды и подтверждаемого микроскопическим исследованием, считают, что испытуемый препарат не соответствует требованиям испытания на стерильность.
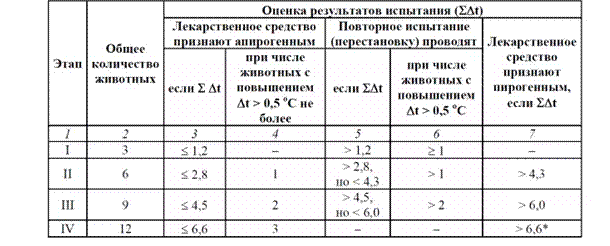
Испытание на пирогенность. Область применения, методика выполнения испытания, оценка результатов. Область применения. Испытание на пирогенность инъекционных растворов и фармацевтических субстанций, из которых они изготавливаются. Методика выполнения. Биологический метод Испытуемое лекарственное средство вводят в ушную вену кролика, если в фармакопейной статье не указан другой путь введения. Объем инъецируемого раствора должен составлять не менее 0,2 мл и не более 10 мл на 1,0 кг массы тела животного. Испытание лекарственного средства проводят на группе из трех кроликов с исходной температурой 38,5-39,5 ºС. Измерения температуры после внутривенного введения испытуемого лекарственного средства проводят с интервалом не более 30 минут на протяжении трех часов. При других путях парентерального введения – на протяжении пяти часов. Учет результатов. На каждом этапе используют трех кроликов. Максимальное число этапов не должно превышать четырех. По окончании каждого из этапов испытания определяют максимальное изменение температуры (дельта t) тела каждого кролика по сравнению с исходным значением. Изменение температуры тела животного ниже исходной величины принимают за нулевое и не учитывают. Для трех кроликов определяют сумму индивидуальных максимальных повышений температур (S Dt). Значения S Dt, полученные на разных этапах испытания, последовательно суммируют, а результаты сравнивают с уровнями, указанными в таблице.
|
||
|
Последнее изменение этой страницы: 2021-07-18; просмотров: 138; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 216.73.216.119 (0.01 с.) |