
Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Гармоническое единство спектра атома
© Верин О.Г. Контакт с автором verinOG@list.ru Открытие законов формирования электронных оболочек атомов [1] дает возможность совершенно по-новому взглянуть на природу атомных спектров. В частности, дробные значения главного квантового числа свидетельствуют о возбуждении кратных резонансов электронных оболочек атомов и составляют для каждого атома свой особый “набор”. Однако при всем многообразии спектров отчетливо проявляются закономерности, говорящие о гармоническом единстве каждого атома, что, несомненно, станет надежным ориентиром для исследователей и найдет применение при анализе и систематизации атомных спектров. Данная статья является продолжением работы по изучению свойств электронных оболочек на основе надежно подтвержденных экспериментами справочных данных о физических характеристиках атомов. ___________________________________________________________________________________ Анализ экспериментальных данных [1] показал, что электронные оболочки атомов являются резонансными образованиями, и поэтому постулат Бора о квантовании момента количества движения электрона вокруг ядра атома на самом деле является условием резонанса: электронная оболочка содержит в себе целое количество длин волн электрона h / p (хотя математически это одно и то же):
Число n называется главным квантовым числом, R – радиус электронной оболочки, p – импульс электрона, h – постоянная Планка. Таким образом, выражение (1) задает “разрешенные” резонансные значения пространственного волнового коэффициента для электронной оболочки
Установлено также, что главное квантовое число может приобретать дробные значения (N1/N2) за счет возбуждения кратных гармоник. Для определения конкретных величин были использованы справочные данные о потенциалах ионизации атомов. В частности, для атомов, имеющих один электрон на внешней оболочке (водородоподобных атомов) эти расчеты наиболее просты и подтвердили наличие кратных резонансов в электронных оболочках. Приведем соответствующие расчеты для атома лития. Длина волны электрона определялась, исходя из его кинетической энергии, которая, в свою очередь, численно соответствует потенциалу ионизации
Поэтому длина волны электрона и условный радиус Rλ (определяющий пространственный волновой коэффициент) определяются из формул:
Например, подставляя в (4) потенциал ионизации лития 5,39 эВ, получаем следующие конкретные величины:
Здесь R Б – радиус Бора, а условный радиус Rλ (показатель скорости пространственных волновых изменений) фактически представлен уже в (2). Таким образом, внешняя электронная оболочка лития характеризуется главным квантовым числом (n =1,593), которое не является целым и находится в промежутке между 1 и 2! Однако в действительности внешняя электронная оболочка лития также является резонансной - с целым количеством длин волн. Достигается это за счет возбуждения более высокочастотной гармоники. Для атома лития целое число длин волн N1=8, характеризующее резонанс внешней электронной оболочки, оказалось результатом умножения числа 1,593 на число N2=5,02, указывающее на номер гармонической составляющей. То есть, пятая гармоника “возбуждает” восемь длин волн резонанса электронной оболочки лития. При этом формула для реального радиуса оболочки оказывается справедливой и при значении n, отличном от целого числа
Эта величина действительно соответствует реальному значению радиуса внешней электронной оболочки лития, получающемуся из выражения для потенциала ионизации одноэлектронной внешней оболочки атома [1]
Так как атомов, подобных литию, с одним электроном на внешней электронной оболочке довольно много, то были проведены аналогичные расчеты и для них. Результаты всех расчетов сведены в таблице, которую мы здесь воспроизводим с тем, чтобы было удобно эти данные сравнить с аналогичными расчетами для возбужденных энергетических уровней. Приведенные в таблице 1 цифры говорят о закономерном характере полученных результатов: внешние оболочки рассмотренных атомов в невозбужденном состоянии имеют дробные значения главного квантового числа. При этом, главные квантовые числа выражаются величинами, близкими к обычным дробям, в числителе и в знаменателе которых стоят целые числа. Таким образом, в работе [1] было установлено, что Природа использует в электронных оболочках не только “простые” резонансы, но и возбуждаемые на кратных гармонических составляющих, в результате чего атомы более компактны и, одновременно, обладают способностью “разместить” в электронных оболочках большое количество электронов (в пучностях резонансов оболочек).
Невозбужденные внешние электронные оболочки атомов. Таблица 1
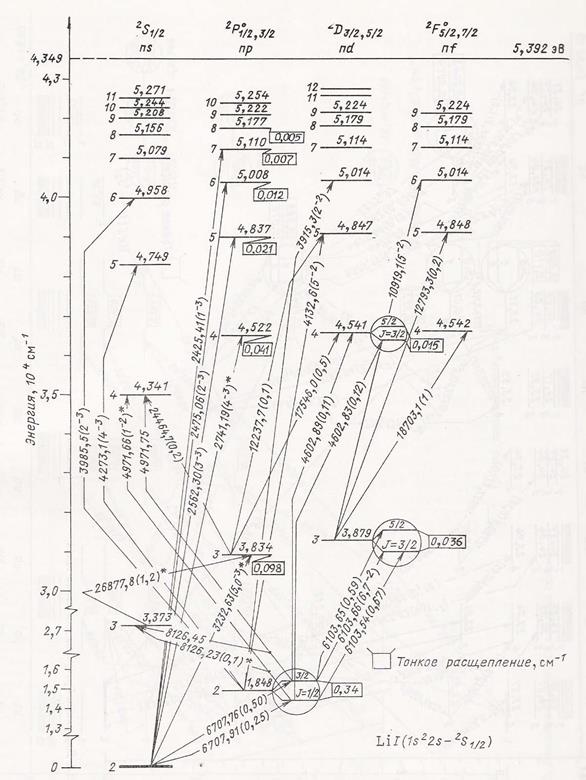
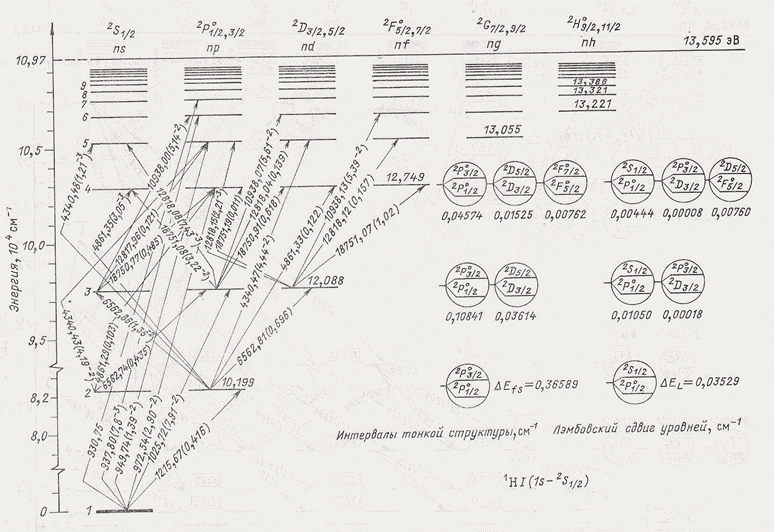
Дополнительным подтверждением этой закономерности является аналогичное явление, обнаруженное при анализе возбужденных состояний атомов и соответствующих спектров поглощения (излучения) атомов. В качестве примера в работе [1] был рассмотрен спектр атома лития. На рис. 1 показана диаграмма Гротриана для атома лития [2], которая изображает совокупность возбужденных энергетических уровней и переходов между ними. Для удобства анализа этой диаграммы были произведены некоторые дополнительные вычисления. Во-первых, уровни энергии нам удобнее отсчитывать не от самого низкого уровня, соответствующего энергии ионизации (как это сделано на диаграмме), а от “абсолютного” нуля (то есть, от энергии на бесконечном расстоянии от атома). Во-вторых, были рассчитаны все те же характеристики электрона для возбужденных уровней, что и в таблице 1. Итоговая таблица 2 включает в себя также главное квантовое число n (первый столбец), которым помечен каждый возбужденный уровень на диаграмме (рис. 1). Это сделано для сравнения с расчетным n (отношением N 1 / N 2). Результаты, отраженные в таблице 2, оказались весьма красноречивыми. Расчетные величины главного квантового числа (n расч.) в большинстве случаев с хорошей точностью совпадают с целочисленными значениями (первый столбец), которыми отмечены соответствующие уровни на диаграмме Гротриана. Однако в шести случаях (почти по каждому третьему возбужденному уровню) составители диаграммы, видимо, долго не могли определиться с главным квантовым числом, так как оно должно быть дробным (N 1 / N 2), а не целым, как это указано на диаграмме. При этом числа N 1, и N 2 определяются с хорошей точностью простыми расчетами. Итак, возбужденные уровни энергии лития приблизительно в 2/3 случаев соответствуют целочисленным (обычным) значениям n, а в 1/3 случаев - дробным значениям главного квантового числа. Эти последние уровни на диаграмме Гротриана “вынужденно” помечены ближайшими целочисленными значениями. Возбужденные состояния атома лития Таблица 2
Из приведенной таблицы следует, что дробные главные квантовые числа в промежутках между целыми числами составляют последовательность значений, увеличивающихся на единицу 13/5, 18/5, 23/5…38/5, которая к тому же еще и продолжает “невозбужденное” значение 8/5 для атома лития (табл.1)!
Кроме того, обращает на себя внимание большая удаленность (R/RB) внешнего электрона от ядра атома на возбужденных уровнях при больших n. Такая удаленность от ядра, казалось бы, должна сводить на нет влияние остова атома на электрон, а параметры возбужденных оболочек должны быть близки к “эталонным” величинам, характерным для атома водорода. Далее мы будем обсуждать все эти “странности”.
Рис. 1. Диаграмма Гротриана для атома лития [2]. Мы повторили здесь некоторые результаты, изложенные в предыдущей статье [1], (а заодно немного уточнили последний столбец в табл.2) для того, чтобы ввести читателя в суть излагаемого вопроса и перейти к дальнейшему изложению исследования атомных спектров. Оказалось, что визуализация информации уже содержащейся в таблице 2, раскрывает дополнительные возможности для осмысления результатов расчетов. На рис. 2 представлен “спектр” главных квантовых чисел возбужденных состояний атома лития. То есть, средний столбец таблицы 2 изображен в виде графика (значения п просто расположены в порядке возрастания). Этот график (или диаграмма), представляющий спектр возбужденных состояний лития, наглядно свидетельствует не об энергетическом “ключе” периодичности спектра, а об определяющей роли частотных взаимосвязей возбужденных состояний с остовом атома. А именно, все указывает на то, что остов атома “генерирует” некий набор частот, с которыми взаимодействует электрон, находясь на возбужденном уровне.
Рис. 2. Спектр п возбужденных состояний атома лития.
Дело в том, что на верхних возбужденных уровнях электрон действительно находится на больших расстояниях от остова атома (таблица 2), и на таких больших расстояниях энергетическое воздействие остова незначительно. Тем более, что размеры самих остовов водородоподобных атомов малы (они были определены в [1], таблица 3), а, следовательно, характеристики более высоких уровней должны были бы, как уже отмечалось, приближаться к аналогичным уровням водорода. Однако спектр не следует этому “очевидному” правилу.
Радиусы атомных остовов [1]. Таблица 3
Тем не менее, диаграммы Гротриана интерпретируют существенные отличия спектров атомов от “эталонного” спектра водорода влиянием других квантовых чисел (наряду с главным квантовым числом). Такой подход, как уже говорилось, не может объяснить реальные спектры атомов. Приходится констатировать, что неудовлетворительное состояние дел с классификацией и систематизацией спектров атомов вызвано не только сложностями самого анализа спектров атомов, но и следствием очевидной несостоятельности существующей теории электронных оболочек атомов. Эту проблему фактически необходимо решать заново, исходя из других физических представлений, а именно, исходя из резонансной природы электронных оболочек и из гармонического единства спектра каждого атома. Чтобы иметь возможность убедиться в этом, достаточно сравнить спектры главных квантовых чисел возбужденных состояний нескольких разных атомов. Для такого сравнения, помимо таблицы 2 из предыдущей работы [1], ниже приведены результаты аналогичных расчетов для спектров атомов водорода, гелия, калия, натрия, серебра, цезия и рубидия.
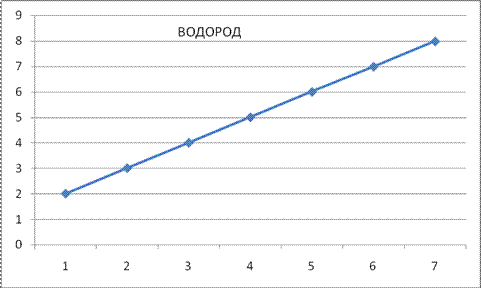
Рис. 3. Диаграмма Гротриана для атома водорода [2]. Из этих данных видно, что чем проще остов атома, тем ярче выражены отдельные гармонические составляющие и их периодическое повторение в спектре главных квантовых чисел. И наоборот, сложные атомные остовы (Os, Rb) создают такое обилие частот, которое обусловливает возбуждение многочисленных электронных состояний, а спектр главных квантовых чисел становится все более плотным и линейным, как у водорода. Начав статью с рассуждения о волновых свойствах электрона, мы теперь опять приходим к выводу о том, что эти свойства не существуют сами по себе [3], а определяются взаимодействием электрона с окружающими его объектами (внешними колебаниями). Соответственно в атомах речь идет о взаимодействии электронов оболочек с колебаниями, которые создают вокруг себя остовы атомов.
Рис. 4. Спектр п возбужденных состояний атома водорода. Возбужденные состояния атома водорода. Таблица 4
Энергия возбужденного уровня атома, как и стационарного энергетического уровня, определяется значением главного квантового числа [4]
Поэтому спектр главных квантовых чисел возбужденных состояний любого атома “автоматически” определяет совокупность соответствующих энергетических уровней и спектр излучения (поглощения). Но анализ спектра главных квантовых чисел, как мы видели, существенно проще в виду того, что ему свойственна определенная периодичность (хотя и не идеальная).
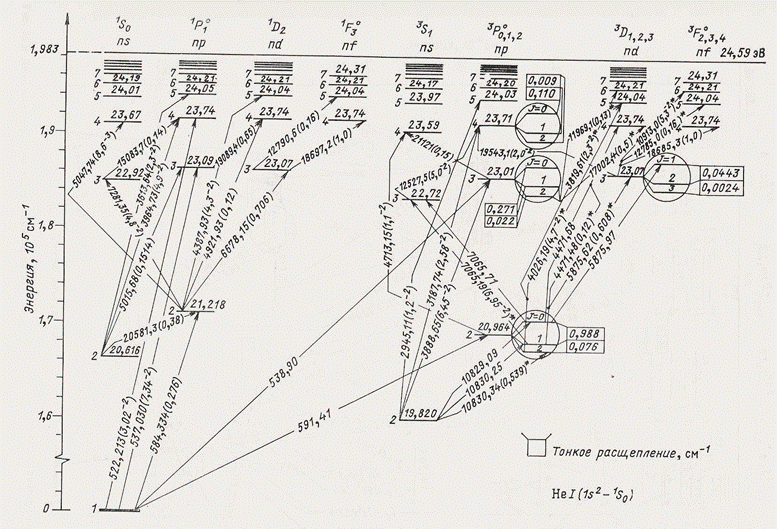
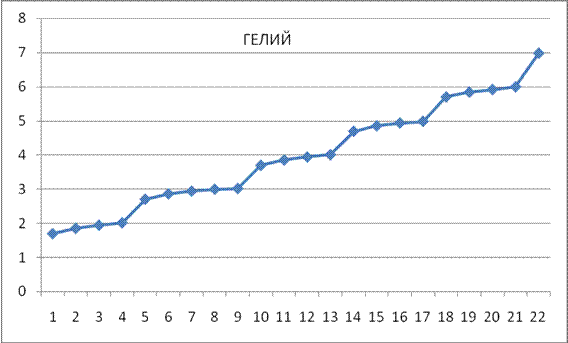
Рис. 5. Диаграмма Гротриана для атома гелия [2].
Рис. 6. Спектр п возбужденных состояний атома гелия.
Возбужденные состояния атома гелия. Таблица 5
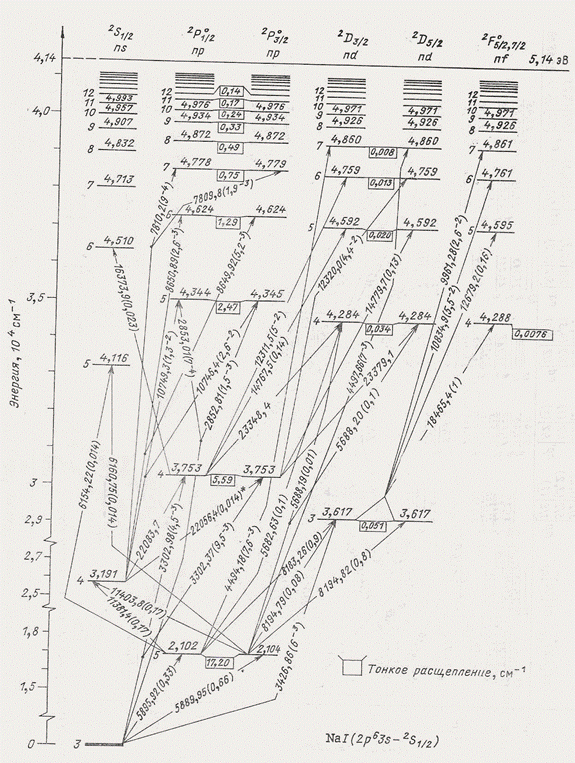
Рис. 7. Диаграмма Гротриана для атома натрия [2].
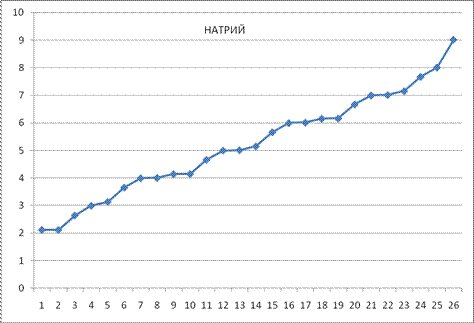
Рис. 8. Спектр п возбужденных состояний атома натрия. Возбужденные состояния атома натрия. Таблица 6
Рис. 9. Диаграмма Гротриана для атома серебра [2].
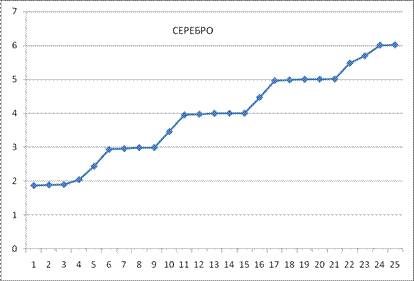
Рис. 10. Спектр п возбужденных состояний атома серебра.
Возбужденные состояния атома серебра. Таблица 7
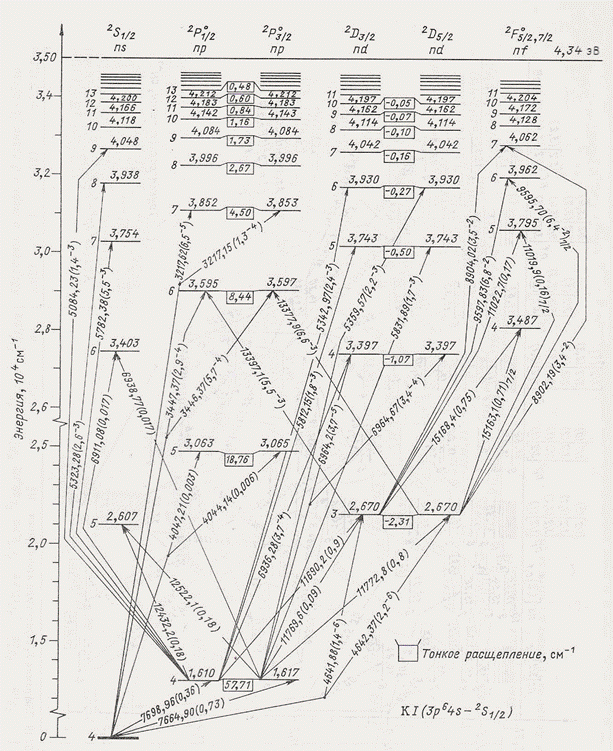
Рис. 11. Диаграмма Гротриана для атома калия [2].
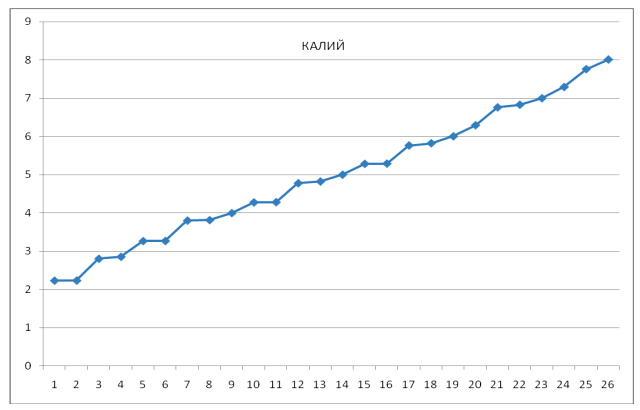
Рис. 12. Спектр п возбужденных состояний атома калия.
Возбужденные состояния атома калия. Таблица 8
Рис. 13. Диаграмма Гротриана для атома цезия [2].
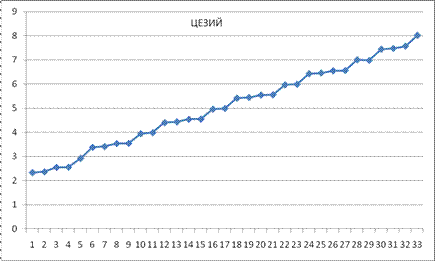
Рис. 14. Спектр п возбужденных состояний атома цезия. Возбужденные состояния атома цезия. Таблица 9
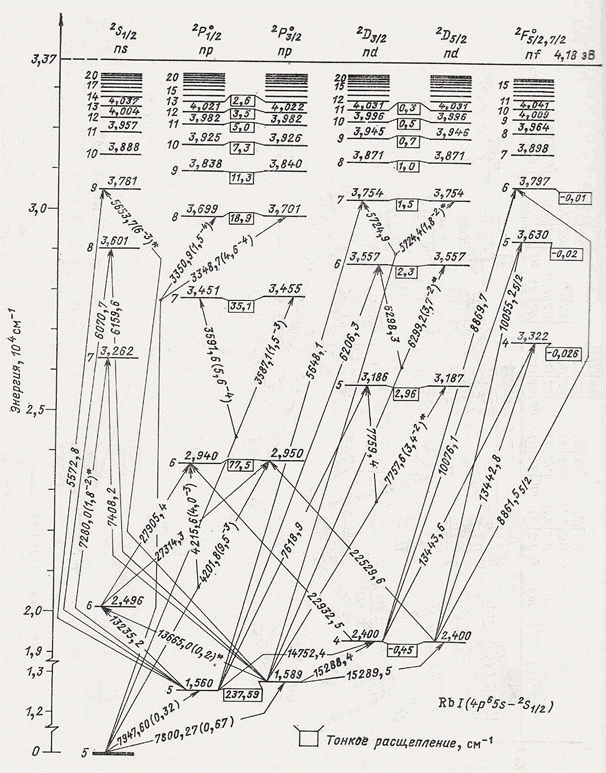
Рис. 15. Диаграмма Гротриана для атома рубидия [2].
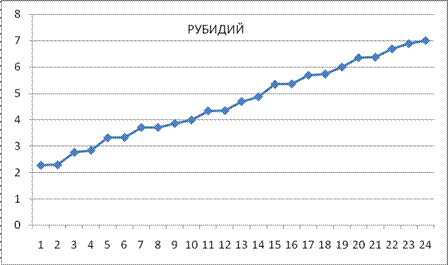
Рис. 16. Спектр п возбужденных состояний атома рубидия. Возбужденные состояния атома рубидия. Таблица 10
Анализ приведенных таблиц и графиков показывает, что для каждого атома характерен свой индивидуальный “набор” (спектр) главных квантовых чисел возбужденных состояний. В промежутках между целыми значениями дробные числа, как правило, составляют последовательности отличающихся на единицу значений. То есть, возбуждение резонансов в электронных оболочках действительно происходит на кратных гармонических составляющих. Откуда берутся эти последовательности дробных величин? Не вдаваясь в теорию, мы можем лишь отметить, что дробными величинами характеризуется уже ближайшая к ядру наименьшая оболочка атомов из двух электронов (первая куперовская пара). В [1] показано, что радиус этой оболочки и сумма потенциалов ионизации определяются дробными значениями (в величинах радиуса Бора и потенциала ионизации водорода – естественных атомных единицах)
Дополнительным фактором образования рядов гармоник является солитонная природа электрона и других частиц, что “автоматически” означает нелинейность их свойств и присутствие большого количества гармонических составляющих в окружающем их поле [3]. Интересно, что возбужденные состояния некоторых атомов (Na, K, Cs), как и у атома лития, “перекликаются” с гармониками основных невозбужденных состояний внешней оболочки атомов (таблица 1). Это еще раз свидетельствует о наличии соответствующих частот колебаний атомного остова, с которыми происходит взаимодействие электрона, находящегося будь то на основном, либо на возбужденном энергетическом уровне. Общей чертой всех приведенных результатов расчетов является широкий диапазон спектров главных квантовых чисел, причем минимальные значения у всех атомов начинаются около 2, как у атома водорода, а максимальные простираются вплоть до десяти и далее (приходится на чем-то ограничиться). В то же время, одинаковый нижний предел главных квантовых чисел возбужденных состояний атомов (около 2) является еще одним свидетельством малых размеров атомных остовов (меньше или порядка радиуса Бора). Следует заметить, что, несмотря на большую “популярность” диаграмм Гротриана у спектроскопистов, химиков и многих других исследователей, в фундаментальные курсы по квантовой механике их обычно не включают [5]. Возможно, это связано с неубедительностью попыток объяснить спектры атомов различными состояниями (квантовыми числами) атомных остовов и самих электронов. Эти надписи находятся в самом верху диаграмм Гротриана. Известно, что решение задачи о движении электрона в кулоновском поле ядра дает результат, согласно которому энергетические уровни определяются только главным квантовым числом. Остальные квантовые числа определяют лишь степень вырождения энергетического уровня. Такие уровни расщепляются (вырождение снимается) только при дополнительных воздействиях (например, из-за влияния спина или стороннего магнитного поля). Однако расщепление уровней, как правило, не велико [4]. Поэтому, учитывая большое расстояние от центра атома до электрона в возбужденном состоянии и малые размеры атомного остова, трудно объяснить столь большие отличия в спектрах разных атомов. То есть, более высокие возбужденные уровни всех атомов должны были бы повторять соответствующие возбужденные уровни водорода, но они “упорно следуют” своим периодическим “спектрам” дробных главных квантовых чисел. Такое “упорство” невозможно объяснить ни чем иным, как мощным воздействием соответствующего “набора” частот, генерируемых остовом атома, который и определяет спектр атома. Поэтому определенная “настороженность” к теоретической стороне диаграмм Гротриана вполне объяснима. Нужно ли в связи с этим отказываться от диаграмм Гротриана? Естественно, нет, поскольку практика показала, что их использование удобно. Просто систему обозначения возбужденных уровней необходимо привести к виду, отражающему физическую реальность, а именно, использовать для обозначения возбужденных уровней дробные величины главных квантовых чисел. В любо
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-07-19; просмотров: 117; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.146.255.127 (0.079 с.) |
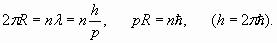 (1)
(1)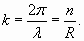 (2)
(2)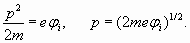 (3)
(3)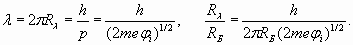 (4)
(4)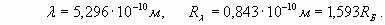
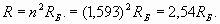 (5)
(5)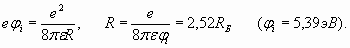 (6)
(6)

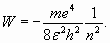 (7)
(7)


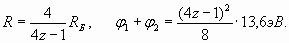 (8)
(8)


