Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Определение ЭДС гальванического элементаИ потенциалов отдельных электродов В зависимости от концентрации растворов Цель работы Усвоить теоретические сведения о природе электрохимического потенциала, влиянии ряда факторов на его величину; освоить методику экспериментального определения величины ЭДС гальванического элемента и потенциалов отдельных электродов; изучить зависимость потенциала электрода от концентрации электролита; сравнить полученные данные с теоретическими расчетами.
Вопросы коллоквиума 1. Причины возникновения скачка потенциала на границе проводник первого рода – электролит. 2. Физический смысл величины электродного потенциала. Стандартный электродный потенциал. Связь величины ЭДС гальванического элемента с термодинамическим потенциалом. 3. Зависимость электродного потенциала и ЭДС гальванического элемента от концентрации электролита (уравнение Нернста). Вывод уравнения Нернста. 4. Типы электродов. 5. Концентрационные гальванические элементы.
Приборы и реактивы
1. Потенциометр постоянного тока P 363; 2. Насыщенный раствор KCl; 3. Соли для приготовления электролита (CuSO4 ∙5H2O, ZnSO4∙7H2O); 4. Сосуды для электродов – 2шт., электроды (медный и цинковый) с присоединенными к ним проводниками – 2 шт.; 5. Мерные цилиндры на 100 см3 – 2 шт., лабораторная посуда. Методика выполнения работы и её обоснование
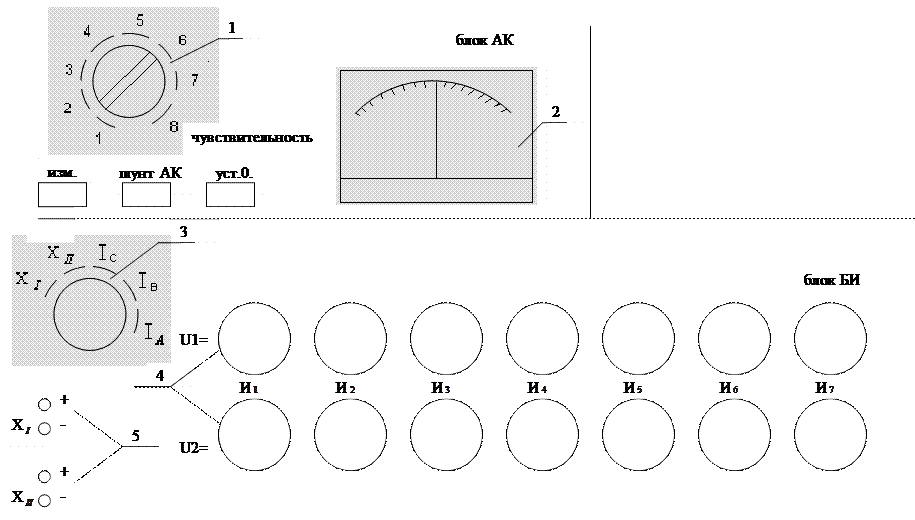
Принципиальная схема установки Экспериментальная установка для определения величины ЭДС гальванического элемента и потенциалов отдельных электродов включает в себя электролитическую ячейку и изображенный на рисунке потенциометр постоянного тока P 363. Потенциометр состоит из трех блоков: измерительного блока (БИ), автокомпенсатора напряжения (АК), блока усилителя и стабилизатора напряжения (СН). Подготовка потенциометра к работе Осматривают панель блока измерения (БИ) и блока автокомпенсатора (АК). Два ряда (U1 и U2) измерительных декадных переключателей (блок БИ) должны быть установлены на отметке 0. В зависимости от того, какие клеммы используются в работе (X1 или X2), измерения производят с помощью соответствующего ряда декадных переключателей (U1 или U2). Кнопка “измерение” блока (АК) должна быть в отжатом положении, ручку чувствительности блока (АК) устанавливают в положение 1. Включают все блоки потенциометра в сеть и прогревают их перед началом измерения не менее 40 минут. Порядок работы на потенциометре (ручка чувствительности блока АК находится в положении 1) 1. Соблюдая полярность подключают источник измерения ЭДС к зажимам X1, ставят переключатель рода работы в положение X1 (блок БИ). 2. Нажимают и зафиксируют кнопку “измерение” на блоке АК. 3. Посредством декадного переключателя И1 (блок БИ) компенсируют измеряемую ЭДС так, чтобы стрелка выходного прибора блока АК была подведена к нулю. 4. Переводят ручку чувствительности блока АК в положение 2 и посредством декадного переключателя И2 компенсируют измеряемую ЭДС. (подобно п.3). 5. Переводят ручку чувствительности в положение 3 и посредством декадного переключателя И3 компенсируют измеряемую ЭДС. 6. Последовательно увеличивая чувствительность переключением до положения 5 и, компенсируя декадными переключателями И4 – И5, заканчивают измерение ЭДС гальванического элемента. 7. По окончании измерения производят отсчет (записывают показания с декадных переключателей) измеряемой ЭДС. 8. Возвращают переключатель “чувствительность” блока АК в положение 1. 9. Ставят декадные переключатели И1 – И5 в положение 0. После выполненных операций 8 и 9 можно производить отключение источника измеряемой ЭДС и другие работы по подготовке к следующим замерам. 10. Для определения потенциалов отдельных электродов, подключают к потенциометру на клеммы X1 контакты от исследуемого и вспомогательного электродов и проводят измерение подобно п.1–9.
Порядок выполнения работы
1. В соответствии полученным заданием готовят исходные растворы электролитов для полуэлементов гальванической ячейки. На аналитических весах взвешивают заданное количество соли, помещают ее в колбу или стакан и заливают рассчитанным и отмеренным мерным цилиндром количеством дистиллированной воды. Перемешивая стеклянной палочкой, растворяют соль и получают раствор. 2. Берут электроды и зачищают их наждачной бумагой. Промывают водой. 3. Взяв ячейку полуэлемента в левую руку таким образом, чтобы сильфон ячейки был сверху, а сосуд наклонен отверстием ячейки вправо, заливают раствор электролита на ¾ объема ячейки. Не изменяя положение ячейки, вставляют электрод в ячейку и небольшим усилием, покручивая под углом, вводят пробку в ячейку. Чтобы убедиться что пробка хорошо закрывает ячейку, наклоняют ее и, смотрят, весь ли периметр пробки смочен раствором. После этого полуэлемент ставят вертикально и подносят носик сильфона к цилиндру. 4. Если сильфон полуэлемента не заполнен электролитом, посредством зажима необходимо разгерметизировать ячейку и ввести небольшое количество воздуха. Разряжение в сосуде уменьшится, и сильфон будет наполнен раствором. Полуэлемент устанавливают в подставку таким образом, чтобы сильфон был погружен в стакан с хлористым калием, и носик его находился в растворе хлористого калия. Таким же образом готовят второй полуэлемент. 5. Присоединяют клеммы проводников от электродов к потенциометру, пользуясь руководством для работы с потенциометром. 6. При определении потенциалов отдельных электродов составляют гальванический элемент полуэлемента исследуемого и вспомогательного электродов. Вспомогательный электрод помещают в стакан с хлористым калием. 7. Подсоединяют проводники измеряемого и вспомогательного электродов к клеммам X1, (убрав один из электродов от клеммы) и проводят измерение ЭДС вновь собранного гальванического элемента (измеряемый электрод – вспомогательный электрод). 8. Закончив все измерения с данной концентрацией электролита в полуэлементах, отсоединяют от клеммы X1 тот полуэлемент, в котором необходимо сменить электролит. 9. Промывают электрод водой, зачищают снова наждачной бумагой и еще раз промывают. 10. Готовят новый раствор электролита путем разбавления исходного и, аналогично п.3, готовят полуэлемент с другой концентрацией электролита. 11. Собирают из полуэлементов гальваническую ячейку и измеряют ЭДС этого гальванического элемента. 12. Полученные при измерении потенциалы отдельных электродов относительно хлоридсеребряного электрода (ХСЭ) пересчитывают относительно водородного электрода. Если исследуемый электрод подсоединен к клемме “+”, а хлоридсеребряный к “–“, то выполняется уравнение
где Если исследуемый электрод присоединен к клемме “–“, а ХСЭ электрод к клемме “+ ‘’, то выполняется уравнение
13. По уравнению Нернста рассчитывают потенциалы отдельных электродов для различных концентраций с учетом активностей ионов в растворе. 14. Зная рассчитанные значения потенциалов отдельных электродов, рассчитывают ЭДС гальванического элемента для различных концентраций E расч. = E катода – E анода. 15. Данные заносят в таблицу.
Рекомендуемый вид таблицы
Рис. Схема потенциометра:1–переключатель чувствительности; 2 – выходной прибор; 3 – переключатель рода работы; 4 – декадные переключатели; 5 – клеммы. Приложения
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-05-11; просмотров: 97; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 3.21.104.72 (0.005 с.) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
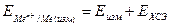 ,
,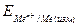 – потенциал электрода относительно стандартного водородного электрода;
– потенциал электрода относительно стандартного водородного электрода;  – потенциал хлоридсеребряного электрода относительно стандартного водородного электрода. Потенциал ХСЭ электрода принимают равным 197мВ.
– потенциал хлоридсеребряного электрода относительно стандартного водородного электрода. Потенциал ХСЭ электрода принимают равным 197мВ. 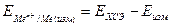 .
.