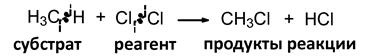Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Способы разрыва ковалентной связи
Гомолитический (свободнорадикальный)
Гомолиз связи v Образующиеся промежуточные частицы – свободные радикалы Гетеролитический (ионный)
Гетеролиз связи v Образующиеся органические промежуточные частицы - карбокатионы (с положительным зарядом на атоме углерода) или - карбоанионы (с отрицательным зарядом на атоме углерода)
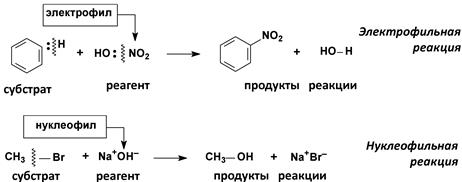
Классификация реакций 1. По характеру изменения связей в субстрате и реагенте (а) Гомолитические реакции
(б) Гетеролитические реакции
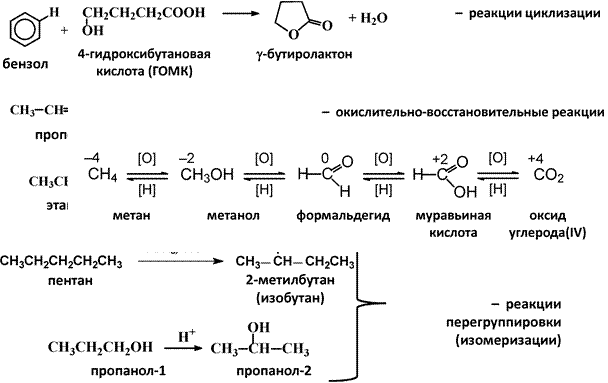
2. По направлению (конечному результату)
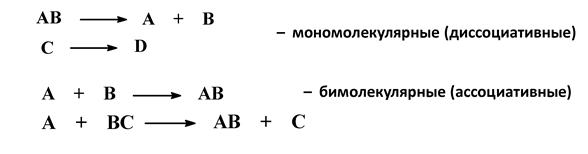
v Изменение степени окисления углерода, выступающего в роли 3. По числу молекул (частиц), участвующих в стадии, определяющей общую скорость реакции
Методики выполнения общих качественных реакций Реакции идентификации кратной связи (двойной, тройной) Бромирование бромной водой В пробирку поместите 2 капли бромной воды, добавьте 2–3 капли исследуемого раствора, встряхните пробирку. Внешние признаки: Наблюдается обесцвечивание желтого раствора бромной воды. 2. Реакция гидроксилирования (реакция Вагнера) В пробирку поместите 2 капли 0,1н KMnO4, добавьте 2–3 капли исследуемого раствора, встряхните пробирку. Внешние признаки: Наблюдается обесцвечивание розового раствора KMnO4 и выпадение бурого осадка MnO2. Реакция идентификации многоатомных спиртов В пробирку поместите 3 капли 0,2н CuSO4, 3 капли 2н NaOH. К образовавшемуся осадку Cu (OH)2 добавьте 1 каплю исследуемого соединения. Внешние признаки: Происходит растворение голубого осадка гидроксида меди с образованием комплексной соли меди тёмно–синего цвета. Опыт следует проводить в избытке щёлочи. Идентификация первичных и вторичных спиртов Реакцией окисления бихроматом калия в кислой среде В пробирку поместите 2 капли исследуемого спирта, добавьте 1 каплю 2н H2SO4 и 2 капли 0,5н K2Cr2O7. Полученный раствор нагрейте над пламенем спиртовки. Внешние признаки: Происходит изменение цвета в синевато–зелёный. Охладите пробирку и добавьте 1–2 капли раствора фуксинсернистой кислоты, если появляется розово-фиолетовое окрашивание, то продуктом окисления является альдегид: следовательно, исходный спирт был первичным. Если не наблюдается изменения окраски фуксинсернистой кислоты – то исходный спирт был вторичным. Третичные спирты в этих условиях не окисляются.
Реакция идентификации фенольного гидроксида В пробирку поместите 1 каплю 1% раствора фенола, добавьте 1 каплю 0,1н FeCl3. Внешние признаки: Наблюдается сине–фиолетовое окрашивание комплексной соли железа.
|
||||||||
|
Последнее изменение этой страницы: 2021-04-04; просмотров: 102; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.220.13.70 (0.004 с.) |