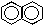Заглавная страница Избранные статьи Случайная статья Познавательные статьи Новые добавления Обратная связь КАТЕГОРИИ: ТОП 10 на сайте Приготовление дезинфицирующих растворов различной концентрацииТехника нижней прямой подачи мяча. Франко-прусская война (причины и последствия) Организация работы процедурного кабинета Смысловое и механическое запоминание, их место и роль в усвоении знаний Коммуникативные барьеры и пути их преодоления Обработка изделий медицинского назначения многократного применения Образцы текста публицистического стиля Четыре типа изменения баланса Задачи с ответами для Всероссийской олимпиады по праву 
Мы поможем в написании ваших работ! ЗНАЕТЕ ЛИ ВЫ?
Влияние общества на человека
Приготовление дезинфицирующих растворов различной концентрации Практические работы по географии для 6 класса Организация работы процедурного кабинета Изменения в неживой природе осенью Уборка процедурного кабинета Сольфеджио. Все правила по сольфеджио Балочные системы. Определение реакций опор и моментов защемления |
Якісні реакції на феноли та нафтоли
В окремі пробірки налити по ≈2 мл розведених розчинів фенолу, гідрохінону, резорцину, пірокатехіну, α- та β-нафтолів і додати до кожної пробірки по 2-3 краплі 3%-ного розчину FeCl3. За результатами спостережень заповнити таблицю:
Розчинність фенолу в воді Помістити в пробірку 0,5-1 г кристалічного фенолу і додати 3-4 мл води, струснути пробірку кілька разів і поставити в штатив на 2-3 хвилини. При цьому суміш розшаровується на фенол (нижній шар) і розчин фенолу в воді. Обережно нагріти суміш і знову охолодити. Записати і пояснити спостереження.
Кислотні властивості фенолу а)Пробірку з сумішшю із досліду 1 струснути до утворення емульсії і додавати краплями 10%-ний розчин NaОН до повного розчинення фенолу. Записати спостереження, молекулярне та йонно-молекулярне рівняння реакції, назвати продукти. Одночасно в іншу пробірку налити кілька крапель (0,5-0,6 мл) н-бутанолу або пентанолу і також додавати 10%-ний розчин NaОН. Чому в цій пробірці розчин не стає прозорим? б)Через розчин натрій феноляту, одержаний в досліді 3а, пропускати вуглекислий газ з апарату Кіппа до припинення змін. Записати спостереження, молекулярне та йонно-молекулярне рівняння реакції, назвати продукти. Порівняти кислотність спиртів, фенолу та карбонатної кислоти.
Бромування фенолу Набрати в пробірку ≈2 мл розведеного розчину фенолу і краплями при струшуванні додавати бромної води доти, доки рідина в пробірці не набуде жовтуватого відтінку. Записати спостереження та рівняння реакції.
6. Нітрування фенолу В плоскодонну конічну колбочку на 50-100 мл налити 10 мл концентрованої HNO3, додати 4мл води і обережно, краплями при струшуванні колби, додати ≈2 мл рідкого (розплавленого) фенолу. Колбу струшувати ще 2-3 хвилини, після чого продукти реакції вилити в склянку з холодною водою. Записати спостереження та рівняння реакції, назвати продукти.
Лабораторна робота № 6. ДОБУВАННЯ ТА ВЛАСТИВОСТІ АЛІФАТИЧНИХ АЛЬДЕГІДІВ ТА КЕТОНІВ
ЕКСПЕРИМЕНТАЛЬНА ЧАСТИНА 1. Добування альдегідів окисненням первинних спиртів Зібрати прилад, наведений на рис. 3.1. В колбу Вюрца налити ≈10 мл хромової суміші, помістити кілька крупинок пемзи або битого фарфору і додати 3-4 мл етанолу. В пробірку-приймач, поміщену в склянку з холодною водою, налити 2-3 мл води, занурити в неї газовідвідну трубку і обережно нагрівати колбу. Оцтовий альдегід, про утворення якого свідчить характерний запах, збирається в пробірці з водою. Записати спостереження, рівняння реакції, назвати продукти. Розчин альдегіду зберегти для наступних дослідів. Добування ацетону Зібрати прилад, показаний на рис. 3.1. В висушену колбу Вюрца помістити 5-10 г безводного кальцій ацетату, закрити її пробкою з термометром, а газовідвідну трубку занурити в пробірку-приймач, в яку заздалегідь налити 3-4 мл холодної води. Нагрівати колбу на газовому пальнику, спочатку обережно, а потім сильно, до обвуглення солі і виділення летких продуктів. Через кілька хвилин, коли об’єм розчину в пробірці-приймачі збільшиться приблизно вдвічі, припинити нагрівання. Якщо одержаний розчин каламутний, його треба відфільтрувати. Записати спостереження, рівняння реакції. Розчин ацетону зберегти для наступних дослідів.
Якісні реакції на альдегіди 1. Відновлення альдегідами купрум(ІІ) гідроксиду. Налити в пробірку 1-2 мл 10%-ного розчину NaOH і додавати краплями при струшуванні 2%-ного розчину CuSO4 до утворення осаду (помутніння розчину). Додати до суміші 1-2 мл розчину, одержаного формаліну, струснути пробірку, нахилити її і обережно нагрівати на газовому пальнику тільки верхню половину суміші. Нижня половина по можливості повинна залишатись холодною для порівняння. Записати спостереження (зміну кольорів), рівняння реакцій, назвати продукти. 2. Відновлення альдегідами диаммінаргентум(ІІ) гідроксиду (реакція срібного дзеркала). В пробірку, вимиту хромовою сумішшю, лугом і дистильованою водою, налити 3-4 мл 1-ного розчину аргентум нітрату і додавати краплями при струшуванні 5%-ний розчин аміаку до розчинення осаду, який утворюється спочатку. До одержаного розчину додати 1-2 мл формаліну і помістити пробірку в водяну баню, нагріту до 65±50С. Через кілька хвилин записати спостереження та рівняння реакцій.
Реакція з реактивом Фелінга а) Приготування реактиву Фелінга. Змішати в пробірці рівні об’єми (по ≈1-2 мл) приготованих заздалегідь 0,25-молярного розчину CuSO4 та розчину, в 100 мл якого міститься 21 г сегнетової солі і 15 г NaOH. При цьому утворюється комплексна сіль (I) за рівнянням: CuSo4 + 2NaOH → Cu(OH)2 + Na2SO4
Аліфатичні альдегіди при нагріванні руйнують комплекс (І), відновлюючи Сu2+ до Cu2O (червоний або жовтий осад). б) До одержаного в п.а) реактиву Фелінга додати ≈1 мл формаліну і нагрівати пробірку до припинення змін, що спостерігаються. Записати спостереження та рівняння реакції.
Дія лугів на альдегіди В окремі пробірки налити по ≈2 мл оцтового альдегіду або формаліну, додати по 3-4 мл 20%-ного розчину NaOH і обережно нагрівати пробірки на газовому пальнику. Записати спостереження, пояснити, чому в одній з пробірок ніяких змін не спостерігається.
|
||||||||||||||||||||||||||||||||||
|
Последнее изменение этой страницы: 2021-03-09; просмотров: 73; Нарушение авторского права страницы; Мы поможем в написании вашей работы! infopedia.su Все материалы представленные на сайте исключительно с целью ознакомления читателями и не преследуют коммерческих целей или нарушение авторских прав. Обратная связь - 18.117.165.66 (0.007 с.) |